16. 溶液对于自然界中的生命活动和人类生产活动具有重要意义。
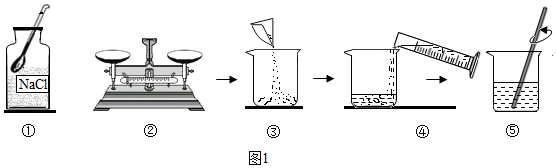
I.图1是某化学小组配制50g溶质质量分数为16%的氯化钠溶液的实验操作示意图,请回答下列问题:
(1)计算:配制该溶液需要氯化钠的质量为
_______g。
(2)称量(量取):
①校零后,若在称量时出现了天平指针右偏,右盘偏低的现象,按下来的操作应该是
________。(填序号)
A.调节平衡螺母
B.减少左盘中食盐
C.增加左盘中食盐
D.减少右盘中砝码
②配制溶液时应选择
______(填写“10”、“50”或“100”)mL量筒量取所需要的水(水的曾度是1.0g/cm
2)。
③若在量取水时俯视量筒凹液面的最低处,其它操作均正确的情况下,则所得溶液的溶质质量分数
________16%(选填“大于”、“等于”、“小于”之一)。
(3)溶解:⑤中溶解时玻璃棒的作用为
______。
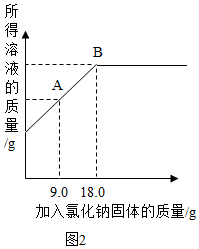
II.在0℃时,向质量为50g的水中不断加入氯化钠固体并搅拌,加入氯化钠的质量与所得溶液的质量关系如图2所示,请回答下列问题:
(4)A点时对应的溶液是氯化钠的
________溶液(选填“饱和”、“不饱和”、“无法确定”之一)。
(5)A点时所得溶液中大量存在的金属阳离子是
________(写离子符号)。
(6)20℃时,求B点所对应氯化钠溶液中溶质的质量分数。(写出计算过程结果,精确到0.1%)