2023年江苏省镇江市丹阳市中考模拟化学试题
江苏
九年级
模拟预测
2023-04-21
537次
整体难度:
适中
考查范围:
物质构成的奥秘、物质的化学变化、身边的化学物质、化学实验、化学与社会发展
2023年江苏省镇江市丹阳市中考模拟化学试题
江苏
九年级
模拟预测
2023-04-21
537次
整体难度:
适中
考查范围:
物质构成的奥秘、物质的化学变化、身边的化学物质、化学实验、化学与社会发展
一、选择题 添加题型下试题
选择题-单选题
|
较易(0.85)
解题方法
您最近一年使用:0次
选择题-单选题
|
较易(0.85)
解题方法
4. 下列做法不符合“健康、安全、绿色、舒适”生活理念的是
| A.低碳生活,节约能源 | B.健康饮食,低油少盐 |
| C.油锅着火,锅盖盖灭 | D.深埋电池,消除污染 |
您最近一年使用:0次
5. 下列归类正确的是
选项 | 归类 | 内容 |
| A | 常见的碱 | 氨水、烧碱、消石灰 |
| B | 金属材料 | 青铜、硬铝、玻璃钢 |
| C | 清洁能源 | 石油、氢能、太阳能 |
| D | 复合肥料 | 碳铵、尿素、硝酸钾 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
选择题-单选题
|
容易(0.94)
解题方法
6. 下图是配制50.0g10.0%NaCl溶液并测定其pH的部分操作,其中不规范的是
A.称量 | B.量取 |
C.溶解 | D.测pH |
您最近一年使用:0次
2022-05-08更新
|
261次组卷
|
7卷引用:2022年江苏省镇江市中考一模化学试题
选择题-单选题
|
适中(0.65)
解题方法
7. 下列实验方法正确的是
| A.用明矾使硬水转化为软水 | B.用灼烧方法区别羊毛线和棉纱线 |
| C.用50mL量筒量取6.5mL稀H2SO4 | D.用酚酞试液检验NaOH溶液是否变质 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
8. 下列排序正确的是
A.利用金属的年代: | B.铜元素质量分数: |
C.常见气体溶解性: | D.溶液的pH: |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
9. 下列指定反应的化学方程式正确的是
A.铝耐腐蚀性好的原因: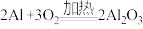 |
B.用磁铁矿炼铁: |
C.证明金属活动性Zn>Ag: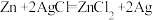 |
D.农业上配制液尔多液: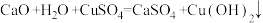 |
您最近一年使用:0次
2023-04-19更新
|
86次组卷
|
2卷引用:2023年江苏省镇江市丹阳市中考模拟化学试题
选择题-单选题
|
较易(0.85)
解题方法
10. 利用CH4和H2O进行催化重整制氢气,反应前后数观示意图如下。

下列说法正确的是

下列说法正确的是
| A.转化①是化合反应 | B.转化过程中共有四种氧化物 |
| C.转化②反应前后分子的个数不变 | D.甲、乙、丙中碳元素的质量分数依次升高 |
您最近一年使用:0次
选择题-单选题
|
较难(0.4)
解题方法
12. 利用下图装置研究NaHCO3的性质,下列说法不正确的是


| A.装置①中固体一直为白色 |
| B.装置②中固体变蓝,证明有H2O生成 |
| C.将装置③中改为CaCl2溶液,仍可证明有CO2生成 |
| D.取等质量NaHCO3和装置①中剩余固体,加入足量稀盐酸反应,都有气泡产生,且NaHCO3产生气体多 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
13. 下列物质的转化在给定条件下均能实现的是
A. |
B.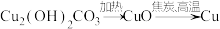 |
C. |
D.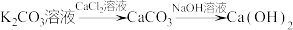 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
14. 下列实验操作能达到实验目的的是
选项 | 物质 | 目的 | 主要实验操作 |
A | CaO和NaOH固体 | 鉴别 | 取样,分别加适量水,测定所得溶液温度 |
B | KCl中混有KClO3 | 除杂 | 先加入适量二氧化锰,再加热至不再产生气体 |
C | CO2中是否混有SO2 | 检验 | 通入稀KMnO4溶液中,观察溶液是否褪色 |
D | KNO3和Ba(NO3)2的混合溶液 | 分离 | 先加入适量的K2SO4溶液,过滤、洗涤,再向滤渣中加入一定量稀HNO3,充分搅拌 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
选择题-单选题
|
较难(0.4)
15. 一种新型合成氨的方法如图所示(Li是一种金属)。下列说法不正确的是
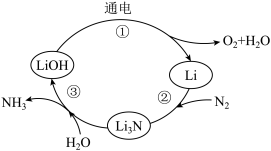
| A.反应①中电能转化为化学能 |
B.反应③为 |
| C.理论上,整个转化过程无需补充水 |
| D.理论上,合成17gNH3,同时得到24gO2 |
您最近一年使用:0次
2022-09-08更新
|
1933次组卷
|
22卷引用:2022年江苏省镇江市中考化学真题
2022年江苏省镇江市中考化学真题2023口袋书系列-专题07 化学计算公式-知识手册 提高练习2023中考一轮复习考点微专题-专题16 质量守恒定律、化学方程式-考点江苏省扬州市邗江区实验学校集团校2022-2023学年九年级下学期3月月考化学试题江苏省扬州市宝应县东北片2022-2023学年九年级下学期3月份纠错化学试题山东省济宁市第十三中学 2022-2023学年九年级下学期第一次月考化学试题2023年江苏省镇江市句容市华阳中学中考模拟化学试题(已下线)选择专练05 化学方程式的计算(25题)-2023年中考化学总复习高频考点必刷题(苏州专用)黑龙江省大庆市第六十九中学2022-2023学年九年级下学期4月月考化学试题2023年江苏省苏州市苏州高新区实验初级中学模拟化学试题2023年江苏省镇江市丹阳市中考模拟化学试题2023年江苏省无锡市滨湖区东绛实验学校中考模拟化学试题2023年江苏省苏州市张家港市梁丰初级中学中考一模化学试题(已下线)化学(江苏扬州卷)-【试题猜想】2023年中考考前最后一卷2023年江苏省扬州市广陵区中考二模化学试题山东省青岛市第三十九中学2023-2024学年九年级上学期12月月考化学试题江苏省扬州市邗江区梅苑双语学校2023-2024学年九年级下学期3月测试化学试卷江苏省镇江市丹徒区上会中学2023-2024学年九年级下学期3月月考化学试题2024年江苏省常州市武进区湖塘实验中学化学中考培优习题(一)2024年江苏省苏州市高新区中考化学模拟练习卷江苏省徐州市沛县第五中学2023-2024学年九年级下学期4月月考化学试题(已下线)专题14? 化学计算(七大题型)-2024年中考化学二轮热点题型归纳与变式演练(江苏通用)
选择题-单选题
|
适中(0.65)
解题方法
16. 下列说法正确的是
| A.纯净物一定是由同种分子构成 |
| B.氯化铵和草木灰混合使用,可提高肥效 |
| C.向鸡蛋清溶液中加入乙酸铅溶液,有固体折出,加水后固体溶解 |
| D.将燃着的镁条伸入某气体中,镁条继续燃烧,该气体不一定是氧气 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
17. 如图为KCl和Na2CO3的溶解度曲线,下判说法正确的是


| A.T2℃时,50gNa2CO3固体加入到50g水中,充分搅拌得100g溶液 |
| B.T3℃时,两物质饱和溶液的溶质质量分数都为42% |
| C.T4℃时,等质量的水能溶解KCl固体的质量比Na2CO3多 |
| D.T3℃两物质的饱和溶液降温到T1℃时,析出晶体的质量相等 |
您最近一年使用:0次
选择题-单选题
|
较难(0.4)
解题方法
18. 下列各组溶液,不用其它试剂就能鉴别出来的是
| A.CaCl2、AgNO3、HCl、Na2CO3 | B.BaCl2、Na2CO3、K2SO4、NaNO3 |
| C.KOH、H2SO4、CaSO4、HNO3 | D.FeCl3、Ba(OH)2、MgCl2、Na2SO4 |
您最近一年使用:0次
19. 向盛有100.0gCuSO4和H2SO4混合溶液的烧杯中,加入过量BaCl2溶液,充分反应后再滴加溶质质量分数为20.0%的NaOH溶液,烧杯中沉淀质量与滴加NaOH溶液质量的关系如图所示,已知V1:V2=2:3。下列说法正确的是

| A.加入NaOH溶液前,溶液中有两种溶质 |
| B.m=79.7 |
| C.原混合溶液中CuSO4与H2SO4的质量比为80:49 |
| D.取点对应溶液,滴加稀H2SO4,不能立即出现白色浑浊 |
您最近一年使用:0次
2023-04-19更新
|
528次组卷
|
4卷引用:2023年江苏省镇江市丹阳市中考模拟化学试题
2023年江苏省镇江市丹阳市中考模拟化学试题2023年福建省宁德市初中毕业班质量检测化学试题(已下线)易错类型16 技巧性计算“四大”方法-备战2024年中考化学考试易错题(全国通用)(已下线)压轴题08 技巧性化学计算-2024年中考化学压轴题专项训练(全国通用)
选择题-单选题
|
适中(0.65)
解题方法
20. 已知: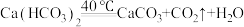 ,
,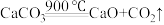 ,现有18.1gCaCO3和Ca(HCO3)2的混合物加热一段时间后剩余固体10.6g,并将气体通入足量澄清石灰水中,得到15.0g白色沉淀,下列说法不正确的是
,现有18.1gCaCO3和Ca(HCO3)2的混合物加热一段时间后剩余固体10.6g,并将气体通入足量澄清石灰水中,得到15.0g白色沉淀,下列说法不正确的是
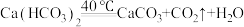 ,
,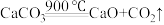 ,现有18.1gCaCO3和Ca(HCO3)2的混合物加热一段时间后剩余固体10.6g,并将气体通入足量澄清石灰水中,得到15.0g白色沉淀,下列说法不正确的是
,现有18.1gCaCO3和Ca(HCO3)2的混合物加热一段时间后剩余固体10.6g,并将气体通入足量澄清石灰水中,得到15.0g白色沉淀,下列说法不正确的是| A.剩余固体为混合物 |
| B.加热生成水的质量为0.9g |
| C.原固体中Ca(HCO3)2和CaCO3的质量比为81:50 |
| D.将剩余固体溶于足量稀盐酸所得溶液中CaCl2的质量为16.65g |
【知识点】 不含杂质的化学方程式计算解读
您最近一年使用:0次
二、填空与简答 添加题型下试题
填空与简答-填空题
|
适中(0.65)
名校
解题方法
21. 用化学符号表示。
(1)锌元素______ ;
(2)相对分子质量最小的氧化物______ ;
(3)氯化钠中的阳离子______ ;
(4)人体中缺少______ 元素,会导致甲状腺疾病。
(1)锌元素
(2)相对分子质量最小的氧化物
(3)氯化钠中的阳离子
(4)人体中缺少
您最近一年使用:0次
2023-04-19更新
|
260次组卷
|
2卷引用:2023年江苏省镇江市丹阳市中考模拟化学试题
22. 选择下列适当的物质填空(选填序号)。
A.干冰 B.食盐C.聚乙烯D.聚氯乙烯E.硫酸F.氧气G.熟石灰H.武德合会
(1)可用于人工降雨的是______ ;
(2)可用于食品包装的是______ ;
(3)可用于金属除锈的是______ ;
(4)可改良酸性土壤的是______ ;
(5)厨房中作调味品的是______ ;
(6)可用于制保险丝的是______ 。
A.干冰 B.食盐C.聚乙烯D.聚氯乙烯E.硫酸F.氧气G.熟石灰H.武德合会
(1)可用于人工降雨的是
(2)可用于食品包装的是
(3)可用于金属除锈的是
(4)可改良酸性土壤的是
(5)厨房中作调味品的是
(6)可用于制保险丝的是
您最近一年使用:0次
2023-04-19更新
|
116次组卷
|
3卷引用:2023年江苏省镇江市丹阳市中考模拟化学试题
填空与简答-填空题
|
适中(0.65)
解题方法
24. 化学促进体育、科学、文化等各项事业蓬勃发展。
(1)“双奥之城”北京成为奥运史上新的里程碑。
①国家速滑馆“冰丝带”采用当前最先进的二氧化碳跨临界直冷制冰技术,可实现CO2循环利用。该技术可有效缓解的环境问题是_______ 。
②水制成冰时,分子之间的间隔_______ (选填“变大”或“变小”)。
(2)中国航天员成功实现在空间站“天和”核心舱在轨驻留半年。

①偏二甲肼(C2H8N2)和N2O4可作火箭推进剂,此推进剂相互反应后生成CO2、H2O和一种常见单质_______ 。(填化学式)
②核心舱中采用含氢氧化锂(LiOH)的过滤器来消除呼出的CO2,生成Li2CO3和水。反应中LiOH和CO2的质量比为_______ 。
(3)“嫦娥五号”探测器带着月壤样品成功回落地球。月壤中含有钛铁矿(FeTiO3)、辉石(CaMgSi2O6)、橄榄石(MgFeSiO4)等。
①CaMgSi2O6用氧化物表示的组成为CaO·MgO·2SiO2,则MgFeSiO4用氧化物表示的组成为_____ 。
②硫酸钛[Ti(SO4)2]是制备钛的原料之一,工业上用FeTiO3与硫酸在加热条件下制备硫酸钛同时生成硫酸亚铁(反应过程中各元素化合价不变),反应的化学方程式为______ 。
(1)“双奥之城”北京成为奥运史上新的里程碑。
①国家速滑馆“冰丝带”采用当前最先进的二氧化碳跨临界直冷制冰技术,可实现CO2循环利用。该技术可有效缓解的环境问题是
②水制成冰时,分子之间的间隔
(2)中国航天员成功实现在空间站“天和”核心舱在轨驻留半年。

①偏二甲肼(C2H8N2)和N2O4可作火箭推进剂,此推进剂相互反应后生成CO2、H2O和一种常见单质
②核心舱中采用含氢氧化锂(LiOH)的过滤器来消除呼出的CO2,生成Li2CO3和水。反应中LiOH和CO2的质量比为
(3)“嫦娥五号”探测器带着月壤样品成功回落地球。月壤中含有钛铁矿(FeTiO3)、辉石(CaMgSi2O6)、橄榄石(MgFeSiO4)等。
①CaMgSi2O6用氧化物表示的组成为CaO·MgO·2SiO2,则MgFeSiO4用氧化物表示的组成为
②硫酸钛[Ti(SO4)2]是制备钛的原料之一,工业上用FeTiO3与硫酸在加热条件下制备硫酸钛同时生成硫酸亚铁(反应过程中各元素化合价不变),反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中(0.65)
解题方法
25. 以碳酸钡原料(含少量SiO2)制备高纯碳酸钡的流程如下。

(1)试剂X应选用______ (选填序号)。
a.稀H2SO4 b.盐酸
(2)操作1、操作2用到的玻璃仪器有烧杯、________ 、漏斗等。
(3)酸溶时,试剂X不能过量太多,一是节约试剂X,二是_______ 。
(4)洗涤时检验晶体已洗净的方法:取最后一次洗涤后的滤液,先滴加足量稀硝酸,再滴加______ (填化学式)溶液,无现象。

(1)试剂X应选用
a.稀H2SO4 b.盐酸
(2)操作1、操作2用到的玻璃仪器有烧杯、
(3)酸溶时,试剂X不能过量太多,一是节约试剂X,二是
(4)洗涤时检验晶体已洗净的方法:取最后一次洗涤后的滤液,先滴加足量稀硝酸,再滴加
您最近一年使用:0次
26. 二氧化氯(ClO2)是一种高效安全的消毒剂,可灭杀新型冠状病毒(2019—nCoV)。制备ClO2可由Na2SO3在H2SO4存在条件下与NaClO3反应制得,同时得到Na2SO4溶液。
(1)ClO2能杀菌消毒,该过程是______ (选填“物理”或“化学”)变化。
(2)写出上述反应的化学方程式______ 。
(1)ClO2能杀菌消毒,该过程是
(2)写出上述反应的化学方程式
【知识点】 化学变化与物理变化判断解读 化学方程式的书写解读
您最近一年使用:0次
三、实验题 添加题型下试题
实验题
|
适中(0.65)
解题方法
27. 请结合下图回答问题。

(1)仪器名称:①______ ,②______ 。
(2)用高锰酸钾制取氧气可选用装置A和____ (选填序号)组合,反应的化学方程式为______ ,试管中棉花团的作用是______ 。
(3)实验室制取CO2的化学方程式为_____ ,选用装置C相对于B的优点是_______ 。
(4)对实验室制取CO2反应后的滤液行探究。向滤液中逐滴加入Na2CO3溶液,用pH传感器连续监测,得到如图1的曲线图。

①滤液中溶质的成分是______ 。
②BC段的现象是______ 。
③DE段的pH几乎不变的原因是________ 。

(1)仪器名称:①
(2)用高锰酸钾制取氧气可选用装置A和
(3)实验室制取CO2的化学方程式为
(4)对实验室制取CO2反应后的滤液行探究。向滤液中逐滴加入Na2CO3溶液,用pH传感器连续监测,得到如图1的曲线图。

①滤液中溶质的成分是
②BC段的现象是
③DE段的pH几乎不变的原因是
您最近一年使用:0次
四、科学探究题 添加题型下试题
科学探究题
|
较难(0.4)
解题方法
28. 某兴趣小组对硫酸铜溶液与碱溶液的反应进行了探究。
I.向烧碱溶液中滴加适量硫酸铜溶液,产生蓝色固体,反应的化学方程式为_______ 。
II.向硫酸铜溶液中滴加适量氨水,产生绿色固体,对绿色固体作如下探究:
【资料】常见绿色固体有碱式碳酸铜[Cu2(OH)2CO3]和硫酸[Cu4(OH)6SO4],都不溶于水,都能与酸反应。
【分析】
(1)甲同学认为不可能是Cu2(OH)2CO3,并得到一致认同,理由是_______ 。
(2)乙同学进行了实验:取适量绿色固体,加入足量的_______ 溶液,振荡后滴加_______ 溶液,产生白色沉淀,则该固体是碱式硫酸铜。
III.继续滴加氨水,固体逐渐溶解,溶液变蓝色,经处理获得蓝色晶体。
【资料】该蓝色晶体为[Cux(NH3)y(H2O)z]SO4,在150℃下分解为硫酸铜、氨气和水。
【实验】取26.4g蓝色晶体用下图装置进行实验探究。

(1)控制温度在150℃持续加热一段时间,并持续通入N2,测得碱石灰增重3.6g。
(2)停止加热,冷却至室温,加入过量浓NaOH溶液,生成9.8g沉淀,证明NaOH溶液过量的方法:静置,向上层清液中滴加______ 溶液,无现象。
【结论】该蓝色晶体的化学式为______ 。
【讨论】若实验结束后未持续通N2,则测得[Cux(NH3)y(H2O)z]SO4中y的值_______ (选填“偏大”、“偏小”成“不变”)
I.向烧碱溶液中滴加适量硫酸铜溶液,产生蓝色固体,反应的化学方程式为
II.向硫酸铜溶液中滴加适量氨水,产生绿色固体,对绿色固体作如下探究:
【资料】常见绿色固体有碱式碳酸铜[Cu2(OH)2CO3]和硫酸[Cu4(OH)6SO4],都不溶于水,都能与酸反应。
【分析】
(1)甲同学认为不可能是Cu2(OH)2CO3,并得到一致认同,理由是
(2)乙同学进行了实验:取适量绿色固体,加入足量的
III.继续滴加氨水,固体逐渐溶解,溶液变蓝色,经处理获得蓝色晶体。
【资料】该蓝色晶体为[Cux(NH3)y(H2O)z]SO4,在150℃下分解为硫酸铜、氨气和水。
【实验】取26.4g蓝色晶体用下图装置进行实验探究。

(1)控制温度在150℃持续加热一段时间,并持续通入N2,测得碱石灰增重3.6g。
(2)停止加热,冷却至室温,加入过量浓NaOH溶液,生成9.8g沉淀,证明NaOH溶液过量的方法:静置,向上层清液中滴加
【结论】该蓝色晶体的化学式为
【讨论】若实验结束后未持续通N2,则测得[Cux(NH3)y(H2O)z]SO4中y的值
您最近一年使用:0次
五、填空与简答 添加题型下试题
填空与简答-填空题
|
较难(0.4)
解题方法
29. 既有一包白色固体,可能含有K2CO3、CuSO4、NaOH、Ba(OH)2、NaCl、(NH4)2SO4中的一种或几种,现做如下实验。
(1)取适量固体与熟石灰混合研磨加热,有氨味,则原固体中一定含有____ 。
(2)另取适量固体加水溶解,过滤得白色固体A和无色滤液B,则原固体一定不含____ 。
(3)取固体A,加入足量稀HCl,固体部分溶解,则原固体一定含有____ 。
(4)取少量滤液B,滴加酚酞溶液,呈红色;另取少量滤液B,滴入足量硝酸银溶液和稀硝酸,静置,取上层清液滴加AgNO3溶液,出现白色沉淀,则原固体中,____ 含(选填“一定”,“可能”或“一定不”,下同)NaOH,____ 含NaCl。
(1)取适量固体与熟石灰混合研磨加热,有氨味,则原固体中一定含有
(2)另取适量固体加水溶解,过滤得白色固体A和无色滤液B,则原固体一定不含
(3)取固体A,加入足量稀HCl,固体部分溶解,则原固体一定含有
(4)取少量滤液B,滴加酚酞溶液,呈红色;另取少量滤液B,滴入足量硝酸银溶液和稀硝酸,静置,取上层清液滴加AgNO3溶液,出现白色沉淀,则原固体中,
您最近一年使用:0次
六、综合应用题 添加题型下试题
综合应用题
|
较难(0.4)
30. 从古至今,铁及其化合物一直被人类广泛应用。
一、铁的冶炼和应用
(1)我国早在春秋战国时期就开始生产和使用铁器。
①深埋的古墓中有些铁器保存至今是因为_____ (选填序号)。
a.铁不活泼 b.密封缺氧 c.干燥少水
②胆矾为CuSO4晶体,《梦溪笔谈》中记载“熬胆矾铁釜久之亦化为铜”,用化学反应方程式表示其原理________________________ 。
(2)铁的化合物在现代更多领域发挥着重要作用。
①活性FeOOH可除去石油开采过程中的有害气体H2S,并获得S,原理如下。

吸收中生成的另一种物质的名称为______ ,再生时发生反应的化学方程式为_____ 。
②碳酸亚铁(FeCO3)可作补血剂,药片表面包裹着淀粉制作的糖衣,淀粉_____ (选填“属于”或“不属于”)糖类,服用药片后与胃酸反应生成______ 被人体吸收,促进血红蛋白生成。
二、铁的化合物制备
实验室利用废铁屑(含少量Fe2O3)为原料制备碳酸亚铁(FeCO3)的流程如下:

(3)酸溶时适当提高反应温度和H2SO4浓度,目的是_______ 。
(4)Fe粉可使“酸溶”产生的Fe2(SO4)3转化为FeSO4,该反应的化学方程式为_____ 。
(5)转化2中温度不宜过高的原因是______ 。
(6)在空气中灼烧FeCO3可获得颜料铁红(Fe2O3)和CO2,反应的化学方程式为_____ 。
三、铁的化合物含量测定
称取含FeCO3的Fe2O3样品21.8g,放入下图所示装置中通入CO,控温在300℃,加热至质量不再改变,测得剩余固体质量为19.6g。

资料:
①FeCO3在282℃分解为FeO。
②用CO还原Fe2O3炼铁的过程大致分为三个阶段:
阶段1:
阶段2:
阶段3:
继续向装置中通CO,分阶段升温,进行CO还原铁的氧化物,加热时测得剩余固体质量随温度变化的曲线如图所示。

(7)实验中观察到装置B中澄清石灰水变浑浊,写出反应的化学方程式_____ 。
(8)样品中Fe2O3的含量为______ %(精确到0.1%)。
(9)图中M点对应的a=_____ 。N点固体的成分及对应的质量为_____ 。
一、铁的冶炼和应用
(1)我国早在春秋战国时期就开始生产和使用铁器。
①深埋的古墓中有些铁器保存至今是因为
a.铁不活泼 b.密封缺氧 c.干燥少水
②胆矾为CuSO4晶体,《梦溪笔谈》中记载“熬胆矾铁釜久之亦化为铜”,用化学反应方程式表示其原理
(2)铁的化合物在现代更多领域发挥着重要作用。
①活性FeOOH可除去石油开采过程中的有害气体H2S,并获得S,原理如下。

吸收中生成的另一种物质的名称为
②碳酸亚铁(FeCO3)可作补血剂,药片表面包裹着淀粉制作的糖衣,淀粉
二、铁的化合物制备
实验室利用废铁屑(含少量Fe2O3)为原料制备碳酸亚铁(FeCO3)的流程如下:

(3)酸溶时适当提高反应温度和H2SO4浓度,目的是
(4)Fe粉可使“酸溶”产生的Fe2(SO4)3转化为FeSO4,该反应的化学方程式为
(5)转化2中温度不宜过高的原因是
(6)在空气中灼烧FeCO3可获得颜料铁红(Fe2O3)和CO2,反应的化学方程式为
三、铁的化合物含量测定
称取含FeCO3的Fe2O3样品21.8g,放入下图所示装置中通入CO,控温在300℃,加热至质量不再改变,测得剩余固体质量为19.6g。

资料:
①FeCO3在282℃分解为FeO。
②用CO还原Fe2O3炼铁的过程大致分为三个阶段:
阶段1:

阶段2:

阶段3:

继续向装置中通CO,分阶段升温,进行CO还原铁的氧化物,加热时测得剩余固体质量随温度变化的曲线如图所示。

(7)实验中观察到装置B中澄清石灰水变浑浊,写出反应的化学方程式
(8)样品中Fe2O3的含量为
(9)图中M点对应的a=
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:物质构成的奥秘、物质的化学变化、身边的化学物质、化学实验、化学与社会发展
试卷题型(共 30题)
题型
数量
选择题
20
填空与简答
7
实验题
1
科学探究题
1
综合应用题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 纯净物和混合物的判断 | 单选题 |
| 2 | 0.85 | 化学变化与物理变化判断 缓慢氧化 蒸发 | 单选题 |
| 3 | 0.85 | 化学性质和物理性质 金刚石的相关知识 金属与氧气反应 碳酸氢钠、碳酸钠、碳酸钙 | 单选题 |
| 4 | 0.85 | 二氧化碳对生活环境的影响 对人体健康危害的物质 灭火原理与方法 水体的污染及保护 | 单选题 |
| 5 | 0.65 | 合金的认识 常见盐的俗名、用途 常见化肥的种类及性质 化石燃料的形成及现状 | 单选题 |
| 6 | 0.94 | 浓溶液稀释配制一定质量分数溶液 溶液的酸碱性的判断与pH的测定 | 单选题 |
| 7 | 0.65 | 硬水的危害及软化方法 强碱露置在空气中的变质 羊毛、合成纤维、棉的鉴别 量筒的正确使用方法和注意事项 | 单选题 |
| 8 | 0.65 | 根据化学式计算元素质量分数 金属元素的存在 溶液酸碱性及pH相关关系 气体发生、收集装置 | 单选题 |
| 9 | 0.65 | 金属与氧气反应 金属与盐溶液反应 工业炼铁的原理及装置 盐类参与的反应 | 单选题 |
| 10 | 0.85 | 化合反应 氧化物的定义 微粒图像的分析及应用 根据化学式计算元素质量分数 | 单选题 |
| 11 | 0.65 | 复分解反应的定义 根据方程式推测化学式 常见的酸碱指示剂及其变色情况 常见盐的俗名、用途 | 单选题 |
| 12 | 0.4 | 不含杂质的化学方程式计算 二氧化碳的检验、验满及净化 碳酸氢钠、碳酸钠、碳酸钙 | 单选题 |
| 13 | 0.65 | 铁在氧气中燃烧及其实验 木炭还原氧化铜的实验 碱的通性 盐类参与的反应 | 单选题 |
| 14 | 0.65 | 氯酸钾制取氧气 生石灰的性质及用途 盐类参与的反应 物质鉴别——选用试剂鉴别 | 单选题 |
| 15 | 0.4 | 化学方程式的书写 不含杂质的化学方程式计算 化学反应中能量变化的实际应用 | 单选题 |
| 16 | 0.65 | 纯净物和混合物的判断 合理使用化肥和农药 蛋白质 燃烧的定义及条件 | 单选题 |
| 17 | 0.65 | 固体溶解度概念 固体溶解度曲线的应用 溶解度的相关计算 溶质质量分数的涵义 | 单选题 |
| 18 | 0.4 | 复分解反应发生的条件 酸的通性 盐类参与的反应 常见物质的颜色 | 单选题 |
| 19 | 0.15 | 有关质量守恒定律的计算 不含杂质的化学方程式计算 盐类参与的反应 | 单选题 |
| 20 | 0.65 | 不含杂质的化学方程式计算 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.65 | 离子符号的含义及书写 元素符号书写及含义 化学式书写及读法 人体内的微量元素——碘、铁元素 | 填空题 |
| 22 | 0.85 | 二氧化碳的用途 常见几种酸的用途 几种常见碱的物理性质及用途 常见盐的俗名、用途 | 填空题 |
| 23 | 0.85 | 浓硫酸的稀释 | 填空题 |
| 24 | 0.65 | 用质量守恒定律确定物质组成 化学方程式的书写 微粒的观点解释现象 二氧化碳对生活环境的影响 | 填空题 |
| 25 | 0.65 | 酸的通性 盐类参与的反应 常见酸碱盐的溶解性 过滤 | 流程题 |
| 26 | 0.65 | 化学变化与物理变化判断 化学方程式的书写 | 填空题 |
| 29 | 0.4 | 盐类参与的反应 几种常见阴、阳离子的鉴别 设计实验探究物质的成分 | 填空题 |
| 三、实验题 | |||
| 27 | 0.65 | 制取二氧化碳的原理 启普发生器原理及使用 溶液酸碱性及pH相关关系 盐类参与的反应 | |
| 四、科学探究题 | |||
| 28 | 0.4 | 化学方程式的书写 盐类参与的反应 设计实验探究物质的成分 | |
| 五、综合应用题 | |||
| 30 | 0.4 | 化学方程式的书写 含杂质的化学方程式计算 一氧化碳还原氧化铁实验 盐类参与的反应 | |

 ,下列说法正确的是
,下列说法正确的是


