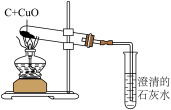
20. 化学兴趣小组应用如图所示的实验对课本中木炭还原氧化铜的反应机理进行了探究。
(1)实验中,同学甲观察到试管中黑色粉末变红,澄清石灰水
______。由此他认为反应生成了铜和二氧化碳。
【提出问题】同学乙提出了质疑:上述现象不能肯定产物一定是铜,也可能含有氧化亚铜(Cu
2O)。
【查阅资料】Cu
2O,为+1价铜的氧化物,红色粉末状固体,不溶于水,遇酸发生反应:
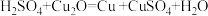
;
(2)【设计实验】取反应后的固体粉末少许于试管中,
_______(补充步骤及现象)。
【得出结论】产物中含有Cu
2O。
【新的问题】Cu
2O是如何产生的呢?
【原理探究】某大学课题组为化学兴趣小组提供了帮助:反应分两步进行:
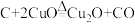
,

,可通过研究Cu
2O的产率来探究碳与氧化铜的反应机理。
【实验数据】课题组通过实验测得的数据如下表:
| 加热时间/min | 0.5 | 1 | 1.5 | 2 | 3 | 4 | 5 | 6 | 8 | 10 | 12 |
| Cu2O的产率/% | 19.7 | 23.8 | 24.3 | 21.7 | 19.2 | 15.4 | 10.7 | 6.9 | 3.2 | 1.7 | 0.8 |
| 产物性状 | 红色夹大量黑色粉末 | 红色夹少量黑色粉末 | 红色粉末 | 红色粉末 | 红色粉末 | 红色粉末 | 红色粉末 | 红色粉末 | 红色粉末 | 色粉末 | 色粉末 |
(3)【交流讨论】由上表数据可知,Cu
2O的产率随加热时间变化情况为
_______。
同学丙认为,老师在演示该实验时仅看到黑色粉末变红不能说明CuO被完全还原为Cu,原因是
_______。
(4)【实验改进】课题组建议老师做该实验时,采用带网罩的酒精灯加热以便缩短反应时间。网罩的作用是
_______。