18. 某学习小组在实验室制取CO
2气体的过程中,不慎用到了浓盐酸,导致制得的CO
2气体中混有氯化氢气体,他们设计了如下除去氯化氢气体并探究CO
2与过氧化钠(Na
2O
2)反应的实验。
查阅资料得知:过氧化钠(Na
2O
2)是一种淡黄色固体,能与CO
2、H
2O发生反应:
2 Na
2O
2+ 2 CO
2=2Na
2CO
3+ O
22 Na
2O
2+ 2 H
2O =4NaOH + O
2 ↑
请回答下列问题:
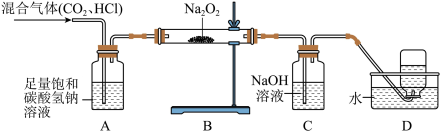
(1)装置A的作用是
___________________。
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含
_____________,该小组同学继续进行探究。
【提出问题】反应后硬质玻璃管中固体的成分是什么?
【做出猜想】猜想一: Na
2CO
3 猜想二: NaOH 猜想三: Na
2CO
3和NaOH
经过讨论,大家一致认为猜想
_____不合理,理由是
_________________。
【实验验证】小组同学取上述形成的溶液M于试管中,向其中加入过量的
________溶液,若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想三成立。
【交流反思】小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,你认为该同学的观点
_________(填“正确”或“错误”),理由是
_________________。
【拓展延伸】在盛有氯化铵(NH
4Cl)浓溶液的试管中,加入足量的过氧化钠(Na
2O
2)固体,有气泡产生,产生的气体是
_________________。