19. 甲、乙两同学对镁与盐酸反应进行系列研究。甲、乙两同学取一根镁条,首先用砂纸打磨除去
_____,观察到镁条的颜色
_____。
研究Ⅰ:镁与盐酸反应过程中的能量变化以及反应速率的变化。
(1)反应中试管外壁发烫,说明镁与稀盐酸反应是
_____反应(填“吸热”或“放热”),反应的化学方程式是
_____。
(2)实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,则t
1﹣t
2内反应速率逐渐加快的主要原因是
_____;
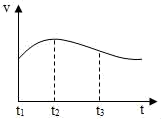
反思:t
2﹣t
3内反应速率逐渐减慢的主要原因是
_____;
研究Ⅱ:反应后所得溶液的酸碱性探究。
(3)用pH试纸测定反应后所得溶液的酸碱度,发现pH略小于7。
甲同学:猜想Ⅰ:稀盐酸过量;猜想Ⅱ:氯化镁溶液呈弱酸性。用pH试纸测定酸酸碱度的方法是
_____。为验证猜想Ⅱ正确,可以通过查阅资料,也可以取纯净的
_____溶液并测定其酸碱度。
(4)乙同学将镁片(有剩余)投入适量稀盐酸,待不再产生气泡时立即测量pH,却发现所得溶液pH大于7,溶液冷却到室温后pH小于7.查阅资料发现①Mg+2H
2O=Mg(OH)
2↓+H
2↑,②20℃时S
Mg(OH)2=0.009g,80℃时 S
Mg(OH)2=0.0108g。根据资料,乙同学实验中pH发生变化的原因是
_____。