【校级联考】山东省滨州市无棣县2019届九年级上学期期末考试化学试题
山东
九年级
期末
2019-03-12
275次
整体难度:
较易
考查范围:
物质的化学变化、身边的化学物质、化学实验、物质构成的奥秘、化学与社会发展
一、选择题 添加题型下试题
| A.用石块修筑长城 | B.指南针指到引航海 |
| C.用泥土烧制陶瓷 | D.在甲骨上刻文字 |
【知识点】 化学变化与物理变化判断解读
| A.氮气的化学性质不活泼,可用于食品的防腐 |
| B.燃烧法测定空气中氧气的含量,能用木炭代替红磷 |
| C.空气的成分按质量计算,氧气大约占21% |
| D.春节大量燃放烟花爆竹,不会造成空气污染 |

| A.该反应涉及到四种原子 |
| B.该反应属于置换反应 |
| C.该反应前后所有元素的化合价都没有变化 |
| D.参加反应的两种分子的个数比为1:1 |
| A.新装修的房子中有异味—分子在不断运动 |
| B.自行车轮胎在阳光下暴晒而炸裂—分子受热,体积变大 |
| C.水通电分解生成氢气和氧气—分子可以再分 |
| D.原子用扫描隧道显微镜才能观测到—原子的体积很小 |
| A.+1 | B.-1 | C.+5 | D.+7 |
【知识点】 化合价代数和的计算与应用解读
| A.二氧化碳,煤 | B.冰水混合物,五氧化二磷 |
| C.矿泉水,生理盐水 | D.净化后的空气,干冰 |
【知识点】 纯净物和混合物的判断解读
| A.硫在空气中燃烧,发出明亮的蓝紫色火焰 |
| B.将氢氧化钠溶液滴入氯化铜溶液,有蓝色沉淀物生成 |
| C.配制100g 10%的氯化钠溶液的主要步骤是计算、溶解、装瓶、贴标签 |
| D.10%的氯化钠溶液,倒出一半后,溶质质量分数变为5% |
| A.血浆(7.35~7.45) | B.胃液(0.9~1.5) |
| C.唾液(6.6~7.1) | D.胆汁(7.1~7.3) |
| A.海洛因和吗啡的组成元素不相同 |
| B.海洛因和吗啡充分燃烧,产物只有二氧化碳和水 |
| C.海洛因由21个碳原子、23个氢原子、1个氮原子和5个氧原子构成 |
| D.海洛因的相对分子质量是369 |

| A.试管1和试管2中气体质量比为2:1 |
| B.试管1和试管2中气体体积比为1:2 |
| C.该实验证明水是由氢原子和氧原子组成的 |
| D.试管2中的气体是氧气 |
【知识点】 电解水实验的现象和结论解读 电解水生成物的验证解读
 2X+8SO2,则X的化学式为
2X+8SO2,则X的化学式为| A.FeO | B.Fe2O3 | C.Fe3O4 | D.FeSO4 |
【知识点】 根据方程式推测化学式解读
| A.分子和原子在化学变化中都能够再分 |
| B.氧化物中一定含有氧元素,所以含有氧元素的化合物一定是氧化物 |
| C.分子、原子都是不带电的微粒,但不带电的微粒不一定都是分子、原子 |
| D.燃烧一般都伴随发光和放热现象,所以有发光放热现象的变化都是燃烧 |
| A.将燃烧的木条伸入到各集气瓶中 | B.测定气体的密度 |
| C.观察颜色、闻气味 | D.滴入紫色石蕊试液,振荡 |
【知识点】 氧气助燃性及实验解读 二氧化碳的检验、验满及净化解读
A.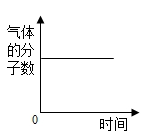 | B.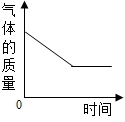 | C.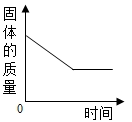 | D.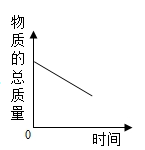 |
【知识点】 用质量守恒定律确定物质组成解读 碳单质的可燃性解读
| 物质 | A | B | C | D |
| 反应前质量/g | 18 | 1 | 3 | 32 |
| 反应后质量/g | 待测 | 26 | 3 | 12 |
| A.物质C一定是该反应的催化剂 | B.待测值为15 |
| C.参加反应的B、D的质量比为5:4 | D.该反应一定是分解反应 |
【知识点】 有关质量守恒定律的计算解读
二、填空与简答 添加题型下试题
(1)铝原子
(4)硝酸银溶液中滴加稀盐酸发生的化学方程式
(1)目前常见的化石燃料包括石油、天然气和煤,它们都属于
(2)氢气被视为21世纪最有发展的新型“绿色能源”原因是:因其制取原料来源广,燃烧放热大,
(3)天然气是一种重要的“非石油化”能源,请回答下列问题:
①甲烷与氧气构成的燃料电池中能量转化形式主要是
a 化学能转化为热能b 电能转化为化学能c 化学能转化为电能
②将CH4和CO2在一定条件下生成CO和H2时,该反应的重大意义是

(1)硒元素的相对原子质量为
(2)C原子在化学反应中易
(3)A和B两种元素的化学性质具有相似性的原因是它们原子的
(4)E粒子带1个单位负电荷,则
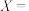
【知识点】 周期表信息示意图及结构示意图的综合考查解读

(1)P点的含义是
(2)t3℃时,20ga物质加入到50g水中不断搅拌,能形成70g溶液吗?
(3)t3℃时,a、b、c三种物质的溶解度按由大到小的顺序排列是
(4)将t1℃时,a、c两种物质饱和溶液的温度升高到t3℃时,两种溶液的溶质质量分数大小关系是
(5)图中阴影部分相对于a、c的溶液来说,分别代表
【知识点】 固体溶解度曲线的应用解读
三、计算题 添加题型下试题
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
| 反应后烧杯中物质的总质量/g | 36.4 | 59.6 | 83.8 | 108.8 |
(1)第1次加入稀盐酸充分反应后,生成二氧化碳的质量是______g。
(2)该贝壳样品中碳酸钙的质量。
【知识点】 含杂质的化学方程式计算解读 制取二氧化碳的原理解读
四、填空与简答 添加题型下试题
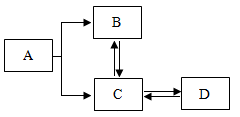
(1)写出物质B的化学式为
(2)由物质B转化为物质C,常用于燃烧的方法,该化学方程式为
(3)由物质C转化为物质D,常用于检验气体C,该化学方程式
(1)自来水、蒸馏水、海水中属于纯净物的是
(2)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:

①③对应的作用分别是
A 杀菌消毒 B 吸附杂质 C 沉淀过滤 D 蒸馏
(3)下列做法能减少水体污染的有
A 大量使用化肥、农药B 工业废气不经处理排放C 禁止使用含磷洗衣粉
(4)硬水给生活和生产带来很多麻烦,日常生活中通过
五、实验题 添加题型下试题

(1)写出仪器T的名称
(2)实验室若用过氧化氢溶液制取并收集氧气,选用的装置
(3)对比装置E和F,可以得出关于可燃物燃烧的条件是
六、科学探究题 添加题型下试题

【提出问题】用红磷燃烧的方法为什么测出的氧气含量远低于21%?
【分析讨论】(1)实验装置漏气;(2)
【实验改进】(1)如图2所示的实验装置进行实验探究。实验前在集气瓶里先装进a体积的水,其作用:一是为了加快集气瓶的冷却速度;二是
(2)如图3所示的实验装置进行实验探究。①在实验过程中,不断推拉注射器的目的是
②写出该实验中反应的化学方程式

③测得实验结果如下(气体体积):(单位:mL)
| 反应前玻璃管内 | 反应前注射器内 | 反应后注射器内 |
| 40 | 30 | 18 |
由此数据可以推算出他测定的空气中氧气的体积分数为
【实验结论】(1)研究空气的成分实验是在密封容器内进行。
(2)该物质在空气中可以燃烧且只与空气中的氧气反应。
(3)燃烧后的产物
试卷分析
试卷题型(共 25题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.94 | 空气各成分及其体积分数 空气中各成分的用途 空气的污染与防治 | 单选题 |
| 3 | 0.85 | 化学实验室安全规则 量筒的正确使用方法和注意事项 物质的加热 液体药品的取用 | 单选题 |
| 4 | 0.65 | 置换反应 微粒图像的分析及应用 常用化合价规律 | 单选题 |
| 5 | 0.94 | 微粒的观点解释现象 | 单选题 |
| 6 | 0.94 | 化合价代数和的计算与应用 | 单选题 |
| 7 | 0.85 | 纯净物和混合物的判断 | 单选题 |
| 8 | 0.85 | 硫在氧气中燃烧及其实验 溶液的基本特征 固体配制一定质量分数溶液 碱的通性 | 单选题 |
| 9 | 0.85 | 溶液的酸碱性的判断与pH的测定 酸碱性对生命活动和农作物生长的影响 | 单选题 |
| 10 | 0.85 | 用质量守恒定律确定物质组成 化学式、分子式及涵义 根据化学式计算相对分子质量 | 单选题 |
| 11 | 0.85 | 电解水实验的现象和结论 电解水生成物的验证 | 单选题 |
| 12 | 0.85 | 根据方程式推测化学式 | 单选题 |
| 13 | 0.85 | 氧化物的定义 分子、原子的区别与联系 燃烧的定义及条件 能量转化与化学变化的关系 | 单选题 |
| 14 | 0.94 | 氧气助燃性及实验 二氧化碳的检验、验满及净化 | 单选题 |
| 15 | 0.65 | 用质量守恒定律确定物质组成 碳单质的可燃性 | 单选题 |
| 16 | 0.65 | 有关质量守恒定律的计算 | 单选题 |
| 二、填空与简答 | |||
| 17 | 0.85 | 元素符号书写及含义 化学式书写及读法 酸的通性 | 填空题 |
| 18 | 0.94 | 氢能源的优点 资源综合利用和新能源开发的重要意义 化石燃料的形成及现状 | 简答题 |
| 19 | 0.85 | 周期表信息示意图及结构示意图的综合考查 | 填空题 |
| 20 | 0.85 | 固体溶解度曲线的应用 | 简答题 |
| 22 | 0.65 | 碳单质与二氧化碳的反应 碳及其化合物间相互转化 物质推断的综合应用 | 推断题 |
| 23 | 0.94 | 常见几种净化水操作的比较 硬水的危害及软化方法 爱护水资源 | 填空题 |
| 三、计算题 | |||
| 21 | 0.65 | 含杂质的化学方程式计算 制取二氧化碳的原理 | |
| 四、实验题 | |||
| 24 | 0.85 | 铁在氧气中燃烧及其实验 过氧化氢制取氧气实验 实验探究燃烧条件 | |
| 五、科学探究题 | |||
| 25 | 0.85 | 测定空气中氧气含量的实验误差分析 测定空气中氧气含量实验的改进 | |