26. 绿矾(FeSO
4·7H
2O)、硫酸亚铁铵[FeSO
4·(NH
4)
2SO
4·6H
2O]是重要的化工试剂。工业上常利用机械加工行业产生的废铁屑为原料制备绿矾、硫酸亚铁铵(如下图)。

已知:
(1)废铁屑中含有FeS等杂质,FeS+H
2SO
4=FeSO
4+H
2S↑,生成的H
2S气体有毒。
(2)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的小,冷却混合液至室温便析出硫酸亚铁铵。
(3)硫酸亚铁易被氧气氧化为硫酸铁,影响硫酸亚铁铵的等级。
请回答下列问题:
实验一:制备绿矾:
图Ⅰ中仪器①盛放的液体是
_____ ,除了发生的反应FeS+H
2SO
4=FeSO
4+H
2S↑外,还发生的另一个反应的化学方程式是
_____ 。广口瓶的作用是
_____ ,烧杯中主要的反应是CuSO
4+H
2S=CuS↓+H
2SO
4,硫酸铜溶液的作用是
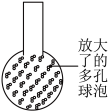
_____ ;此处烧杯中的导管最好换成多孔球泡,目的是
_____ 。
实验二:制备硫酸亚铁铵:
如图Ⅱ。实验步骤如下:
①连接仪器,
_____②制备FeSO
4溶液:先关闭止水夹A,再打开止水夹
_____ ,从分液漏斗滴入稀H
2SO
4至锥形瓶中。其中NaOH溶液中发生反应的化学方程式为
_____ ,此过程中氢气的作用是
_____ 。
③制备硫酸亚铁铵:待锥形瓶中的铁屑快反应完时,关闭止水夹
_____ ,打开止水夹
_____ ,不久会看到锥形瓶中的液体被压入饱和硫酸铵溶液中,放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵晶体。
实验三:对所制得的硫酸亚铁铵样品进行加热分析:
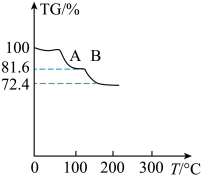
温度与TG%的关系如图所示,已知,200℃以前只有结晶水失去。[Mr(FeSO
4·(NH
4)
2SO
4·6H
2O)=392],已知:TG%=
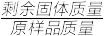
×100%。
TG%从100%降低为72.4%时,发生反应的化学方程式是
_____ 。试计算AB段物质的化学式
_____ (写出计算过程)。