19. 学习了碳单质的化学性质,知道碳与氧气反应能够生成CO
2或CO后,某学习小组同学联想到木炭粉与氧化铜发生反应可能有:①2CuO+C

2Cu+CO
2↑;②CuO+C

Cu+CO↑。他们想验证自己的想法,请你同他们一起进行探究。
【猜想与假设】
木炭粉与氧化铜反应生成的产物有三种可能:
(1)产物是铜和一氧化碳;
(2)产物是铜和二氧化碳;
(3)产物是
____________________。
【设计方案】
(1)检验产物中是否有CO
2的方法是
_____________________(用化学方程式表示)。
(2)如何检验产物是否存在CO,学习小组同学找查了资料: CO的特征反应是CO能使某种氯化钯的黄色混合液变蓝。
【实验结论】设计的实验装置(如图)
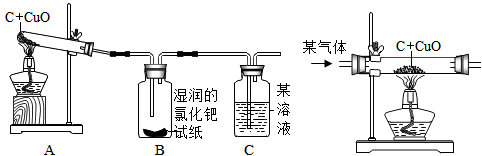
实验报告:
| 实验现象 | 实验结论 |
| ①A中________________ | ①有铜生成 |
| ②B中黄色试纸变蓝 | ②有______________生成 |
| ③C中_______________ | ③有CO2生成 |
【反思与评价】
(1)实验结束时,为防止Cu被氧化,必须先停止加热,待Cu冷却后再将试管口的胶塞取下,因此,若没有B瓶,可能导致的后果是
__________________。
(2)从环保角度看,如图装置有缺陷,怎么办?
___________________。
(3)检验生成的气体中是否含有CO,也可以将混合气体通过灼热的氧化铜粉末,看黑色固体是否会逐渐变红,写出相关反应的化学方程式
_____________________。
【拓展与延伸】
(1)若采用如图装置代替图中A装置,既可排尽试管中的空气,还可以将反应产生的气体赶出来,那么通入的“某气体”是什么?
________________________。
(2)假若24.4g木炭粉与氧化铜混合物充分反应后,只生成二氧化碳气体,且反应后剩余固体质量为20g。求剩余固体中金属铜的质量分数
__________________。