广东省深圳市盐田区深圳外国语学校2020-2021学年九年级上学期第三次月考化学试题
广东
九年级
阶段练习
2020-12-27
344次
整体难度:
容易
考查范围:
物质的化学变化、身边的化学物质、化学与社会发展、物质构成的奥秘、化学实验
一、选择题 添加题型下试题
A.光合作用 | B.金属导电 |
C.钢铁生锈 | D.蜡烛燃烧 |
【知识点】 化学变化与物理变化判断解读 金属的物理通性与用途解读 钢铁的锈蚀解读
| A.生活垃圾分类放置,处理 | B.用自备的布袋取代塑料袋购物 |
| C.合理施用化肥和农药 | D.工业废水无需处理直接排放 |
| A.氢气、干冰、大理石 | B.天然气、锰酸钾、澄清石灰水 |
| C.活性炭、氯化氢、洁净的空气 | D.金刚石、稀有气体、氯化钠 |
【知识点】 纯净物和混合物的判断解读 单质和化合物的判断解读
| A.氧气的使用要远离火源,因为氧气可燃烧 |
| B.水中鱼类能生存,是因为水中会溶解少量氧气 |
| C.氧气可支持植物的光合作用 |
| D.铁丝在氧气中燃烧,产生耀眼的白光和红色固体 |
| A.一氧化碳和二氧化碳的化学性质不同,是因为分子结构不同 |
| B.金刚石和石墨的物理性质不同,是因为原子的核外电子数不同 |
| C.碳元素和氧元素的种类不同,是因为原子的质子数不同 |
| D.钠原子和钠离子的化学性质不同,是因为钠原子和钠离子的最外层电子数不同 |
| A.自来水厂净水的方法主要有沉淀、过滤、吸附和蒸馏 |
| B.保持水的化学性质的最小粒子是水分子 |
| C.生活中将硬水软化的方法通常是煮沸 |
| D.水体污染的主要污染源是工业废水、农业污水和生活污水 |

| A.每个锂离子带1个单位的正电荷 | B.锂元素位于元素周期表的第一周期 |
| C.锂元素与镁元素化学性质相似 | D.锂离子电池放电时,电能转化成化学能 |
| A.金刚石和石墨都是由碳元素组成的 |
| B.长期未用而难开启的铁锁,可在锁孔中加入少量铅笔芯末作润滑剂 |
| C.石墨常用作电极是因为石墨熔点高且质软 |
| D.活性炭可用作防毒面具的滤毒剂 |
①原子数目;②分子数目;③元素种类;④物质种类;⑤原子种类;⑥物质的总质量;⑦分子种类;⑧元素化合价
| A.①③⑥⑧ | B.①③⑤⑥ | C.②④⑦⑧ | D.②④⑤⑦ |
【知识点】 质量守恒定律内容及适用范围解读 质量守恒定律的微观解释解读
| A.银元素:Au | B.S 2-的结构示意图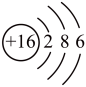 |
| C.氧化铁:FeO | D.钡离子:Ba2+ |
| A.一些元素可以形成多种离子 | B.同种元素的原子质量一定相等 |
| C.组成元素相同的纯净物不一定是同种物质 | D.元素的化学性质与原子的核外最外层电子数关系密切 |
| A.维生素P是由碳、氢、氧三种元素组成的混合物 |
| B.维生素P分子由27个碳原子、30个氢原子、16个氧原子构成 |
| C.维生素P中碳、氢、氧三种元素的原子个数比为162∶15∶128 |
| D.维生素P在足量的氧气中充分燃烧,产物为CO2和H2O |

| A.水中可加入少量硫酸钠以增强水的导电性 |
| B.a、b 两玻璃管中产生的气体质量之比是 2:1 |
| C.将燃着的木条放在 b 玻璃管尖嘴口,开启活塞,木条燃烧更旺 |
| D.由实验可知水由氢元素和氧元素组成 |
【知识点】 电解水实验的现象和结论解读 电解水生成物的验证解读

| A.反应物和生成物中共有3种氧化物 | B.该反应中,乙是氧化剂,具有氧化性 |
| C.反应中丙和丁的质量比为1∶1 | D.图中x的数值为4 |
| A.细铁丝燃烧实验中集气瓶底部放少量水——防止氧气受热逸出 |
| B.探究空气中氧气含量试验中红磷要足量——充分观察磷在空气中燃烧的现象 |
| C.实验室制取蒸馏水时在蒸馏瓶中放入沸石——加快蒸馏速度 |
| D.实验室用排水法收集氧气时等气泡均匀连续放出再收集——防止收集到的气体不纯 |
| A.元素是具有相同质子数的一类原子的总称,具有相同质子数的粒子一定是同种元素 |
| B.蜡烛在空气中燃烧后质量减小,说明不是所有化学反应都遵守质量守恒定律 |
| C.离子都带有电荷,但带电荷的微粒不一定是离子 |
| D.由同种分子构成的物质是纯净物,所以纯净物一定由同种分子构成 |
A.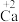 | B.Na+ | C.H | D.CO2 |
A.H2O2 H2↑+O2↑ H2↑+O2↑ | B.CO2+ Ca(OH)2 CaCO3+ H2O CaCO3+ H2O |
C.2Al+ O2 2AlO 2AlO | D.Zn+2HCl==ZnCl2+ H2↑ |
| A.微粒观:氯化钠是由氯化钠离子构成的 |
| B.转化观:石墨在一定条件下可以转化为金刚石属于化学变化 |
| C.结构观:红磷和白磷燃烧都生成五氧化二磷,因为它们是由同种分子构成的 |
| D.守恒观:1g 硫在 2g 氧气中充分燃烧生成 3g 二氧化硫 |
①可能是混合物 ②一定是氧化物
③可能是化合物 ④一定含氢分子
⑤可能是单质 ⑥在一定条件下可能有氧气产生
| A.①②③⑥ | B.①③④⑥ | C.①②③⑤ | D.①③⑥ |
| A.Na2O2要密封保存 | B.Na2O2中氧元素在反应后化合价未发生变化 |
| C.反应后固体质量增加 | D.R的化学式为CO2 |
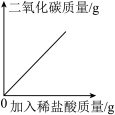 | 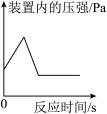 |  | 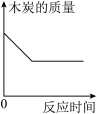 |
| A向一定量石灰石中滴加稀盐酸 | B在某一密闭装置内点燃红磷 | C加热一定量高锰酸钾固体 | D一定质量的木炭与过量氧气反应 |
| A.A | B.B | C.C | D.D |
| 构成物质的微粒 |  |  | M |  |  |
| 反应前的质量/g | 68 | 32 | 0 | 1 | |
| t 时刻的质量/g | 8 | x | |||
| 反应后的质量/g | 0 | 0 | y | 37 |
| A.X=16 |
| B.物质 M 中一定不含氧元素 |
C.此反应中, 与 与 的化学计量数之比为 2:1 的化学计量数之比为 2:1 |
D.若将表中 增加到 96g,则会生成 增加到 96g,则会生成 污染性气体 污染性气体 |
| 选项 | 实验目的 | 实验方案 |
| A | 探究石蜡中含有碳元素 | 用干冷的烧杯在蜡烛火焰上方,观察现象 |
| B | 鉴别铜粉与碳粉 | 分别加入足量水,观察是否溶解 |
| C | 除去 KCl 固体中的少量KClO3 | 加入少量的二氧化锰,加热 |
| D | 探究呼出气体与空气中氧气含量 | 燃着的小木条分别伸入两瓶气体中,观察现象 |
| A.A | B.B | C.C | D.D |

| A.碳片是一种混合物 | B.碳片和 C60是同一种物质 |
| C.在一定条件下,碳片可与二氧化碳反应 | D.碳片在氧气中完全燃的产物是CO |
| A.5:16 | B.20:73 | C.5:4 | D.80:73 |
【知识点】 根据化学方程式计算质量比解读

| A.CuO 和C 恰好完全反应 |
| B.t1和 t2时,固体中铜元素质量保持不变 |
| C.b 是残留固体的质量 |
| D.d 是二氧化碳的质量 |
【知识点】 有关质量守恒定律的计算解读 木炭还原氧化铜的实验解读
| A.110g | B.70g | C.88g | D.144g |
【知识点】 不含杂质的化学方程式计算解读
二、填空与简答 添加题型下试题

①若该微粒带2个单位负电荷,则微粒的化学符号为
②A、B两微粒的核外电子排布情况均如图,且能构成物质AB2,则AB2的化学式为
(2)①“文房四宝”之一的墨由炭黑中加入天然胶等制成。水墨画能长时间保存,是因为墨汁中的炭黑在常温时化学性质
②敦煌壁画色彩艳丽,矿物颜料功不可没,其蓝色源于石青[Cu3(OH)2(CO3)x]。石青中铜元素(+2价)与碳元素的质量比为
(1)氨气(NH3)在纯氧中完全燃烧,生成空气中含量最多的物质及一种生活中最常见的液体:
(2)淡黄色固体在空气中燃烧产生有刺激性气味的气体:
(3)实验室加热两种固体的混合物制取氧气:
(4)葡萄糖(化学式为 C6H12O6)在有适当催化剂的条件下,可转化成乙醇(C2H5OH)和二氧化碳:
三、实验题 添加题型下试题
(1)某小组在老师的指导下对药品的选用进行了如下探究。
按下表进行实验,取等质量的大理石加入足量酸溶液中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如图1 所示:
| 实验编号 | 药品 |
| Ⅰ | 块状大理石、10%盐酸溶液 |
| Ⅱ | 块状大理石、10%硫酸溶液 |
| Ⅲ | 大理石粉末、10%盐酸溶液 |

查阅资料:氯化钙易溶于水,硫酸钙微溶于水。
最终同学们确定用曲线乙对应的药品制备二氧化碳,相应的化学方程式是
(2)图甲为利用鸡蛋壳和白醋制取和收集二氧化碳的家庭实验装置。
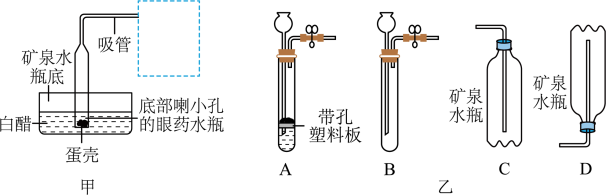
①带小孔的眼药水瓶下部可浸入和离开白醋,可以控制反应的进行与停止,它相当于乙图中的
②该装置线框中应选用乙图中的
③检验 CO2气体是否集满的方法是
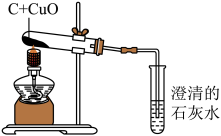
(1)木炭和氧化铜反应的化学方程式为
(2)证明碳具有还原性的实验现象是
(3)实验结束时,应先将弹夹夹紧连接导管的胶皮管,再熄灭酒精灯,这样操作的目的是
(4)小萱和小睿同学讨论后联想到单质碳的化学性质,认为在实验中还可能会有 CO 产生。
【查阅资料】CO 气体能使湿润的黄色氯化钯试纸变蓝色。
小温同学根据小萱和小睿同学的猜想,结合查阅的资料,改进了实验装置,如下:

实验过程中若观察到
(5)小温从环保角度考虑,认为小凡的实验装置可以做的改进是
【知识点】 木炭还原氧化铜的实验解读 污染性、可燃性尾气的处理解读
四、填空与简答 添加题型下试题

若丙为单质,则甲的化学式为
【知识点】 过氧化氢制取氧气实验解读 电解水原理解读

(1)C、D 的化学式分别是
(2)B→A 的化学方程式是
(3)A→C 的实验现象为
(4)图中变化属于化合反应的有
五、计算题 添加题型下试题

(1)生成氧气的质量是____g。
(2)列式计算该样品中过氧化钠的质量分数____。
【知识点】 含杂质的化学方程式计算解读
试卷分析
试卷题型(共 37题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 化学变化与物理变化判断 金属的物理通性与用途 钢铁的锈蚀 | 单选题 |
| 2 | 0.85 | 水体的污染及保护 “三废”处理 合理使用化肥与农药 | 单选题 |
| 3 | 0.94 | 纯净物和混合物的判断 单质和化合物的判断 | 单选题 |
| 4 | 0.85 | 物质与氧气反应的共性分析 氧气助燃性及实验 铁在氧气中燃烧及其实验 | 单选题 |
| 5 | 0.65 | 原子结构 最外层电子在化学变化中的作用 结构、性质与用途的关系 分子是保持物质化学性质的最小微粒 | 单选题 |
| 6 | 0.85 | 自来水厂净化过程 硬水的危害及软化方法 爱护水资源 分子是保持物质化学性质的最小微粒 | 单选题 |
| 7 | 0.65 | 原子结构示意图含义及应用 最外层电子在化学变化中的作用 原子结构示意图与元素在周期表中的位置相互推断 化学反应中能量变化的实际应用 | 单选题 |
| 8 | 0.94 | 同种元素组成的物质 金刚石的相关知识 石墨的相关知识 活性炭的吸附性 | 单选题 |
| 9 | 0.85 | 质量守恒定律内容及适用范围 质量守恒定律的微观解释 | 单选题 |
| 10 | 0.65 | 微粒结构示意图书写 离子符号的含义及书写 元素符号书写及含义 化学式书写及读法 | 单选题 |
| 11 | 0.94 | 纯净物和混合物的判断 基于构成原子的各微粒数值关系的计算 最外层电子在化学变化中的作用 元素的概念 | 单选题 |
| 12 | 0.65 | 质量守恒定律的微观解释 纯净物和混合物的判断 化学式、分子式及涵义 化学符号周围数字的含义 | 单选题 |
| 13 | 0.85 | 电解水实验的现象和结论 电解水生成物的验证 | 单选题 |
| 14 | 0.65 | 还原剂、氧化剂 根据化学方程式计算质量比 氧化物的定义 微粒图像的分析及应用 | 单选题 |
| 15 | 0.65 | 测定空气中氧气的含量实验的过程 铁在氧气中燃烧及其实验 高锰酸钾制取氧气实验 常见几种净化水操作的比较 | 单选题 |
| 16 | 0.65 | 质量守恒定律内容及适用范围 离子的概念及形成 物质化学性质的决定因素 元素的概念 | 单选题 |
| 17 | 0.65 | 离子符号的含义及书写 元素符号书写及含义 化学式、分子式及涵义 常见元素、原子团的化合价 | 单选题 |
| 18 | 0.94 | 化学方程式含义 过氧化氢制取氧气实验 二氧化碳与碱的反应及实验 金属与酸反应原理 | 单选题 |
| 19 | 0.65 | 化学变化与物理变化判断 根据化学方程式计算质量比 物质化学性质的决定因素 分子是保持物质化学性质的最小微粒 | 单选题 |
| 20 | 0.65 | 纯净物和混合物的判断 单质和化合物的判断 氧化物的定义 | 单选题 |
| 21 | 0.85 | 分解反应 | 单选题 |
| 22 | 0.65 | 根据方程式推测化学式 根据化学方程式计算质量比 化合价代数和的计算与应用 | 单选题 |
| 23 | 0.65 | 测定空气中氧气的含量实验的过程 制取氧气实验的图像问题 碳单质的可燃性 制取二氧化碳的原理 | 单选题 |
| 24 | 0.4 | 有关质量守恒定律的计算 用质量守恒定律确定物质组成 化学方程式的书写 | 单选题 |
| 25 | 0.65 | 氯酸钾制取氧气 金属的物理通性与用途 蜡烛燃烧的实验探究及产物分析 探究人体吸入和呼出气体成分 | 单选题 |
| 26 | 0.85 | 同种元素组成的物质 根据新信息判断碳单质的性质 碳单质与二氧化碳的反应 | 单选题 |
| 27 | 0.65 | 制取二氧化碳的装置 | 单选题 |
| 28 | 0.4 | 根据化学方程式计算质量比 | 单选题 |
| 29 | 0.65 | 有关质量守恒定律的计算 木炭还原氧化铜的实验 | 单选题 |
| 30 | 0.65 | 不含杂质的化学方程式计算 | 单选题 |
| 二、填空与简答 | |||
| 31 | 0.65 | 原子结构示意图含义及应用 根据化学式计算元素质量比 化合价代数和的计算与应用 碳单质的稳定性 | 填空题 |
| 32 | 0.85 | 化学方程式的书写 | 填空题 |
| 35 | 0.85 | 过氧化氢制取氧气实验 电解水原理 | 推断题 |
| 36 | 0.85 | 铁在氧气中燃烧及其实验 制取二氧化碳的原理 电解水原理 物质推断的综合应用 | 推断题 |
| 三、实验题 | |||
| 33 | 0.65 | 制取二氧化碳的原理 制取二氧化碳的装置 制取二氧化碳原理的拓展 二氧化碳的检验、验满及净化 | |
| 34 | 0.85 | 木炭还原氧化铜的实验 污染性、可燃性尾气的处理 | |
| 四、计算题 | |||
| 37 | 0.65 | 含杂质的化学方程式计算 | |







