23. 化学是一门以实验为基础的学科,气体的制备是其中一种重要的实验。现有如下仪器供选。

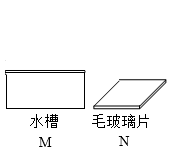
【实验一】用大理石(或石灰石)和稀盐酸制取CO
2。
(1)仪器A的名称是
_______,仪器C的名称是
_______。
(2)组装整套装置时,可选用图中的A、B、C、I、J、L、N和
_______。
(3)实验室制取CO
2气体反应的符号表达式为
_______,检验CO
2气体时常用到澄清的石灰水,该反应的符号表达式为
_______。
【实验二】实验室制取O
2并进行一系列探究。
【探究1】用高锰酸钾为原料制取并收集氧气
(1)该方法制取氧气的反应符号表达式为
_____;若选用排水集气法,组装整套装置时,伸入集气瓶口的导管应选择上图中的
____。
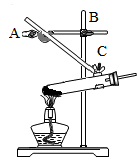
(2)某同学组装的发生装置如右图所示,其中有一处明显的错误,若要改正错误,需要操作的旋钮是
___(填字母)。
(3)某小组经实验测定,排水法收集的氧气平均浓度为89.7%,向上排空气法收集的氧气平均浓度为79.7%,对比排水法和向上排空气法,
_____法收集的氧气更纯净。用向上排空气法收集到的氧气浓度只有80%左右的原因有
_____。(填字母编号)
A 氧气的密度略大于空气的密度
B 加热高锰酸钾固体生成的氧气浓度只有80%左右
C 当观察到带火星木条复燃时,集气瓶内还有空气
D 当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
(4)某同学在实验室用高锰酸钾制氧气,加热一段时间后停止实验(高锰酸钾未完全分解),他测得剩余物质中两种金属元素的质量分数分别为:锰元素质量分数11.0%,钾元素的质量分数39.0%,请问剩余物质中氧元素的质量分数为
____。(填字母编号)
A 4%
B 14.5%
C 25.5%
D 50%
【探究2】对H
2O
2分解所用各种催化剂的催化效果进行定量对比探究
【小资料】海藻酸钠是一种天然高分子物质,在本实验中性质稳定。实验方案如下:
Ⅰ.用MnO
2、CuO、Fe
2O
3、Cr
2O
3四种催化剂分别与海藻酸钠混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO
2的海藻酸钠微球,采用左下图装置进行实验。改用其他三种微球,分别重复上述实验,得到锥形瓶内压强随时间变化的曲线图(下图)。


(1)用双氧水、二氧化锰为原料制取氧气的符号表达式为
_____,该反应属于
_____反应(填基本反应类型)。
(2)每次实验时,海藻酸钠微球数应相同的原因
_____。
(3)用含MnO
2的海藻酸钠微球进行实验,60s左右时压强瞬间回落,其原因是
_____。
(4)从实验曲线看,催化效果较好、反应较温和,过程较安全的催化剂是
_____。