将等质量的锌粉和铁粉,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答:

(1)金属X是______ ,判断的理由为______ 。
(2)从图中你还能获得的信息有______  答一条即可
答一条即可 。
。

(1)金属X是
(2)从图中你还能获得的信息有
 答一条即可
答一条即可 。
。
更新时间:2020-04-14 11:59:11
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】各种物质之间存在着某种联系。请分别选用“>”、“<”、“=”填写空白。
(1) 空气中元素含量:氧________ 氮;
(2) 核外电子数:钠离子________ 钠原子;
(3) 含碳量:甲醛 (CH2O)________ 葡萄糖(C6H12O6);
(4) 金属与稀盐酸反应的剧烈程度:锌片________ 铁片
(5) 铜丝在火焰上灼烧,灼烧后的“铜丝”质量________ 原铜丝的质量;
(6) 硬铝,其硬度__________ 铝的硬度。
(1) 空气中元素含量:氧
(2) 核外电子数:钠离子
(3) 含碳量:甲醛 (CH2O)
(4) 金属与稀盐酸反应的剧烈程度:锌片
(5) 铜丝在火焰上灼烧,灼烧后的“铜丝”质量
(6) 硬铝,其硬度
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】氧化锌(ZnO)俗称锌白,可用于湿疹、癣等皮肤病的治疗。工业级粗氧化锌(含有FeO、MnO、NiO等杂质)提纯为“锌白”的流程如图所示。
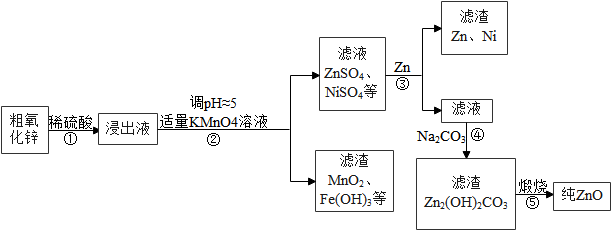
(1)已知步骤①中金属氧化物与硫酸反应生成盐和水。步骤①中主要发生反应的化学方程式为__________ 。
(2)步骤②中化合价发生变化的元素是___________ (填元素符号)。
(3)步骤③中化学反应基本类型为_______ 反应,金属活动性顺序中Zn应该排在Ni的_____ (填“前”或“后”)面。
(4)步骤④中滤液溶质的主要成分为___________ 。
(5)反应⑤的化学方程式为:Zn2(OH)2CO3 2ZnO+CO2↑+
2ZnO+CO2↑+__________ ;若在实验室中进行此反应,Zn2(OH)2CO3固体应放在______ (选填“坩埚” 或“蒸发皿”)中高温加热;从“碳达峰”和“碳中和”角度分析,吸收二氧化碳的试剂为_________ 。

(1)已知步骤①中金属氧化物与硫酸反应生成盐和水。步骤①中主要发生反应的化学方程式为
(2)步骤②中化合价发生变化的元素是
(3)步骤③中化学反应基本类型为
(4)步骤④中滤液溶质的主要成分为
(5)反应⑤的化学方程式为:Zn2(OH)2CO3
 2ZnO+CO2↑+
2ZnO+CO2↑+
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】镉(Cd)及其化合物在电镀、电池、颜料等领域中有广泛应用。镉是一种 “氢前金属 ”,金属活动性介于锌和铜之间 。镉元素常见化合价为 +2 。
某兴趣小组在探究金属化学性质时,将锌粉和镉粉的混合物加入到盛有一定量硝酸银溶液和硝酸铜溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。实验结果有图 1 、图 2 两种情况 。请回答下列问题:
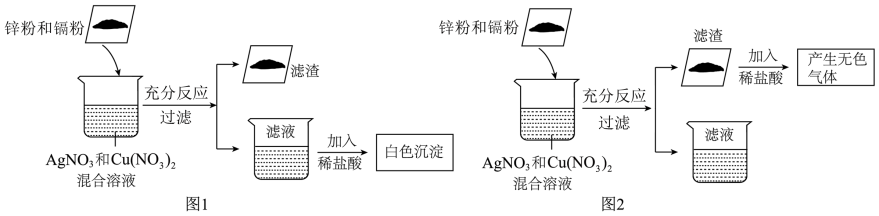
(1)图1是向滤液中加入稀盐酸,观察到有白色沉淀产生。滤液中一定含有的金属离子为______ (填离子符号)。
(2)图2是向滤渣中加入稀盐酸,观察到有无色气体产生。滤渣中一定含有______ (填化学式),滤液中可能含有______ (填化学式)。
某兴趣小组在探究金属化学性质时,将锌粉和镉粉的混合物加入到盛有一定量硝酸银溶液和硝酸铜溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。

(1)图1是向滤液中加入稀盐酸,观察到有白色沉淀产生。滤液中一定含有的金属离子为
(2)图2是向滤渣中加入稀盐酸,观察到有无色气体产生。滤渣中一定含有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】将锌粉加入到一定质量Mg(NO3)2、Cu(NO3)2、AgNO3的混合溶液中,充分反应后过滤,可以得到溶液和固体。
(1)写出一个可能发生反应的化学方程式_____
(2)若向固体中加入稀盐酸,有气泡产生,此时溶液中所含有的溶质是______
(3)若反应后溶液为蓝色,且反应前混合溶液质量与反应后过滤出的溶液质量相等,此时的固体成分是_____
(1)写出一个可能发生反应的化学方程式
(2)若向固体中加入稀盐酸,有气泡产生,此时溶液中所含有的溶质是
(3)若反应后溶液为蓝色,且反应前混合溶液质量与反应后过滤出的溶液质量相等,此时的固体成分是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】向一定量Cu(NO3)2、AgNO3和Al(NO3)3的混合溶液中加入一定量的Zn,充分反应后,过滤,可得到固体和溶液。
(1)请写出一定发生的反应的化学方程式:______ 。
(2)若反应后的溶液呈蓝色,向过滤出的固体中加入稀盐酸,一定_____ (选填“有”或“没有”)气体产生。
(3)若加入锌的质量和反应后过滤出的固体质量相等,则过滤后所得到的固体中一定含有______ 。
(1)请写出一定发生的反应的化学方程式:
(2)若反应后的溶液呈蓝色,向过滤出的固体中加入稀盐酸,一定
(3)若加入锌的质量和反应后过滤出的固体质量相等,则过滤后所得到的固体中一定含有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
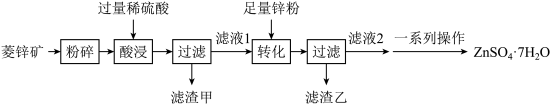
【推荐3】硫酸锌可制备各种含锌材料,在防腐、医学上有很多应用。菱锌矿的主要成分是ZnCO3,还含有少量的二氧化硅和氧化铁。以菱锌和为原料制备ZnSO4·7H2O的工艺流程如下图所示。(二氧化硅难溶于水,也不与稀硫酸反应)
(1)“酸浸”中观察到的现象是_________________ 。
(2)滤液1中含有的阳离子是_________________ 。(填离子符号)
(3)“转化”中加入足量锌粉,反应的化学方程式有: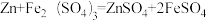 和
和_________________ (写一个即可)。
(4)下列说法正确的是 (填标号)。
(1)“酸浸”中观察到的现象是
(2)滤液1中含有的阳离子是
(3)“转化”中加入足量锌粉,反应的化学方程式有:
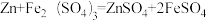 和
和(4)下列说法正确的是 (填标号)。
| A.“粉碎”是为了使菱锌矿在“酸浸”中与稀硫酸充分反应 |
| B.在“转化”中加入锌粉,若无气泡冒出,说明锌粉已足量 |
| C.滤渣甲、滤渣乙均能与稀硫酸反应产生气体 |
| D.滤液2的质量一定比滤液1的质量大 |
您最近一年使用:0次



