根据如图甲、乙两种物质的溶解度曲线回答相关问题:
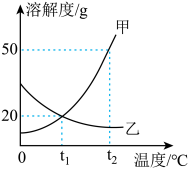
(1)常压下,CO2在水中的溶解度随温度的变化趋势类似于________ (填“甲”或“乙”)曲线。
(2) t2℃时若将75g甲的饱和溶液稀释成10%,需加水的质量为____________ 。
(3)将t2℃时,甲、乙两种物质的饱和溶液降温至t1℃(其他条件不变),所得溶液的溶质质量分数的关系是甲_________ 乙。(填“>”“<”或“=”)

(1)常压下,CO2在水中的溶解度随温度的变化趋势类似于
(2) t2℃时若将75g甲的饱和溶液稀释成10%,需加水的质量为
(3)将t2℃时,甲、乙两种物质的饱和溶液降温至t1℃(其他条件不变),所得溶液的溶质质量分数的关系是甲
更新时间:2020-04-30 11:12:18
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图甲是甲、乙、丙三种固体物质的溶解度曲线图。

(1)甲图中,P点所表示的含义为_______ ,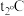 时,甲、乙、丙三种物质中,溶解度由小到大的关系是
时,甲、乙、丙三种物质中,溶解度由小到大的关系是_______ 。
(2)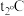 时,将50g的甲物质加到100g水中,充分搅拌后所得溶液的质量是
时,将50g的甲物质加到100g水中,充分搅拌后所得溶液的质量是_______ g。
(3)将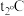 时甲、乙、丙三种物质的饱和溶液降温到
时甲、乙、丙三种物质的饱和溶液降温到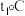 时三种物质的溶质质量分数由大到小的顺序是
时三种物质的溶质质量分数由大到小的顺序是_______ 。
(4)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为甲、乙、丙三种固体物质中的_______ 物质。
(5)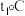 时,将乙物质的不饱和溶液转变成饱和溶液可采取的方法有
时,将乙物质的不饱和溶液转变成饱和溶液可采取的方法有_______ (写一种方法即可)。

(1)甲图中,P点所表示的含义为
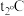 时,甲、乙、丙三种物质中,溶解度由小到大的关系是
时,甲、乙、丙三种物质中,溶解度由小到大的关系是(2)
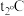 时,将50g的甲物质加到100g水中,充分搅拌后所得溶液的质量是
时,将50g的甲物质加到100g水中,充分搅拌后所得溶液的质量是(3)将
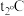 时甲、乙、丙三种物质的饱和溶液降温到
时甲、乙、丙三种物质的饱和溶液降温到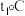 时三种物质的溶质质量分数由大到小的顺序是
时三种物质的溶质质量分数由大到小的顺序是(4)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为甲、乙、丙三种固体物质中的
(5)
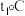 时,将乙物质的不饱和溶液转变成饱和溶液可采取的方法有
时,将乙物质的不饱和溶液转变成饱和溶液可采取的方法有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】我国化学家侯德榜所创立的侯氏制碱法,既提高了原料利用率,又可将产物氯化铵用作化学肥料,“变废为宝”,促进了世界制碱技术的发展。侯氏制碱法的部分工艺流程如下:
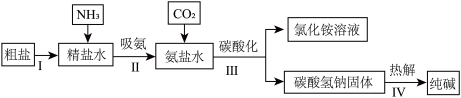
(1)步骤Ⅲ中先通入氨气形成饱和氨盐水,再加压通入二氧化碳,这样操作的目的是___________________ ,过滤后所得滤液是碳酸氢钠的__________ (填“饱和”或者“不饱和”)溶液,写出该步骤中发生反应的化学方程式______________________________ 。
(2)“侯氏制碱法”是在氨碱法基础上,向滤出碳酸氢钠晶体后的氯化铵溶液中加入食盐,使其中的氯化铵单独结晶析出用作_____ 肥,该化学肥料的作用是__________________ ,氯化钠溶液则可循环利用;相比“氨碱法制纯碱”,“侯氏制碱法”的优点有__________________ (填序号)。
a.用等量的食盐可以生产更多的纯碱,同时得到化肥氯化铵,NaCl的利用率高
b.不产生用途不大且难处理的 ,对环境更加友好
,对环境更加友好
c.侯氏制碱法中 可以循环使用,后续无须补充
可以循环使用,后续无须补充
(3)写出步骤Ⅳ中发生反应的化学方程式__________ 。
(4)如图是碳酸氢钠和氯化铵的溶解度曲线图。

① ℃碳酸氢钠的溶解度
℃碳酸氢钠的溶解度____ 氯化铵的溶解度(填“大于”“小于”或“等于”之一)。
② ℃时将25g氯化铵固体加入盛有50g水的烧杯中,充分溶解,得到的氯化铵溶液中溶质与溶液的质量比为
℃时将25g氯化铵固体加入盛有50g水的烧杯中,充分溶解,得到的氯化铵溶液中溶质与溶液的质量比为__________ (填最简整数比)。加热烧杯。使溶液升温至 ℃,此时该溶液的溶质质量分数是
℃,此时该溶液的溶质质量分数是__________ 。

(1)步骤Ⅲ中先通入氨气形成饱和氨盐水,再加压通入二氧化碳,这样操作的目的是
(2)“侯氏制碱法”是在氨碱法基础上,向滤出碳酸氢钠晶体后的氯化铵溶液中加入食盐,使其中的氯化铵单独结晶析出用作
a.用等量的食盐可以生产更多的纯碱,同时得到化肥氯化铵,NaCl的利用率高
b.不产生用途不大且难处理的
 ,对环境更加友好
,对环境更加友好c.侯氏制碱法中
 可以循环使用,后续无须补充
可以循环使用,后续无须补充
(3)写出步骤Ⅳ中发生反应的化学方程式
(4)如图是碳酸氢钠和氯化铵的溶解度曲线图。

①
 ℃碳酸氢钠的溶解度
℃碳酸氢钠的溶解度②
 ℃时将25g氯化铵固体加入盛有50g水的烧杯中,充分溶解,得到的氯化铵溶液中溶质与溶液的质量比为
℃时将25g氯化铵固体加入盛有50g水的烧杯中,充分溶解,得到的氯化铵溶液中溶质与溶液的质量比为 ℃,此时该溶液的溶质质量分数是
℃,此时该溶液的溶质质量分数是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】M、N两物质的溶解度曲线如图所示,回答下列问题:

(1)P点的含义是_____ 。
(2)将接近饱和的N溶液变为饱和溶液,可采用的方法_____ 。
(3)20℃时,将等质量的M、N两种固体,分别加入盛有等量水的A、B试管中,充分溶解后,可观察到如图所示的现象。则A试管中对应的物质是_____ ,此时,对A试管中物质进行如下操作,能使其溶液的溶质的质量分数一定发生变化的是_____ (填字母序号)。

a、加少量水 b、加入少量N物质 c、降温 d、恒温蒸发溶剂

(1)P点的含义是
(2)将接近饱和的N溶液变为饱和溶液,可采用的方法
(3)20℃时,将等质量的M、N两种固体,分别加入盛有等量水的A、B试管中,充分溶解后,可观察到如图所示的现象。则A试管中对应的物质是

a、加少量水 b、加入少量N物质 c、降温 d、恒温蒸发溶剂
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】我国科学家侯德榜为我国纯碱和氮肥工业技术的发展做出了杰出的贡献。如图是侯氏联合制碱法和西方索尔维制碱法的工艺流程。(已知, )
)

根据以上信息回答下列问题。
(1)盐水精制的过程是除去溶液中各种杂质的过程。为将盐水中含有的MgC12以沉淀除去,可以向其中加入过量的______ (填试剂名称)来除去。
(2)上述流程的侯氏联合制碱法中,可循环利用的物质是______ 。(写一种)
(3)氨碱工业最关键的一步是:在加压的条件下,不断向饱和的氨盐水中通入二氧化碳气体,溶液中会有碳酸氢钠晶体析出。试分析该流程需要“加压”的原因:______ 。
(4)在氨碱工业的历史上,如何处理流程中剩余的氯化铵溶液,出现了两种工艺:一是“索尔维法”,即在氯化铵溶液中加入物质X______ (填化学式),产生了可循环使用的氨气和大量固体废弃物氯化钙;二是我国化学家侯德榜发明的“联合制碱法”,即在氯化铵溶液中加入适量氯化钠晶体。降低了氯化铵的______ ,使氯化铵晶体单独析出得到另一种产品一一氮肥。
(5)在氨碱工业处理剩余的氯化铵溶液时,不直接加热蒸发结晶析出氯化铵固体的原因是:______ 。
 )
)
根据以上信息回答下列问题。
(1)盐水精制的过程是除去溶液中各种杂质的过程。为将盐水中含有的MgC12以沉淀除去,可以向其中加入过量的
(2)上述流程的侯氏联合制碱法中,可循环利用的物质是
(3)氨碱工业最关键的一步是:在加压的条件下,不断向饱和的氨盐水中通入二氧化碳气体,溶液中会有碳酸氢钠晶体析出。试分析该流程需要“加压”的原因:
(4)在氨碱工业的历史上,如何处理流程中剩余的氯化铵溶液,出现了两种工艺:一是“索尔维法”,即在氯化铵溶液中加入物质X
(5)在氨碱工业处理剩余的氯化铵溶液时,不直接加热蒸发结晶析出氯化铵固体的原因是:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】根据所学化学知识回答下列问题:
(1)“加铁酱油”可预防贫血,其中的“铁”是指_____ (填 “元素”或“原子”)。
(2)冰箱中放活性炭除去异味,这是利用了活性炭的_____ 性 。
(3)加热冷水,当温度尚未达到沸点时,水中常有气泡冒出的原因是_____ 。
(4)食醋是常用的调味品,一般含有 3%~5%的醋酸(化学式CH3COOH)。醋酸由_____ 种元素组成,0.1mol 醋酸中约含有_____ 个分子(用科学记数法表示)。
(5)实验是进行科学探究的重要方式。请根据图示回答问题:

Ⅰ.图1中细铁丝在氧气中燃烧时,加少量水的作用是_____ 。
Ⅱ.图2电解水可制取氢气,电极X为电源的_____ (填“正”或“负”) 极,反应的化学方程式为_____ ;氢气作为新能源,其主要优点为_____ (写出一点)。
Ⅲ.图3中试管A、B是对比实验,试管A中固体几乎不溶,试管B中固体全部溶解,该实验说明了影响物质溶解性的因素是_____ 。
(6)汽车尾气中含有许多有害气体,使用催化转换器可减少有害气体的排放,其中某一反应过程的微观变化如图所示。

I.该反应的化学方程式为_____ 。
II.物质丁中元素的存在形态为_____ (填“游离态”或“化合态”)。
(1)“加铁酱油”可预防贫血,其中的“铁”是指
(2)冰箱中放活性炭除去异味,这是利用了活性炭的
(3)加热冷水,当温度尚未达到沸点时,水中常有气泡冒出的原因是
(4)食醋是常用的调味品,一般含有 3%~5%的醋酸(化学式CH3COOH)。醋酸由
(5)实验是进行科学探究的重要方式。请根据图示回答问题:

Ⅰ.图1中细铁丝在氧气中燃烧时,加少量水的作用是
Ⅱ.图2电解水可制取氢气,电极X为电源的
Ⅲ.图3中试管A、B是对比实验,试管A中固体几乎不溶,试管B中固体全部溶解,该实验说明了影响物质溶解性的因素是
(6)汽车尾气中含有许多有害气体,使用催化转换器可减少有害气体的排放,其中某一反应过程的微观变化如图所示。

I.该反应的化学方程式为
II.物质丁中元素的存在形态为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水是一种重要的自然资源,爱护水资源,人人有责。

(1)如图所示电解水的实验中,需要在水中加入少量的Na2SO4,以增强___________ 。玻璃管b端连接电源的___________ 极。请写出电解水的化学方程式___________ 。
(2)自来水厂净水过程中,有时可利用明矾溶于水形成的胶状物对杂质的___________ ,使杂质沉降来来达到净水目的。
(3)如图是溶解度曲线。据图回答下列问题。

①图中P点表示___________ 。
②将t3℃时a、b、c三种物质的饱和溶液。降温到t1℃溶质质量分数由大到小是___________ 。

(1)如图所示电解水的实验中,需要在水中加入少量的Na2SO4,以增强
(2)自来水厂净水过程中,有时可利用明矾溶于水形成的胶状物对杂质的
(3)如图是溶解度曲线。据图回答下列问题。

①图中P点表示
②将t3℃时a、b、c三种物质的饱和溶液。降温到t1℃溶质质量分数由大到小是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】甲、乙、丙三种固体物质的溶解度曲线如下图所示。
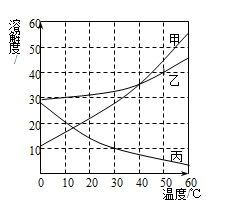
(1)20℃时,甲、乙、丙三种物质的溶解度由大到小的顺序为_____ 。
(2)20℃时,将50g乙物质放入100g水中充分溶解,所得溶液是_____ 溶液 填“饱和”或“不饱和”
填“饱和”或“不饱和” 。将此溶液升温至50℃,此时该溶液的溶质质量分数为
。将此溶液升温至50℃,此时该溶液的溶质质量分数为_____ 。(结果精确到0.1%)
(2)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数最小的是_____ (填“甲”、“乙”或“丙”)。

(1)20℃时,甲、乙、丙三种物质的溶解度由大到小的顺序为
(2)20℃时,将50g乙物质放入100g水中充分溶解,所得溶液是
 填“饱和”或“不饱和”
填“饱和”或“不饱和” 。将此溶液升温至50℃,此时该溶液的溶质质量分数为
。将此溶液升温至50℃,此时该溶液的溶质质量分数为(2)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数最小的是
您最近一年使用:0次




