我国的煤炭资源丰富,但液体燃料短缺。通过“煤液化”技术,用煤炭和水制取甲醇(CH3OH)对我国具有重要意义。主要流程如下:

(1)合成塔中发生的化学反应的微观示意图如下,请在方框内补全相应微粒的图示_____ 。
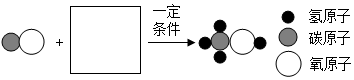
(2)下列关于甲醇生产的说法中,合理的是_____ (填字母序号)
A根据信息推测,甲醇是一种液体燃料
B煤炭与水在常温下即可生成CO和H2
C甲醇的生产会受到CO和H2比例的影响
(3)乙醇燃烧时发生反应: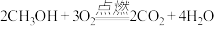 若甲醇燃料的质量为32t,则完全燃烧时消耗氧气的质量为
若甲醇燃料的质量为32t,则完全燃烧时消耗氧气的质量为_____ t。

(1)合成塔中发生的化学反应的微观示意图如下,请在方框内补全相应微粒的图示

(2)下列关于甲醇生产的说法中,合理的是
A根据信息推测,甲醇是一种液体燃料
B煤炭与水在常温下即可生成CO和H2
C甲醇的生产会受到CO和H2比例的影响
(3)乙醇燃烧时发生反应:
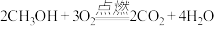 若甲醇燃料的质量为32t,则完全燃烧时消耗氧气的质量为
若甲醇燃料的质量为32t,则完全燃烧时消耗氧气的质量为
更新时间:2020-05-20 14:28:04
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】用“ ”和“
”和“ ”分别表示氮原子和氧原子,下图是氮气与氧气在放电条件下发生反应的微观模拟图。请回答下列问题:
”分别表示氮原子和氧原子,下图是氮气与氧气在放电条件下发生反应的微观模拟图。请回答下列问题:

(1)该反应的方程式为______ ;参加反应的氮气和氧气的质量比是______ 。
(2)该反应的基本反应类型是______ 。
(3)从微观视角分析该反应的实质是______ 。化学反应前后各物质的质量总和相等的原因是______ 。
 ”和“
”和“ ”分别表示氮原子和氧原子,下图是氮气与氧气在放电条件下发生反应的微观模拟图。请回答下列问题:
”分别表示氮原子和氧原子,下图是氮气与氧气在放电条件下发生反应的微观模拟图。请回答下列问题:
(1)该反应的方程式为
(2)该反应的基本反应类型是
(3)从微观视角分析该反应的实质是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】小明同学欲通过化学实验证明“质量守恒定律”,确定以“稀盐酸与碳酸钙反应”为研究对象,设计的实验装置如图所示.
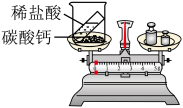
(1)根据实验目的,小明应该测量的数据是______________ (填“只有反应前”“只有反应后”“反应前、后”之一)整个反应装置(包括锥形瓶、气球和药品)的质量.
(2)实验步骤如下:
①按如图方式放好仪器,使天平平衡,记录称量数据.
②将碳酸钙粉末全部倒入锥形瓶中,观察到锥形瓶中液体里出现的现象之一是_______________ .
③当反应结束时,同学们发现天平的指针偏向右边,同学们又重新称量记录了数据.
他们感到困惑,其他操作均正常,实验现象与数据为何与预测结果不符?请帮他们分析导致天平不平衡的原因________________________________
同学们呢经过讨论,意识到自己所犯的错误,有_______ 生成或参与的化学反应必须在 ________ 装置内进行,才能正确验证质量守恒定律。于是他们对试验装置进行了重新设计,如图所示实验步骤如下:
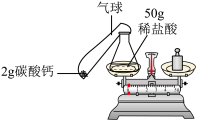
①按如图方式放好仪器,使天平平衡,记录称量数据.
②将碳酸钙粉末全部倒入锥形瓶中,观察现象。
③当反应结束时,气球完全鼓起,他们发现天平的指针仍然偏向右边,你认为出现该实验现象的合理解释最应该是下列各项中的_______ (填序号)
A.该反应前后原子的种类、数目变少
B.该反应生成物的总质量小于反应物的总质量
C.空气的浮力作用干扰了实验结果
D.生成气体的反应不遵守质量守恒定律.
若不考虑该因素的影响,该反应是否遵循质量守恒定律?_______
请从微观方面说明原因_______________________________________________________ 。

(1)根据实验目的,小明应该测量的数据是
(2)实验步骤如下:
①按如图方式放好仪器,使天平平衡,记录称量数据.
②将碳酸钙粉末全部倒入锥形瓶中,观察到锥形瓶中液体里出现的现象之一是
③当反应结束时,同学们发现天平的指针偏向右边,同学们又重新称量记录了数据.
他们感到困惑,其他操作均正常,实验现象与数据为何与预测结果不符?请帮他们分析导致天平不平衡的原因
同学们呢经过讨论,意识到自己所犯的错误,有

①按如图方式放好仪器,使天平平衡,记录称量数据.
②将碳酸钙粉末全部倒入锥形瓶中,观察现象。
③当反应结束时,气球完全鼓起,他们发现天平的指针仍然偏向右边,你认为出现该实验现象的合理解释最应该是下列各项中的
A.该反应前后原子的种类、数目变少
B.该反应生成物的总质量小于反应物的总质量
C.空气的浮力作用干扰了实验结果
D.生成气体的反应不遵守质量守恒定律.
若不考虑该因素的影响,该反应是否遵循质量守恒定律?
请从微观方面说明原因
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】阅读下列科普短文,然后回答问题:
臭氧的化学式是O3,在通常状况下是淡蓝色、有鱼腥臭味的气体。臭氧不稳定,一旦受热极易转化成O2,并放出大量的热。臭氧的氧化能力比氧气(O2)强得多。臭氧层能吸收太阳辐射中的大量紫外线,使地球上的生物免遭紫外线的伤害,它是一切生命的保护层。超音速飞机排出的废气中的一氧化碳(CO)、二氧化碳(CO2)、一氧化氮(NO)等气体,家用电冰箱中使用的制冷剂“氟利昂”等对臭氧层有很大的破坏作用,会使臭氧层形成空洞,从而使更多的紫外线照射到地球表面,导致皮肤癌的发病率大大增加。
(1)臭氧属于______ (填“单质”或“化合物”),O3表示一个____ (填“原子”、“分子”或“离子”)。
(2)写出臭氧的物理性质________ (一点即可)。
(3)氧气转变成臭氧的过程属于_____ (填“物理”或“化学”)变化;在此过程中,下列不会发生变化的是__ (填字母)。
A.原子种类 B.分子种类 C.原子数目
(4)分离氧气和臭氧的混合物,类似于工业制氧气,是利用了它们的____ 不同。
(5)将带火星的木条伸入到盛有 O3 的集气瓶中,可以看到___ 的现象。
(6)依据科普短文,可采取_______ 的方法保护臭氧层。
(7)二氧化硫(SO2)遇到O3微热,即被迅速氧化成三氧化硫(SO3),SO3跟水反应生成硫酸,这是除去废气中SO2的理想方法。写出SO2与O3反应的化学方程式______ ,该反应属于的基本类型是____ 反应。
(8)空气中含有的少量臭氧(O3)可以起到消毒、杀菌作用,但臭氧过量对人体有害。我国的环境空气质量标准对空气中臭氧的最高浓度(单位体积的空气中所含臭氧的质量)限值如下表所示:
反应原理:2KI+H2O+O3=2KOH+O2+I2↓;为测定某地空气中臭氧的含量,将50m3的空气通过足量的KI溶液,生成I2的质量为25.40mg。通过计算确定该地空气中臭氧的浓度级别为______ 。【相对原子质量I:127】
臭氧的化学式是O3,在通常状况下是淡蓝色、有鱼腥臭味的气体。臭氧不稳定,一旦受热极易转化成O2,并放出大量的热。臭氧的氧化能力比氧气(O2)强得多。臭氧层能吸收太阳辐射中的大量紫外线,使地球上的生物免遭紫外线的伤害,它是一切生命的保护层。超音速飞机排出的废气中的一氧化碳(CO)、二氧化碳(CO2)、一氧化氮(NO)等气体,家用电冰箱中使用的制冷剂“氟利昂”等对臭氧层有很大的破坏作用,会使臭氧层形成空洞,从而使更多的紫外线照射到地球表面,导致皮肤癌的发病率大大增加。
(1)臭氧属于
(2)写出臭氧的物理性质
(3)氧气转变成臭氧的过程属于
A.原子种类 B.分子种类 C.原子数目
(4)分离氧气和臭氧的混合物,类似于工业制氧气,是利用了它们的
(5)将带火星的木条伸入到盛有 O3 的集气瓶中,可以看到
(6)依据科普短文,可采取
(7)二氧化硫(SO2)遇到O3微热,即被迅速氧化成三氧化硫(SO3),SO3跟水反应生成硫酸,这是除去废气中SO2的理想方法。写出SO2与O3反应的化学方程式
(8)空气中含有的少量臭氧(O3)可以起到消毒、杀菌作用,但臭氧过量对人体有害。我国的环境空气质量标准对空气中臭氧的最高浓度(单位体积的空气中所含臭氧的质量)限值如下表所示:
| 浓度限值(mg/m3) | ||
| 一级标准0.12 | 二级标准0.16 | 三级标准0.20 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】镁铝合金具有密度小,耐腐蚀、耐磨和导电性能好等优点。
一定质量的某种镁铝合金在12.0g氧气中充分燃烧,生成6.0g氧化镁和20.4g氧化铝。
(1)镁在氧气中燃烧的化学方程式为______ 。
(2)该合金中镁铝原子的个数比为______ 。
一定质量的某种镁铝合金在12.0g氧气中充分燃烧,生成6.0g氧化镁和20.4g氧化铝。
(1)镁在氧气中燃烧的化学方程式为
(2)该合金中镁铝原子的个数比为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室用氯酸钾和二氧化锰组成的混合物装入试管中,加热制取氧气,剩余固体的质量(g)随加热时间(t)的变化关系如图一曲线所示,请回答下列问题:_________ 。
(2)产生氧气的质量是:_________ g。
(3)根据已知条件求解生成氯化钾(x)的比例式为:_________ 。
(4)二氧化锰的质量是:_________ g。
(5)图二所示为某变量y随反应时间的变化趋势,则纵坐标y可以表示的是_________。
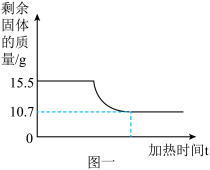
(2)产生氧气的质量是:
(3)根据已知条件求解生成氯化钾(x)的比例式为:
(4)二氧化锰的质量是:
(5)图二所示为某变量y随反应时间的变化趋势,则纵坐标y可以表示的是_________。
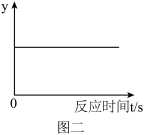
| A.固体中MnO2的质量 | B.固体中钾元素的质量分数 |
| C.固体中氧元素的质量 | D.固体中氯元素的质量 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】空气是宝贵的自然资源,如图是以空气等为原料合成尿素[CO(NH2)2]的流程。请按要求回答相关问题:
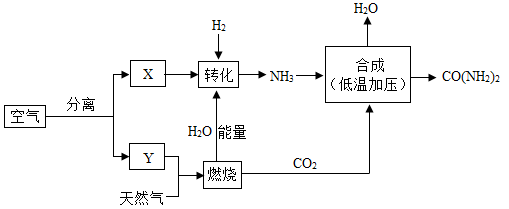
(1)空气属于混合物,X是空气中含量为78%的气体,该气体是_____ (填名称)。空气中用来代替氢气填充飞艇、气球的气体是 _____ (填化学式)。
(2)图中分离空气的过程属中_____ (填“氮气”或“氧气”) 先被蒸发出来。已知常压下氮气沸点﹣196℃,氧气沸点﹣183℃,从微观角度解释空气液化过程中 _____ 。
(3)天然气主要成分是CH4,写出CH4在空气中燃烧符号表达式_____ 。
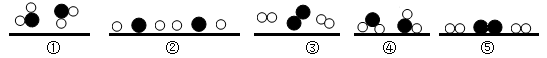
(4)同学们查阅资料后知道了一种使水分解制氢气的方法,水在通过并接触催化剂表面时,分解的微观示意图如图:(“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示催化剂),则水分解的微观过程的正确顺序是
”表示催化剂),则水分解的微观过程的正确顺序是 _____ (填序号)。变化过程的微观实质是 _____ 。

(1)空气属于混合物,X是空气中含量为78%的气体,该气体是
(2)图中分离空气的过程属中
(3)天然气主要成分是CH4,写出CH4在空气中燃烧符号表达式
(4)同学们查阅资料后知道了一种使水分解制氢气的方法,水在通过并接触催化剂表面时,分解的微观示意图如图:(“
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示催化剂),则水分解的微观过程的正确顺序是
”表示催化剂),则水分解的微观过程的正确顺序是 
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下图中“ ”表示碳原子,“
”表示碳原子,“ ”表示氧原子。
”表示氧原子。

其中表示混合物的是____________ (填图的编号), B图表示____________ (填物质名称),B与C反应的化学方程式是_______________ 。
 ”表示碳原子,“
”表示碳原子,“ ”表示氧原子。
”表示氧原子。
其中表示混合物的是
您最近一年使用:0次




