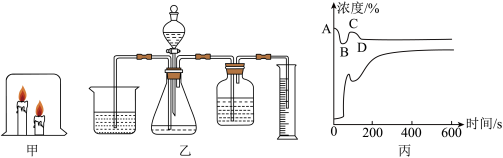
某校化学兴趣小组同学将一只烧杯罩在2支高低不同的燃着的蜡烛上(如图1所示),发现总是高的蜡烛先熄灭。请你同他们一起进行探究。
【提出问题】为什么高的蜡烛先熄灭?
【猜想假设】猜想1:高的蜡烛先灭是因为上部的二氧化碳浓度高;猜想2:高的蜡烛先灭是因为上部的氧气先被消耗。
【实验探究1】为了验证猜想1是否成立,冰冰同学进行了如下实验:
明明对冰冰的结论表示怀疑,他用图乙装置收集一瓶80%二氧化碳和20%氧气的混合气体,然后将燃着的蜡烛伸入收集的混合气体瓶中,发现_________ ,从而证明冰冰的结论不正确。
【实验探究2】明明为了验证猜想2,他利用手持技术实验,用O2、CO2传感器在烧杯顶部测量杯内两支蜡烛从点燃到全部熄灭后,杯内O2和CO2的浓度变化,如图丙所示,图中______ (填“上方”或“下方”)的曲线表示CO2浓度的变化。反应后剩余氧气浓度为15.65%,二氧化碳浓度为1.898%,氧气浓度明显下降,二氧化碳浓度却增大不多。
【实验结论】___________ 。
【反思评价】根据图2中上面一条曲线(装置内氧气浓度)变化分析,在________ (填“A”“B”“C”或“D”)点时蜡烛全部熄灭:请解释曲线AB段、BC段、CD段变化的原因。
AB段:_____________ ;BC段:___________ ;CD段:_________

【提出问题】为什么高的蜡烛先熄灭?
【猜想假设】猜想1:高的蜡烛先灭是因为上部的二氧化碳浓度高;猜想2:高的蜡烛先灭是因为上部的氧气先被消耗。
【实验探究1】为了验证猜想1是否成立,冰冰同学进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 将浸有澄清石灰水的滤纸条分别放在烧杯的顶部和底部,在滤纸条上滴加酚酞,变色后,用烧杯罩住点燃的高低蜡烛,观察高低滤纸条褪色顺序(实验装置如图甲所示) | 猜想1成立,该实验涉及的反应的化学方程式为 |
明明对冰冰的结论表示怀疑,他用图乙装置收集一瓶80%二氧化碳和20%氧气的混合气体,然后将燃着的蜡烛伸入收集的混合气体瓶中,发现
【实验探究2】明明为了验证猜想2,他利用手持技术实验,用O2、CO2传感器在烧杯顶部测量杯内两支蜡烛从点燃到全部熄灭后,杯内O2和CO2的浓度变化,如图丙所示,图中
【实验结论】
【反思评价】根据图2中上面一条曲线(装置内氧气浓度)变化分析,在
AB段:
更新时间:2020-06-04 15:25:02
|
相似题推荐
科学探究题
|
较难
(0.4)
名校
【推荐1】某兴趣小组在学习了CO2的有关知识后,开展了如下探究。
【活动一】探究CO2的性质
小组同学设计了图1所示装置探究CO2的性质,a、d为用紫色石蕊溶液润湿的棉球,b、c为用紫色石蕊溶液染成紫色的干燥棉球,缓慢通入干燥的CO2一段时间。

(1)观察到_______ 的现象,说明CO2能与水反应。
(2)观察到d比a先变红的现象,说明_______ 。
(3)取出已变红的棉球,然后用酒精灯微热,能观察到棉球又变成紫色,原因是_______ (用符号表达式说明)。
【活动二】探究CO2的收集方法
【查阅资料】氢氧化钠溶液能与CO2反应,能有效吸收CO2。
【提出问题】对于CO2的收集方法,兴趣小组甲同学认为只能用向上排空气法收集,乙同学认为还可以采
用排水法收集。
【实验探究】步骤1:小组同学利用如图2所示装置制取CO2,以锥形瓶作收集装置,并采用以下三种方法
收集。
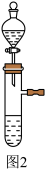
方法一:当反应装置开始产生CO215s后,用排水法收集CO2备用。
方法二:当反应装置开始产生CO215s后,用向上排空气法收集CO2备用。
方法三:当反应装置开始产生CO215s后,用向上排空气法收集CO2,将燃着的木条放在锥形瓶口,待木条熄灭(视CO2收集满)立即盖上玻璃片备用。
步骤Ⅱ:将一定浓度的足量氢氧化钠溶液分别滴入以上锥形瓶中,用压强传感器测得瓶内压强变化情况如
图3所示,用CO2传感器测得瓶内CO2的纯度如表。

【实验结论】
(4)根据数据可知_______ (选填“甲”或“乙”)同学的说法错误。
【反思交流】
(5)收集二氧化碳时,15s以后再收集的目的是_______ 。
(6)根据实验数据分析,用燃着的木条检验二氧化碳收集满_______ (选填“准确”或“不准确”)。
【活动一】探究CO2的性质
小组同学设计了图1所示装置探究CO2的性质,a、d为用紫色石蕊溶液润湿的棉球,b、c为用紫色石蕊溶液染成紫色的干燥棉球,缓慢通入干燥的CO2一段时间。

(1)观察到
(2)观察到d比a先变红的现象,说明
(3)取出已变红的棉球,然后用酒精灯微热,能观察到棉球又变成紫色,原因是
【活动二】探究CO2的收集方法
【查阅资料】氢氧化钠溶液能与CO2反应,能有效吸收CO2。
【提出问题】对于CO2的收集方法,兴趣小组甲同学认为只能用向上排空气法收集,乙同学认为还可以采
用排水法收集。
【实验探究】步骤1:小组同学利用如图2所示装置制取CO2,以锥形瓶作收集装置,并采用以下三种方法
收集。

方法一:当反应装置开始产生CO215s后,用排水法收集CO2备用。
方法二:当反应装置开始产生CO215s后,用向上排空气法收集CO2备用。
方法三:当反应装置开始产生CO215s后,用向上排空气法收集CO2,将燃着的木条放在锥形瓶口,待木条熄灭(视CO2收集满)立即盖上玻璃片备用。
步骤Ⅱ:将一定浓度的足量氢氧化钠溶液分别滴入以上锥形瓶中,用压强传感器测得瓶内压强变化情况如
图3所示,用CO2传感器测得瓶内CO2的纯度如表。

| 方法 | 一 | 二 | 三 |
| 纯度% | 91.1 | 69.5 | 61.9 |
(4)根据数据可知
【反思交流】
(5)收集二氧化碳时,15s以后再收集的目的是
(6)根据实验数据分析,用燃着的木条检验二氧化碳收集满
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】如图是超市中某种维生素C冲剂包装上的说明书,当向该冲剂加入水时,发现粉末逐渐溶解消失,产生大量的气泡。据此探究:

[提出问题]为什么冲剂加水产生气泡?你认为加水后产生气泡主要是①____________ 反应造成的。怎样检验冲剂中含有氯化钠?
[进行假设]维生素C、B1和其它一些有机物不干扰检验氯化钠的。
[设计实验]为了检验粉末中存在NaCl,只要求检验Cl-即可,请完成下列实验方案:
[交流讨论]维生素C冲剂说明书上贮藏条件是低温、避光,反之,包装袋会鼓起,理由④________________________________ 。
[知识拓展]市场上的冲剂花样繁多,而在燕麦冲剂中含有痕量(极少量)的Fe粉,冲剂中加入铁粉的目的是⑤__________________________ ,该冲剂食用过多会引发涨肚,原因是⑥ _____________________________________________ 。

[提出问题]为什么冲剂加水产生气泡?你认为加水后产生气泡主要是①
[进行假设]维生素C、B1和其它一些有机物不干扰检验氯化钠的。
[设计实验]为了检验粉末中存在NaCl,只要求检验Cl-即可,请完成下列实验方案:
| 实验步骤 | 实验现象 | 结论 |
| 取少量冲剂放入试管中加水溶解后,然后 ② | 在此过程中,看到的现象是 ③ | 冲剂中存在Cl- |
[交流讨论]维生素C冲剂说明书上贮藏条件是低温、避光,反之,包装袋会鼓起,理由④
[知识拓展]市场上的冲剂花样繁多,而在燕麦冲剂中含有痕量(极少量)的Fe粉,冲剂中加入铁粉的目的是⑤
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐3】学习了CO2的性质后,同学们对“CO2的溶解性”产生了兴趣,在老师的指导下开展了实验探究活动。
【提出问题】在实验室条件下,1体积的水究竟能溶解多少体积的CO2
【进行实验】
(1)如图所示,向一个集满CO2气体的软塑料瓶中加入约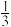 体积的水,立即旋紧瓶盖,振荡,观察到
体积的水,立即旋紧瓶盖,振荡,观察到___________ ,将瓶倒转,放入水中,取下瓶盖,观察到瓶内液面缓慢上升到塑料瓶的约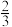 处。
处。
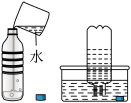
(2)得出结论:1体积的水能溶解___________ 。
【改进实验】
如图所示,取2支医用注射器分别抽取CO2和水,用胶管连接,交替推动2支注射器的活塞,反复多次至数据不再变化。
记录数据如下:
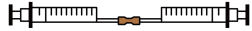
(3)反复多次交替推动注射器活塞的目的是___________ 。
(4)由表中数据可知,在实验室条件下,1体积水最多能溶解___________ 体积的CO2。
【反思质疑】
(5)实验(1)中测得结果比改进实验中结果偏大,请你推测可能的原因是___________ 。
【数字化实验】
如图所示,为了多渠道确认CO2能溶于水,小组同学用数字化实验测量了容器内压强的变化。
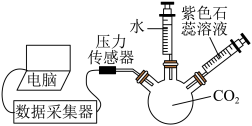
(6)连接好仪器,___________ (填实验操作名称)。
在三颈烧瓶中收集满CO2气体后,设置好数据采集参数。
点击数据采集按钮,将水注入,观察压强曲线变化(如图所示)。

(7)曲线不再变化后,停止收集数据,将紫色石蕊溶液注入烧瓶中,观察到___________ ,原因是___________ 。
(8)加入水后气压明显上升的原因是___________ 。
(9)停止收集数据时,瓶内气压大于初始气压的原因可能是___________ 。
【提出问题】在实验室条件下,1体积的水究竟能溶解多少体积的CO2
【进行实验】
(1)如图所示,向一个集满CO2气体的软塑料瓶中加入约
 体积的水,立即旋紧瓶盖,振荡,观察到
体积的水,立即旋紧瓶盖,振荡,观察到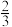 处。
处。
(2)得出结论:1体积的水能溶解
【改进实验】
如图所示,取2支医用注射器分别抽取CO2和水,用胶管连接,交替推动2支注射器的活塞,反复多次至数据不再变化。
记录数据如下:

| 抽取CO2的体积 | 抽取水的体积 | 混合后总体积 |
| 10 mL | 10 mL | 13 mL |
(3)反复多次交替推动注射器活塞的目的是
(4)由表中数据可知,在实验室条件下,1体积水最多能溶解
【反思质疑】
(5)实验(1)中测得结果比改进实验中结果偏大,请你推测可能的原因是
【数字化实验】
如图所示,为了多渠道确认CO2能溶于水,小组同学用数字化实验测量了容器内压强的变化。

(6)连接好仪器,
在三颈烧瓶中收集满CO2气体后,设置好数据采集参数。
点击数据采集按钮,将水注入,观察压强曲线变化(如图所示)。

(7)曲线不再变化后,停止收集数据,将紫色石蕊溶液注入烧瓶中,观察到
(8)加入水后气压明显上升的原因是
(9)停止收集数据时,瓶内气压大于初始气压的原因可能是
您最近一年使用:0次
【推荐1】新年联欢晚会上,老师给同学们表演了一个魔术:大烧杯中盛有一只燃着的蜡烛和一团包有过氧化钠(Na2O2)的棉花,将一瓶二氧化碳倒入烧杯中,蜡烛慢慢的熄灭,然后棉花突然剧烈的燃烧起来。这出乎意料的现象引起了同学们的极大兴趣,请你参与同学们的讨论和探究。
蜡烛熄灭的原因是__________ 。
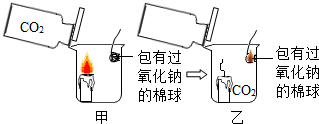
【提出问题】棉花为什么会燃烧?
【提出猜想】
(1)可能是蜡烛燃烧引燃了棉花。
(2)可能是二氧化碳与过氧化钠反应生成了氧气。
(3)_________ 。
【实验验证】
【实验结论】
(1)CO2与Na2O2反应生成了氧气与一种化合物,化学方程式为________ 。
(2)通常CO2可作灭火剂,但有些物质(如Na2O2)着火,不能用CO2熄灭。
蜡烛熄灭的原因是

【提出问题】棉花为什么会燃烧?
【提出猜想】
(1)可能是蜡烛燃烧引燃了棉花。
(2)可能是二氧化碳与过氧化钠反应生成了氧气。
(3)
【实验验证】
| 序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
| ① | 按下图所示装置进行实验 | 蜡烛慢慢熄灭 | 猜想(1) |
| ② | 向盛满二氧化碳的集气瓶中加入适量的过氧化钠粉末,充分振荡并 | 二氧化碳与过氧化钠反应生成了氧气,猜想(2)成立 | |
| ③ | 猜想(3)成立 |
(1)CO2与Na2O2反应生成了氧气与一种化合物,化学方程式为
(2)通常CO2可作灭火剂,但有些物质(如Na2O2)着火,不能用CO2熄灭。
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某化学研究小组对蜡烛(主要由碳、氢元素组成)燃烧进行了如下探究:
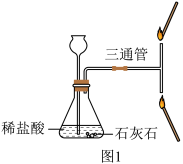
(1)设计图1所示实验,请推测靠近三通管________ (填“上口”或“下口”)的火柴火焰先熄灭,理由是 __________ 。
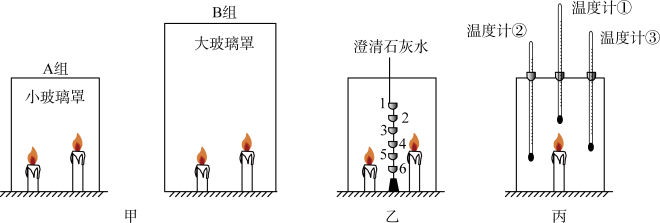
(2)小明用大小不同的玻璃罩罩在两组点燃的蜡烛上(如图甲),观察发现A组实验高处烛焰先熄灭,B组实验低处烛焰先熄灭。
[提出问题]导致A组实验高处烛焰先熄灭,B组实验低处烛焰先熄灭的原因是什么?
[查阅资料]物质燃烧释放大量的热,生成物受热膨胀,密度降低向上运动。
[猜想与假设]
假设1:烛焰熄灭可能与二氧化碳浓度有关;
假设2:烛焰熄灭可能与_________ 浓度太低有关;
假设3:烛焰熄灭可能与温度有关;
[设计实验]
实验一:将6个盛有等量澄清石灰水的敞口容器固定在铁丝上,点燃蜡烛,立即用小玻璃罩罩上(如图乙)。分别记下各容器内石灰水变浑浊所需的时间。多次重复实验获得数据如表。
①说明此时高蜡烛附近的二氧化碳浓度比低蜡烛附近的浓度________ (填“高”或“低”) ,导致A组实验高处烛焰先熄灭。
②请写出澄清石灰水变浑浊的化学方程式__________ 。
实验二:将3支温度计分别挂在大玻璃罩内不同位置(如图丙),点燃蜡烛,一段时间后发现温度计①示数明显增大,温度计②③示数增大不明显。
①实验二研究的问题是_______ 。
②结合本实验的研究结果,对B组实验现象做出简要解释:______ 。
(1)设计图1所示实验,请推测靠近三通管

(2)小明用大小不同的玻璃罩罩在两组点燃的蜡烛上(如图甲),观察发现A组实验高处烛焰先熄灭,B组实验低处烛焰先熄灭。

[提出问题]导致A组实验高处烛焰先熄灭,B组实验低处烛焰先熄灭的原因是什么?
[查阅资料]物质燃烧释放大量的热,生成物受热膨胀,密度降低向上运动。
[猜想与假设]
假设1:烛焰熄灭可能与二氧化碳浓度有关;
假设2:烛焰熄灭可能与
假设3:烛焰熄灭可能与温度有关;
[设计实验]
实验一:将6个盛有等量澄清石灰水的敞口容器固定在铁丝上,点燃蜡烛,立即用小玻璃罩罩上(如图乙)。分别记下各容器内石灰水变浑浊所需的时间。多次重复实验获得数据如表。
| 容器编号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 平均时间/秒 | 3.2 | 3.8 | 5.0 | 7.1 | 11.1 | 19.0 |
①说明此时高蜡烛附近的二氧化碳浓度比低蜡烛附近的浓度
②请写出澄清石灰水变浑浊的化学方程式
实验二:将3支温度计分别挂在大玻璃罩内不同位置(如图丙),点燃蜡烛,一段时间后发现温度计①示数明显增大,温度计②③示数增大不明显。
①实验二研究的问题是
②结合本实验的研究结果,对B组实验现象做出简要解释:
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】实验探究一:探究空气中CO2的含量已经达到影响人体健康的程度。
【查阅资料】空气中CO2的体积分数为1%时,人会有心跳加快、困乏、注意力不集中、轻度恶心等症状;体积分数为5%时,会有呼吸不畅、头晕、耳鸣、血压升高等症状:体积分数为10%时,会有严重缺氧、丧失意识、昏迷等症状。
【提出问题】在没有专业测量仪器的情况下,如何检验空气中CO2的含量已经达到影响人体健康的程度?
【设计实验】依据CO2的性质,设计检验方法。
(1)根据方法2的预期现象推断,所需试剂X是______________ 。
【配制样品】常温常压下,配制CO2体积分数不同的气体样品。
(2)收集5 mLCO2与空气混合,得到500 mL含CO2________ %的气体样品;收集25mLCO2与空气混合,得到500 mL含CO2_________ %的气体样品。
【进行实验】常温常压下,集气瓶和试管中盛有空气或CO2气体样品,分别进行以下实验。
【解释与应用】
(3)从灭火原理分析,方法1中均没有出现“燃着木条熄灭”的原因是______________ 。
(4)1班有部分同学在教室内出现“困乏、注意力不集中”等症状时,小陈同学想用上述实验方法检测教室内CO2气体的含量,他应该选用的方法是______________ (填方法序号)。
(5)2班小昱同学收集了教室中的气体,尝试用方法2进行实验,发现溶液由紫色变为红色。由此现象推测此时教室中CO2的含量可能为____________ 。(填字母序号)。
A.1%以下 B.1% C.1%-5% D.5%以上
实验探究二:探究CO2在不同条件下的溶解情况
为减少CO2的不利影响,利用CO2在水等溶剂中的溶解性来吸收CO2是实现“碳中和”的途径之一。小霏同学做如下2个实验。
【实验1】探究CO2在水和食盐水(模拟海水)中的溶解情况
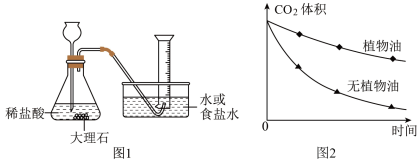
相同条件下,该小组分别用排水法、排食盐水法收集CO2 (如图1),待收集100 mL CO2后,移出导管,每隔一段时间观察并记录量筒内CO2体积。重复实验,所测数据平均值如下表:
(6)图1发生装置中反应的化学方程式为_____________ 。
(7)由上表数据分析:①能用排水法收集CO2的理由是______________ 。
②相同条件下,等体积水和食盐水吸收CO2更多的是___________ (填“水”或“食盐水”)。
(8)海洋封存CO2可能带来的危害是__________ (写出1点即可)。
【实验2】探究植物油隔离对CO2在水中溶解情况的影响
(9)小方设计并完成以下对照实验:用两个量筒分别收集100 mL CO2倒置于水槽中,向其中一个量筒内注入少量植物油,使CO2与水被植物油隔开(CO2与植物油不反应)测得量筒内CO2体积随时间的变化曲线如图2。分析图2可得出的结论是_____________ 。
【查阅资料】空气中CO2的体积分数为1%时,人会有心跳加快、困乏、注意力不集中、轻度恶心等症状;体积分数为5%时,会有呼吸不畅、头晕、耳鸣、血压升高等症状:体积分数为10%时,会有严重缺氧、丧失意识、昏迷等症状。
【提出问题】在没有专业测量仪器的情况下,如何检验空气中CO2的含量已经达到影响人体健康的程度?
【设计实验】依据CO2的性质,设计检验方法。
| 性质CO2 | 检验方法 | 预期现象 | |
| 方法1 | 不能燃烧不支持燃烧 | 用燃着木条检验 | 燃着木条熄灭 |
| 方法2 | 与水反应 | 用 X 溶液检验 | 溶液由紫色变成红色 |
| 方法3 | 与石灰水反应 | 用澄清石灰水检验 | 澄清石灰水变浑浊 |
【配制样品】常温常压下,配制CO2体积分数不同的气体样品。
(2)收集5 mLCO2与空气混合,得到500 mL含CO2
【进行实验】常温常压下,集气瓶和试管中盛有空气或CO2气体样品,分别进行以下实验。
| 方法序号 | 方法1 | 方法2 | 方法3 |
| 实验过程 |  | 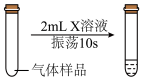 |  |
| 空气 | 正常燃烧 | 溶液无明显变化 | 澄清石灰水不变浑浊 |
| 含CO21%的气体样品 | 正常燃烧 | 溶液无明显变化 | 澄清石灰水变浑浊 |
| 含CO25%的气体样品 | 正常燃烧 | 溶液由紫色变成红色 | 澄清石灰水变浑浊 |
(3)从灭火原理分析,方法1中均没有出现“燃着木条熄灭”的原因是
(4)1班有部分同学在教室内出现“困乏、注意力不集中”等症状时,小陈同学想用上述实验方法检测教室内CO2气体的含量,他应该选用的方法是
(5)2班小昱同学收集了教室中的气体,尝试用方法2进行实验,发现溶液由紫色变为红色。由此现象推测此时教室中CO2的含量可能为
A.1%以下 B.1% C.1%-5% D.5%以上
实验探究二:探究CO2在不同条件下的溶解情况
为减少CO2的不利影响,利用CO2在水等溶剂中的溶解性来吸收CO2是实现“碳中和”的途径之一。小霏同学做如下2个实验。
【实验1】探究CO2在水和食盐水(模拟海水)中的溶解情况

相同条件下,该小组分别用排水法、排食盐水法收集CO2 (如图1),待收集100 mL CO2后,移出导管,每隔一段时间观察并记录量筒内CO2体积。重复实验,所测数据平均值如下表:
| 时间/h | 0 | 0.5 | 6 | 12 | 24 | 48 |
| 排水法时CO2体积/mL | 100 | 98.5 | 85.5 | 77 | 66 | 59 |
| 排食盐水法时CO2体积/mL | I00 | 99 | 93 | 90.5 | 89 | 88 |
(7)由上表数据分析:①能用排水法收集CO2的理由是
②相同条件下,等体积水和食盐水吸收CO2更多的是
(8)海洋封存CO2可能带来的危害是
【实验2】探究植物油隔离对CO2在水中溶解情况的影响
(9)小方设计并完成以下对照实验:用两个量筒分别收集100 mL CO2倒置于水槽中,向其中一个量筒内注入少量植物油,使CO2与水被植物油隔开(CO2与植物油不反应)测得量筒内CO2体积随时间的变化曲线如图2。分析图2可得出的结论是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐1】某化学兴趣小组在做“铁在氧气中燃烧”实验时,进行了一系列探究活动,请你一同参与。
【探究一】

(1)小组的实验过程如图甲所示。铁丝表面要先用砂纸打磨光亮再绕成“螺旋状”,铁丝绕成“螺旋状”的目的是_______ 。该反应的文字表达式是_______ 。
【探究二】影响铁丝燃烧的因素。
【设计并实验】
经过讨论后,小组同学取两种不同直径的铁丝,以氧气的体积分数为变量进行实验如表:
【分析讨论】
(2)选择实验_______ (填实验编号)的数据进行探究,可对比氧气浓度对0.5mm铁丝燃烧程度的影响。
(3)为了更准确地了解直径为0.9mm的铁丝燃烧所需氧气的最低浓度,你认为同学们继续进行实验应选取的氧气体积分数的范围是_______ 。
【实验结论】
(4)根据表格数据,可以得出铁丝的燃烧与_______ 、_______ 等因素有关。
【实验拓展】
(5)小组同学用图乙装置收集一瓶(150mL)含氧气的体积分数约为60%的气体,方法是:在150mL集气瓶里装满水,塞紧胶塞并关闭活塞b,打开活塞a通入氧气,把瓶里的水排入量筒,当量筒内的水达到设定的体积后立即关闭活塞a,然后打开活塞b通入空气,把瓶里的水全部排入量筒。则停止通入氧气时量筒内水的体积约为_______ (提示:空气中氧气的体积分数约为1/5)。
A 25mL
B 40mL
C 60mL
D 75mL
(6)小红对铁丝燃烧实验进行了简化设计,如图丙所示。简述改实验设计的优点____ 。
【探究一】

(1)小组的实验过程如图甲所示。铁丝表面要先用砂纸打磨光亮再绕成“螺旋状”,铁丝绕成“螺旋状”的目的是
【探究二】影响铁丝燃烧的因素。
【设计并实验】
经过讨论后,小组同学取两种不同直径的铁丝,以氧气的体积分数为变量进行实验如表:
| 试验编号 | 铁丝直径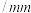 | 氧气的体积分数 浓度 浓度 | 实验现象 |
| A | 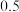 | 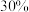 | 铁丝发红,无法燃烧 |
| B | 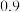 | 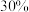 | 无法燃烧 |
| C | 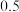 |  | 燃烧不剧烈,少量火星 |
| D | 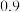 |  | 铁丝发红,无法燃烧 |
| E | 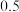 |  | |
| F | 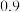 |  | 燃烧不剧烈,少量火星 |
(2)选择实验
(3)为了更准确地了解直径为0.9mm的铁丝燃烧所需氧气的最低浓度,你认为同学们继续进行实验应选取的氧气体积分数的范围是
【实验结论】
(4)根据表格数据,可以得出铁丝的燃烧与
【实验拓展】
(5)小组同学用图乙装置收集一瓶(150mL)含氧气的体积分数约为60%的气体,方法是:在150mL集气瓶里装满水,塞紧胶塞并关闭活塞b,打开活塞a通入氧气,把瓶里的水排入量筒,当量筒内的水达到设定的体积后立即关闭活塞a,然后打开活塞b通入空气,把瓶里的水全部排入量筒。则停止通入氧气时量筒内水的体积约为
A 25mL
B 40mL
C 60mL
D 75mL
(6)小红对铁丝燃烧实验进行了简化设计,如图丙所示。简述改实验设计的优点
您最近一年使用:0次
【推荐2】人体代谢产生的过氧化氢,对人体有毒害作用。人体肝脏中的过氧化氢酶能催化过氧化氢分解产生氧气和水。某同学查阅资料发现,FeCl3也能催化过氧化氢分解。为比较过氧化氢酶和FeCl3催化效率的高低,该同学在28℃环境下进行了如下探究:
(1)提出问题:过氧化氢酶和FeCl3催化效率哪个更高?
(2)猜想与假设:___________ ;
(3)实验材料:适宜浓度的FeCl3溶液,适宜浓度的新鲜猪肝研磨液(含有过氧化氢酶),___________ ,实验器材如试管等;
(4)实验步骤:
①取2支洁净的试管,编号为1、2,并各注入3mL适宜浓度的过氧化氢溶液,
②向1号试管内滴入2滴适宜浓度的FeCl3溶液,向2号试管内___________ ,
③观察并记录两支试管产生气泡的情况;
(5)预测实验结果,请写出一种可能的实验结果___________ ;
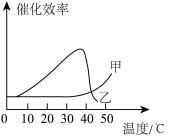
(6)在以上探究基础上,该同学又完成了“探究温度对猪肝研磨液和FeCl3催化效率的影响”实验,实验结果如图所示,图中代表猪肝研磨液催化效率的曲线是___________ ,判断的理由是___________ 。
(1)提出问题:过氧化氢酶和FeCl3催化效率哪个更高?
(2)猜想与假设:
(3)实验材料:适宜浓度的FeCl3溶液,适宜浓度的新鲜猪肝研磨液(含有过氧化氢酶),
(4)实验步骤:
①取2支洁净的试管,编号为1、2,并各注入3mL适宜浓度的过氧化氢溶液,
②向1号试管内滴入2滴适宜浓度的FeCl3溶液,向2号试管内
③观察并记录两支试管产生气泡的情况;
(5)预测实验结果,请写出一种可能的实验结果
(6)在以上探究基础上,该同学又完成了“探究温度对猪肝研磨液和FeCl3催化效率的影响”实验,实验结果如图所示,图中代表猪肝研磨液催化效率的曲线是

您最近一年使用:0次
【推荐3】人教版化学教材九年级上册“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
【实验结论】(1)A试管中产生的气体是_____ 。
(2)实验II、Ⅲ证明:氧化铁的_____ 和______ 在反应前后均没有发生变化,可以作为过氧化氢分解的催化剂。(3)写出氧化铁催化过氧化氢分解的文字表达式_______ 。
【实验评价】(4)实验设计IV的目的是_____ 。
(5)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是____ 。
【实验拓展】(6)查阅资料得知,氧化铜、红砖头、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是_____
A MnO2只能作过氧化氢溶液分解的催化剂B同一个化学反应可以有多种催化剂
C催化剂只能加快化学反应的速率D用作催化剂的物质不可能是其他反应的反应物或生成物
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| I.分别取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
| Ⅲ.将实验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 |  |
| IV.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |  |
【实验结论】(1)A试管中产生的气体是
(2)实验II、Ⅲ证明:氧化铁的
【实验评价】(4)实验设计IV的目的是
(5)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是
【实验拓展】(6)查阅资料得知,氧化铜、红砖头、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是
A MnO2只能作过氧化氢溶液分解的催化剂B同一个化学反应可以有多种催化剂
C催化剂只能加快化学反应的速率D用作催化剂的物质不可能是其他反应的反应物或生成物
您最近一年使用:0次



