某研究性学习小组选用98%的浓硫酸(密度1.84g/cm3)和黄铜样品进行下列实验。
实验一:配制100g 9.8%的稀硫酸
主要步骤:
(1)计算:需要浓硫酸_______ mL(精确到0.1)。
(2)量取:a. 量取所需的浓硫酸;
b. 用_____ mL(选填“50”、“100”或“200”)量筒量取所需的水。如果量水时俯视读数,会导致所配稀硫酸的溶质质量分数_____ (选填“偏大”、“偏小”或“不变”)。
(3)稀释。
实验二:完成相关测定
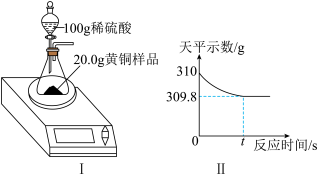
小组同学取20g黄铜样品放入图Ⅰ锥形瓶中,将稀硫酸全部加入,恰好完全反应后天平示数的变化如图Ⅱ所示。请计算:
(1)生成氢气______ g。
(2)黄铜样品中铜的质量_____ (请写出计算过程,下同)。
(3)反应后所得溶液中溶质的质量分数(精确到0.1%)_____ 。
实验一:配制100g 9.8%的稀硫酸
主要步骤:
(1)计算:需要浓硫酸
(2)量取:a. 量取所需的浓硫酸;
b. 用
(3)稀释。
实验二:完成相关测定

小组同学取20g黄铜样品放入图Ⅰ锥形瓶中,将稀硫酸全部加入,恰好完全反应后天平示数的变化如图Ⅱ所示。请计算:
(1)生成氢气
(2)黄铜样品中铜的质量
(3)反应后所得溶液中溶质的质量分数(精确到0.1%)
更新时间:2020-07-19 23:51:43
|
相似题推荐
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】某兴趣小组展开了对硝酸钾固体及其溶液的实验探究,现配制50克5%的硝酸钾溶液。
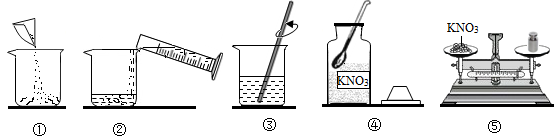
(1)以上正确的操作顺序是________________ ;
A.④⑤①②③ B.①②③④⑤ C.⑤②①④③ D.③④①②⑤
(2)本实验需称取硝酸钾固体_________ g;若称取固体时,托盘天平的指针略微向右偏移时,需进行的操作是__________________________________________ ;
(3)现在有10g20%的硝酸钾溶液(密度1.13g/cm3),若稀释成该浓度的溶液,则需要加入_____ g的水,稀释过程中除烧杯和玻璃棒外还需要的仪器是__________________ ;
(4)若所配溶液中硝酸钾的质量分数偏小,可能原因有______________ 。
A.用托盘天平称取时,左边放砝码右边放硝酸钾
B.转移已配好的溶液时,有少量液体溅出
C.用量筒取水时仰视读数
D.烧杯用蒸馏水润洗后再配制溶液

(1)以上正确的操作顺序是
A.④⑤①②③ B.①②③④⑤ C.⑤②①④③ D.③④①②⑤
(2)本实验需称取硝酸钾固体
(3)现在有10g20%的硝酸钾溶液(密度1.13g/cm3),若稀释成该浓度的溶液,则需要加入
(4)若所配溶液中硝酸钾的质量分数偏小,可能原因有
A.用托盘天平称取时,左边放砝码右边放硝酸钾
B.转移已配好的溶液时,有少量液体溅出
C.用量筒取水时仰视读数
D.烧杯用蒸馏水润洗后再配制溶液
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】KNO3和KCl的溶解度曲线如图所示。
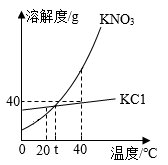
(1)20℃时,KNO3的溶解度_________ (填“大于”、“等于”或“小于”)KCl的溶解度。
(2)将40℃ KNO3的饱和溶液降温至20℃,该溶液的溶质质量分数会______ (填“变大”、“变小”或“不变”)。
(3)40℃时,将70g KCl的饱和溶液稀释成质量分数为10%的溶液,需要加水的质量为___ 。

(1)20℃时,KNO3的溶解度
(2)将40℃ KNO3的饱和溶液降温至20℃,该溶液的溶质质量分数会
(3)40℃时,将70g KCl的饱和溶液稀释成质量分数为10%的溶液,需要加水的质量为
您最近一年使用:0次
【推荐1】铁是当今社会应用最广泛的金属。
(1)如图是铁在元素周期表中的相关信息及铁原子结构示意图,下列说法错误的是
(2)生产生活中的铁制品大多由铁合金制成。合金属于________ (填“合成材料”或“金属材料”);作为铁的一种合金,生铁可用于制作铁锅,利用的是铁具有良好的________ 性。
(3)工业上通过冶炼铁矿石获取铁。某同学利用下图装置在实验室模拟炼铁。________ 。
②从环保角度考虑,请写出一种尾气处理方法________ 。
③为检验B 装置中是否还有 NaOH,该同学取B 中溶液样品,加入足量的Ca(OH)2溶液,充分反应后,向上层清液滴加无色酚酞溶液进行检验。请找出该方案不合理之处并说明理由________ 。
(4)铁制品一旦锈蚀,需及时除锈。工业上常用稀硫酸除铁锈(Fe2O3), 该反应的化学方程式为_______________
(5)废弃铁制品还可以回收利用。某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现溶质质量分数为20%的废硫酸19.6t,与足量的废铁屑反应,可生产硫酸亚铁的质量是多少?
(1)如图是铁在元素周期表中的相关信息及铁原子结构示意图,下列说法错误的是
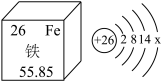
| A.铁原子的核电荷数为26 | B.铁的相对原子质量为55.85g |
| C.x=2 | D.铁位于元素周期表第四周期 |
(2)生产生活中的铁制品大多由铁合金制成。合金属于
(3)工业上通过冶炼铁矿石获取铁。某同学利用下图装置在实验室模拟炼铁。
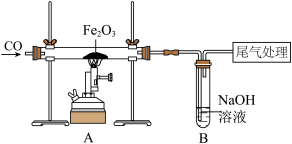
②从环保角度考虑,请写出一种尾气处理方法
③为检验B 装置中是否还有 NaOH,该同学取B 中溶液样品,加入足量的Ca(OH)2溶液,充分反应后,向上层清液滴加无色酚酞溶液进行检验。请找出该方案不合理之处并说明理由
(4)铁制品一旦锈蚀,需及时除锈。工业上常用稀硫酸除铁锈(Fe2O3), 该反应的化学方程式为
(5)废弃铁制品还可以回收利用。某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现溶质质量分数为20%的废硫酸19.6t,与足量的废铁屑反应,可生产硫酸亚铁的质量是多少?
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】向盛有一定质量氧化钙和碳酸钙混合物的烧杯中加入142g稀盐酸,恰好完全反应,一定温度下,得到153.2g不饱和溶液。则该不饱和溶液的溶质质量分数是(结果保留一位小数)___________ 。
您最近一年使用:0次