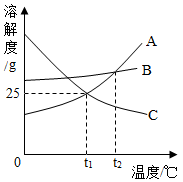
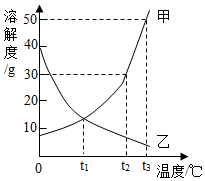
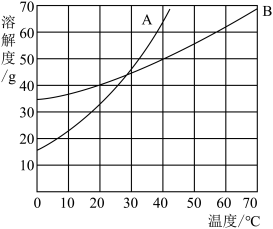
分析处理图表中的信息是学习化学的一种重要的方法。
氯化钠和硝酸钾两种物质的溶解度随温度(0℃-100℃)的变化见下表。
请分析表格中的数据,回答下列问题:
(1)从表格中可以得到一条信息是_____ ;
(2)若两种物质的溶解度相等,此时所对应的温度范围在________ 之间;
(3)某同学欲从含有少量硝酸钾的氯化钠中分离出氯化钠,他应采取的方法是_____ ;
(4)在20 ℃时,向50 g水加入25 g硝酸钾中,充分搅拌后得到的是硝酸钾的_____ (填“饱和溶液”或“不饱和溶液”),其质量是______ g;将上述溶液升温到60 ℃,该溶液的质量为_________ g。
氯化钠和硝酸钾两种物质的溶解度随温度(0℃-100℃)的变化见下表。
| 0 ℃ | 20 ℃ | 40 ℃ | 60 ℃ | 80 ℃ | 100 ℃ | |
| NaCl(g) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3(g) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(1)从表格中可以得到一条信息是
(2)若两种物质的溶解度相等,此时所对应的温度范围在
(3)某同学欲从含有少量硝酸钾的氯化钠中分离出氯化钠,他应采取的方法是
(4)在20 ℃时,向50 g水加入25 g硝酸钾中,充分搅拌后得到的是硝酸钾的
更新时间:2020/09/30 13:26:45
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】(淮安市某盐化厂生产的碳酸钠粗产品中含有少量氯化钠,碳酸钠和氯化钠的溶解度与温度的关系如图所示,回答下列问题:
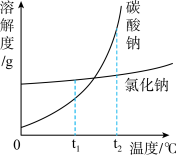
(1)t1℃时碳酸钠与氯化钠中溶解度较大的物质是___________ ,
(2)t1℃时碳酸钠饱和溶液升温至t2℃,所得溶液的溶质质量分数____________ (填“变大”、“变小”或“不变”),
(3)除去碳酸钠中混有少量氯化钠的方法是_______ 。

(1)t1℃时碳酸钠与氯化钠中溶解度较大的物质是
(2)t1℃时碳酸钠饱和溶液升温至t2℃,所得溶液的溶质质量分数
(3)除去碳酸钠中混有少量氯化钠的方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示是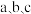 三种固体物质的溶解度曲线。
三种固体物质的溶解度曲线。
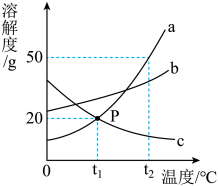
(1)点 表示的含义
表示的含义______ ;
(2)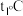 时,将
时,将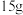 固体
固体 加入
加入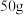 水中,形成溶液质量为
水中,形成溶液质量为______ ;
(3)为除去 中混有的少量
中混有的少量 ,可采用
,可采用______ (填“蒸发结晶”或“降温结晶”)法。
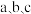 三种固体物质的溶解度曲线。
三种固体物质的溶解度曲线。
(1)点
 表示的含义
表示的含义(2)
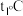 时,将
时,将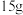 固体
固体 加入
加入 水中,形成溶液质量为
水中,形成溶液质量为(3)为除去
 中混有的少量
中混有的少量 ,可采用
,可采用
您最近一年使用:0次
【推荐1】溶液在生产、生活中起着十分重要的作用。请回答(1)-(2)题。
(1)如图,在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯中加水进搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是_______ 。
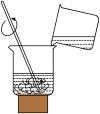
A 氯化钠 B 硝酸铵 C 氢氧化钠 D 蔗糖
(2)用汽油或加了洗涤剂的水都能除去衣服上的油污,两者去油污的原理分别是_______ 。
A 乳化、乳化 B 乳化、溶解 C 溶解、乳化 D 溶解、溶解
如图是甲、乙、丙三种固体物质的溶解度曲线。请回答(3)(4)题。
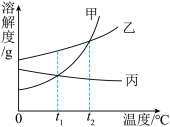
(3)现有t1℃时甲乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是_______ 。
A 甲=乙>丙 B 乙>甲=丙 C 乙>甲>丙 D 甲>乙>丙
(4)为了将近饱和的丙溶液变为饱和溶液,可采用的方法有_______ (有2-3个选项符合题意)。
A 加固体丙 B 加水 C 降低温度 D 蒸发浓缩
(1)如图,在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯中加水进搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是

A 氯化钠 B 硝酸铵 C 氢氧化钠 D 蔗糖
(2)用汽油或加了洗涤剂的水都能除去衣服上的油污,两者去油污的原理分别是
A 乳化、乳化 B 乳化、溶解 C 溶解、乳化 D 溶解、溶解
如图是甲、乙、丙三种固体物质的溶解度曲线。请回答(3)(4)题。

(3)现有t1℃时甲乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是
A 甲=乙>丙 B 乙>甲=丙 C 乙>甲>丙 D 甲>乙>丙
(4)为了将近饱和的丙溶液变为饱和溶液,可采用的方法有
A 加固体丙 B 加水 C 降低温度 D 蒸发浓缩
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】下表是氯化钠和氯化钾在不同温度时的溶解度。
(1)40℃时,氯化钠的溶解度为__________ 。
(2)20℃时,将20g氯化钠固体加入到50g水中,充分溶解,所得氯化钠溶液为__________ (选填“饱和溶液”或“不饱和溶液”)。
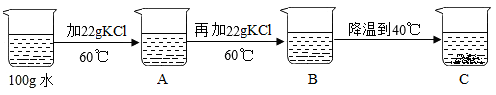
(3)某同学进行实验如下图所示,得到相应的A、B、C三种溶液,C中析出的氯化钾固体质量为__________ g。为使C中固体溶解,至少需加入__________ g水。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | |
(2)20℃时,将20g氯化钠固体加入到50g水中,充分溶解,所得氯化钠溶液为
(3)某同学进行实验如下图所示,得到相应的A、B、C三种溶液,C中析出的氯化钾固体质量为

您最近一年使用:0次
【推荐3】研究物质的溶解度对于生产生活有重要意义。下表是碳酸钠的溶解度随温度的变化情况。
_________ 。
(2)将10℃时225g碳酸钠饱和溶液变为20℃时的碳酸钠饱和溶液进行的操作:先升高温度到20℃;再加入_______ g碳酸钠固体。
(3)如图所示实验;烧杯③中的溶液属于_______ (选填“饱和”或“不饱和”)溶液。烧杯④中出现的现象是______________ 。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 |
| 溶解度/g | 7 | 12.5 | 21.5 | 39.7 | 49 | 46 | 43.6 |
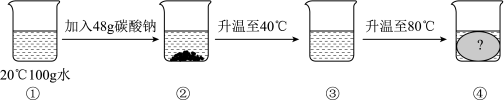
(2)将10℃时225g碳酸钠饱和溶液变为20℃时的碳酸钠饱和溶液进行的操作:先升高温度到20℃;再加入
(3)如图所示实验;烧杯③中的溶液属于
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】M、N、P三种物质的溶解度曲线如图,请回答下列问题:
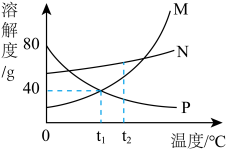
(1)能从图中得到的信息是______ 。(写出一条即可)
(2)若M中混有少量N,最好采用______ 的方法提纯M。
(3)t1℃时把40gM投入80g水中,得到的溶液质量是______ g。

(1)能从图中得到的信息是
(2)若M中混有少量N,最好采用
(3)t1℃时把40gM投入80g水中,得到的溶液质量是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】氯化钠和硝酸钾在不同温度时的溶解度如下表,请回答下列问题。
(1)影响固体物质溶解度大小的因素是___________ (填一种)。
(2)20℃时,将20gNaCl加入50g水中,所得溶液是___________ (填“饱和”或“不饱和”)溶液。
(3)20℃时,将136g饱和的氯化钠溶液稀释成质量分数为20%的氯化钠溶液,需要加水的质量为___________ 。
(4)在一定温度下,将含有55gKNO3、18gNaCl的混合物完全溶解在50g水中。改变温度至t℃时,使KNO3析出,NaCl不析出,则t的取值范围是___________ (KNO3和NaCl的溶解度互不影响)。
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | |
(2)20℃时,将20gNaCl加入50g水中,所得溶液是
(3)20℃时,将136g饱和的氯化钠溶液稀释成质量分数为20%的氯化钠溶液,需要加水的质量为
(4)在一定温度下,将含有55gKNO3、18gNaCl的混合物完全溶解在50g水中。改变温度至t℃时,使KNO3析出,NaCl不析出,则t的取值范围是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】请用“>”,“<”或“=”填空:
(1)V1mL水和V2mL酒精混合后所得溶液的体积_______ (V1+V2)mL;
(2)t1℃时,氢氧化钙的饱和溶液降温至t2℃时,则变成不饱和溶液。其t1℃时饱和溶液中溶质的质量分数_______ t2℃不饱和溶液的溶质质量分数。
(1)V1mL水和V2mL酒精混合后所得溶液的体积
(2)t1℃时,氢氧化钙的饱和溶液降温至t2℃时,则变成不饱和溶液。其t1℃时饱和溶液中溶质的质量分数
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】根据图1图2和图3回答下列问题。
(1)图1的海水中含有大量氯化钠,氯化钠是由(填离子符号)_____ 和_____ 构成;
(2)图2的试管B中的气体的化学式是_____ ,该气体的检验方法是______ ;
(3)分析图1可知,在水蒸发的过程中,下列说法正确的是(填字母序号,下同)_____ ;
A 水分子不断运动 B 水分子之间间隔不变
C 氢、氧原子不发生改变 D 水分子可以保持水的物理性质
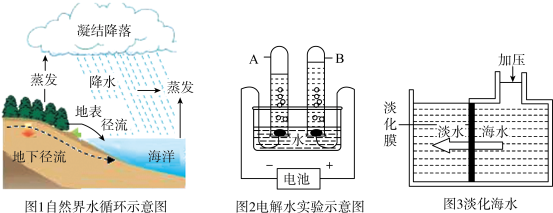
(4)如图3是采用膜分离技术的海水淡化装置,加压后,只有水分子可以通过淡化膜,其他粒子不能通过淡化膜.加压前后,装置右侧海水中,下列各量减小的是_____ .
A 溶质质量分数 B 溶剂质量 C 溶液质量 D 溶质质量.
(1)图1的海水中含有大量氯化钠,氯化钠是由(填离子符号)
(2)图2的试管B中的气体的化学式是
(3)分析图1可知,在水蒸发的过程中,下列说法正确的是(填字母序号,下同)
A 水分子不断运动 B 水分子之间间隔不变
C 氢、氧原子不发生改变 D 水分子可以保持水的物理性质

(4)如图3是采用膜分离技术的海水淡化装置,加压后,只有水分子可以通过淡化膜,其他粒子不能通过淡化膜.加压前后,装置右侧海水中,下列各量减小的是
A 溶质质量分数 B 溶剂质量 C 溶液质量 D 溶质质量.
您最近一年使用:0次