生产实际和实验室中有很多金属材料。
(1)铁制品表面经常涂上一层铝粉,铝具有较好的抗腐蚀性能的原因是什么______ ?
(2)为验证质量守恒定律,某同学设计了如图实验。说明该实验不能达到实验目的的理由______ 。
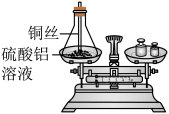
(3)探究金属活动性顺序时,某学生测定硫酸铜溶液的pH<7。将锌粒放入硫酸铜溶液中(溶剂不参与反应),锌粒表面有紫红色物质析出,还有无色无味气体产生的“异常”现象。推测该气体可能是_____________ 。
(4)某兴趣小组想从含有氯化亚铁、氯化铜的废液中回收金属铜和氯化亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:
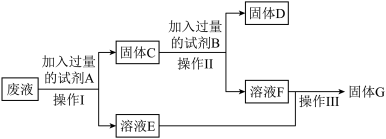
①操作Ⅲ的名称是_____________ ,除去的物质是_____________ (填化学式)。
②操作Ⅱ中加入过量的试剂B的目的是什么______ ?
③写出加入过量试剂A发生反应的化学方程式______ 。
(1)铁制品表面经常涂上一层铝粉,铝具有较好的抗腐蚀性能的原因是什么
(2)为验证质量守恒定律,某同学设计了如图实验。说明该实验不能达到实验目的的理由

(3)探究金属活动性顺序时,某学生测定硫酸铜溶液的pH<7。将锌粒放入硫酸铜溶液中(溶剂不参与反应),锌粒表面有紫红色物质析出,还有无色无味气体产生的“异常”现象。推测该气体可能是
(4)某兴趣小组想从含有氯化亚铁、氯化铜的废液中回收金属铜和氯化亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:

①操作Ⅲ的名称是
②操作Ⅱ中加入过量的试剂B的目的是什么
③写出加入过量试剂A发生反应的化学方程式
2018九年级下·河南南阳·学业考试 查看更多[2]
更新时间:2020-11-02 19:17:39
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】定量研究对于化学科学发展有重大作用,因此我们应能利用质量守恒定律解决一些实际问题。
(1)某物质完全燃烧后生成二氧化碳和水。则该物质一定含有的元素是______
(2)下图A、B、C三个实验用于验证质量守恒定律,每个实验至少需要进行_____ (填“1”“2”“3”)次称量;图A实验中气球的作用__________ ;做图B实验时,将试管中的盐酸与烧杯中的碳酸钠混合时看到的现象:________ ,这三个实验中不适合用于验证质量守恒定律的是_______ 选填序号)。

(3)取63.2g高锰酸钾,加热一段时间后停止,共收集到3.2g氧气。计算:
①已反应的高锰酸钾的质量为_______ 克。
②剩余固体中氧元素的质量分数为______ 。(精确到0.1%)
(1)某物质完全燃烧后生成二氧化碳和水。则该物质一定含有的元素是
(2)下图A、B、C三个实验用于验证质量守恒定律,每个实验至少需要进行

(3)取63.2g高锰酸钾,加热一段时间后停止,共收集到3.2g氧气。计算:
①已反应的高锰酸钾的质量为
②剩余固体中氧元素的质量分数为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】请回答下列问题。
(一)用如图所示的 个实验验证质量守恒定律。
个实验验证质量守恒定律。
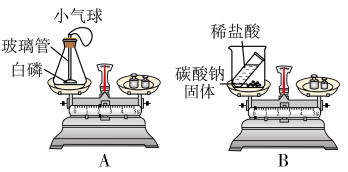
(1)图A所示实验:在实验前要在锥形瓶底部铺一层细沙,其作用是______ 。实验过程中,可看到气球的变化情况是 ______ 。
(2)在B实验中,实验前天平示数为102.2克,实验后天平示数为100克,该反应______ (填“遵循”、“不遵循”)质量守恒定律。
(二)现代生活中,人们越来越注重微量元素的摄取。碘元素对人体有着至关重要的作用。下图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:

(3)碘酸钾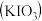 中碘元素、氧元素的质量比是
中碘元素、氧元素的质量比是________ 。
(4)计算一袋500g碘盐中含碘酸钾的质量是_________ mg (结果精确到0.1mg。)
(一)用如图所示的
 个实验验证质量守恒定律。
个实验验证质量守恒定律。
(1)图A所示实验:在实验前要在锥形瓶底部铺一层细沙,其作用是
(2)在B实验中,实验前天平示数为102.2克,实验后天平示数为100克,该反应
(二)现代生活中,人们越来越注重微量元素的摄取。碘元素对人体有着至关重要的作用。下图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:

(3)碘酸钾
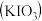 中碘元素、氧元素的质量比是
中碘元素、氧元素的质量比是(4)计算一袋500g碘盐中含碘酸钾的质量是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)为验证质量守恒定律,某同学设计了如图实验。该实验能否达到实验目的?请说明理由。________ 。
②为制得CO2的水溶液,CO2应从B装置的_______ (填“m”或“n”)口通入。
③将CO2的水溶液转移至烧杯,并组装C装置,置于阳光下一段时间,观察到有气泡产生,该气体可能是什么?_________ ;写出检验该气体的操作:_________ 。
(3)如图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。已知由一氧化碳发生装置得到的CO中混杂有CO2和H2O。_______ 。
②从环保的角度考虑,请写出一种尾气处理方法_________ 。
③若没有A装置,则该实验不能达到检验气体生成物的目的,请说明原因_________ 。
(4)实验室用32g高锰酸钾和二氧化锰的固体混合物制取氧气,充分反应后剩余固体质量为28.8g,则原混合物中高锰酸钾的质量分数是多少?
(1)为验证质量守恒定律,某同学设计了如图实验。该实验能否达到实验目的?请说明理由。
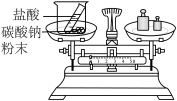
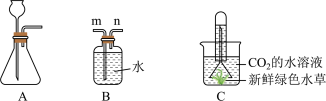
②为制得CO2的水溶液,CO2应从B装置的
③将CO2的水溶液转移至烧杯,并组装C装置,置于阳光下一段时间,观察到有气泡产生,该气体可能是什么?
(3)如图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。已知由一氧化碳发生装置得到的CO中混杂有CO2和H2O。
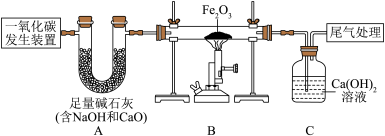
②从环保的角度考虑,请写出一种尾气处理方法
③若没有A装置,则该实验不能达到检验气体生成物的目的,请说明原因
(4)实验室用32g高锰酸钾和二氧化锰的固体混合物制取氧气,充分反应后剩余固体质量为28.8g,则原混合物中高锰酸钾的质量分数是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】人类文明进步与金属材料发展关系十分密切。请回答下列问题:
(1)2021年三星堆考古现场,“沉睡三千年,一醒惊天下”。1986年震惊世界的三星堆遗址,时隔三十余年后,辉煌灿烂的新发现再惊天下,一件件国之瑰宝次第现世,新发现6座古蜀“祭祀坑”,已出土黄金面具等500余件重要文物。历经几千年,出土的金器仍熠熠生辉,这是因为___________(选填字母编号)。
(2)铝合金不仅在日常生活中大量使用而且在航天航空领域中都发挥着重要的作用。
请回答下列问题:
①用铝合金制造飞机外壳的主要优点是___________ 、___________ 。
②下列关于铝合金材料的说法正确的是___________ 。
A.金属铝的化学性质非常稳定
B.铝表面容易生成一层致密的氧化铝薄膜,因而有良好的抗腐蚀性
C.废旧铝合金没有回收价值
(3)把铜锌加热熔合可制得黄铜合金,它有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组同学欲测定某黄铜中铜的质量分数(假设黄铜样品中不含其它杂质),取该黄铜样品25g于烧杯中,向其中逐渐加入溶质质量分数为9.8%的稀硫酸,烧杯中剩余固体的质量与加入稀硫酸的质量关系如图所示。

试回答:
①当加入稀硫酸至图中B点时,烧杯中溶液中的溶质是___________ (填写化学式)。
②通过计算求黄铜样品中铜的质量分数_________ 。(计算结果精确到0.1%)
(1)2021年三星堆考古现场,“沉睡三千年,一醒惊天下”。1986年震惊世界的三星堆遗址,时隔三十余年后,辉煌灿烂的新发现再惊天下,一件件国之瑰宝次第现世,新发现6座古蜀“祭祀坑”,已出土黄金面具等500余件重要文物。历经几千年,出土的金器仍熠熠生辉,这是因为___________(选填字母编号)。
| A.金器表面形成了一层致密的保护膜 | B.金的化学性质很稳定 |
请回答下列问题:
①用铝合金制造飞机外壳的主要优点是
②下列关于铝合金材料的说法正确的是
A.金属铝的化学性质非常稳定
B.铝表面容易生成一层致密的氧化铝薄膜,因而有良好的抗腐蚀性
C.废旧铝合金没有回收价值
(3)把铜锌加热熔合可制得黄铜合金,它有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组同学欲测定某黄铜中铜的质量分数(假设黄铜样品中不含其它杂质),取该黄铜样品25g于烧杯中,向其中逐渐加入溶质质量分数为9.8%的稀硫酸,烧杯中剩余固体的质量与加入稀硫酸的质量关系如图所示。

试回答:
①当加入稀硫酸至图中B点时,烧杯中溶液中的溶质是
②通过计算求黄铜样品中铜的质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】南京第二届夏季青奥会上,中国代表团获得金银铜奖牌共计63枚。
(1)体育馆内照明的导线大多数是铜导线,用铜做导线是利用金属铜的_____ 性和导电性。
(2)体育馆雄伟壮观的主体建筑使用了大量的金属铝板,铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,反应的化学方程式是_____ 。
(3)砳砳(lèlè)是2014年南京青奥会吉祥物,其外材料为纯羊毛,内充PET纤维。PET纤维属于_____ (选填“天然纤维”、“合成纤维”)。
(4)小彭同学想对家中一只10g手镯(银锌合金)中银的含量进行探究。在老师的指导下:他将该手镯放在烧杯中,用足量的稀硫酸分多次加入并与手镯充分反应,实验结果如图所示。

①如果小彭同学用所得的纯银制作一枚戒指,其质量不会超过_____ 克。
②试计算所用稀硫酸的溶质质量分数。(请在答卷纸上写出计算过程)_____
(1)体育馆内照明的导线大多数是铜导线,用铜做导线是利用金属铜的
(2)体育馆雄伟壮观的主体建筑使用了大量的金属铝板,铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,反应的化学方程式是
(3)砳砳(lèlè)是2014年南京青奥会吉祥物,其外材料为纯羊毛,内充PET纤维。PET纤维属于
(4)小彭同学想对家中一只10g手镯(银锌合金)中银的含量进行探究。在老师的指导下:他将该手镯放在烧杯中,用足量的稀硫酸分多次加入并与手镯充分反应,实验结果如图所示。

①如果小彭同学用所得的纯银制作一枚戒指,其质量不会超过
②试计算所用稀硫酸的溶质质量分数。(请在答卷纸上写出计算过程)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】材料学的发展水平,制约着制造业的发展水平。
(1)在铝合金、橡胶、涤纶几种物质中属于合成材料的是_______ 。
(2)被誉为“中国天眼”的500米口径球面射电望远镜的球面射电板是用铝合金板制作的。如图是铝在元素周期表中的部分信息,画出铝原子的结构示意图:_______ ,现代社会使用大量的铁、铝,铝制品具有良好抗腐蚀性能的原因是_______ 。

(3)许多钢铁制品外壳都用各种涂料覆盖,作用是_______ ;在实际工作中,常用稀硫酸除铁锈,反应的化学方程式是_______ 。
(4)为探究铁、铜两种金属的活动性,康康设计了如下实验:
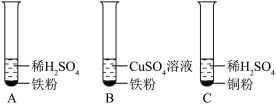
健健认为康康设计的实验不够科学简单,认为不需要的实验是_______ (填序号),将康康设计的实验B、C试管反应后的废液倒入废液缸中,过滤,向所得滤液中加入铁粉,若有气泡产生,则滤渣的成分是_______ 。
(5)氢气是我国重点发展的一种新能源。金属铝能与氢氧化钠溶液反应生成氢气( )。将100kg含铝94.5%的废铝加入到足量的氢氧化钠溶液中完全反应,计算能生成氢气
)。将100kg含铝94.5%的废铝加入到足量的氢氧化钠溶液中完全反应,计算能生成氢气_____ 千克?
(1)在铝合金、橡胶、涤纶几种物质中属于合成材料的是
(2)被誉为“中国天眼”的500米口径球面射电望远镜的球面射电板是用铝合金板制作的。如图是铝在元素周期表中的部分信息,画出铝原子的结构示意图:

(3)许多钢铁制品外壳都用各种涂料覆盖,作用是
(4)为探究铁、铜两种金属的活动性,康康设计了如下实验:

健健认为康康设计的实验不够科学简单,认为不需要的实验是
(5)氢气是我国重点发展的一种新能源。金属铝能与氢氧化钠溶液反应生成氢气(
 )。将100kg含铝94.5%的废铝加入到足量的氢氧化钠溶液中完全反应,计算能生成氢气
)。将100kg含铝94.5%的废铝加入到足量的氢氧化钠溶液中完全反应,计算能生成氢气
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】实验课上,同学们利用下列装置进行气体制备的学习。
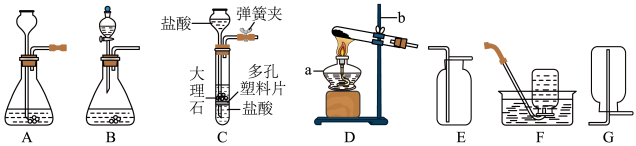
请你用已学的化学知识回答下列问题:
(1)图中仪器a的名称是______ ;仪器b的名称是______ 。
(2)在实验室里常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,不用粉末状大理石的原因是______ ,写出上述反应的化学方程式:______ 。
(3)装置A、B和C都能制取二氧化碳气体,但装置C与前两者相比较,你认为装置C的优势是______ 。
(4)实验室用加热无水乙酸钠固体和氢氧化钠固体制取甲烷气体。在通常情况下甲烷是一种无色无味的气体,难溶于水,密度比空气小。现实验室制取较纯净的甲烷应选用的发生和收集装置是______ 。(填字母编号)
(5)若用装置B制取氢气,原料是锌和稀硫酸,则该反应的化学方程式为______ 。
(6)在实验室用25g大理石与足量的稀盐酸完全反应(杂质不反应),可以生成8.8g的二氧化碳气体,则大理石中碳酸钙的质量分数是多少?

请你用已学的化学知识回答下列问题:
(1)图中仪器a的名称是
(2)在实验室里常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,不用粉末状大理石的原因是
(3)装置A、B和C都能制取二氧化碳气体,但装置C与前两者相比较,你认为装置C的优势是
(4)实验室用加热无水乙酸钠固体和氢氧化钠固体制取甲烷气体。在通常情况下甲烷是一种无色无味的气体,难溶于水,密度比空气小。现实验室制取较纯净的甲烷应选用的发生和收集装置是
(5)若用装置B制取氢气,原料是锌和稀硫酸,则该反应的化学方程式为
(6)在实验室用25g大理石与足量的稀盐酸完全反应(杂质不反应),可以生成8.8g的二氧化碳气体,则大理石中碳酸钙的质量分数是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】合金有着广泛的应用。
(1)以下属于合金的是______。
(2)Mg2Cu是一种贮氢合金,如图是制取与贮存氢气的一种方法,

①ZnFe2O4中Fe的化合价为______ 。
②循环制氢体系中制取氢气的总反应的化学方程式是______ 。
③贮氢反应过程中,一定质量的Mg2Cu合金完全吸收氢气,生成MgH2、合金MgCu2的混合物,将该混合物与过量的稀盐酸完全反应放出氢气的质量______ Mg2Cu合金吸收氢气的质量。(选填“大于”、“等于”或“小于”)。(已知:MgH2+2HCl=MgCl2+2H2↑)。
(3)生铁和钢均为铁的合金。
①生铁的含碳量______ 钢的含碳量(选填“大于”、“等于”或“小于”)。
②取一定量生铁与足量稀硫酸充分反应后,产生0.1g氢气。则该生铁样品中含铁的质量是多少(生铁中其余成分均不与稀硫酸反应)?______ (写出计算过程 )
(1)以下属于合金的是______。
| A.黄铜 | B.焊锡 | C.不锈钢 | D.磁铁矿 |
(2)Mg2Cu是一种贮氢合金,如图是制取与贮存氢气的一种方法,

①ZnFe2O4中Fe的化合价为
②循环制氢体系中制取氢气的总反应的化学方程式是
③贮氢反应过程中,一定质量的Mg2Cu合金完全吸收氢气,生成MgH2、合金MgCu2的混合物,将该混合物与过量的稀盐酸完全反应放出氢气的质量
(3)生铁和钢均为铁的合金。
①生铁的含碳量
②取一定量生铁与足量稀硫酸充分反应后,产生0.1g氢气。则该生铁样品中含铁的质量是多少(生铁中其余成分均不与稀硫酸反应)?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐3】近年来,我国载人航天事业取得了举世瞩目的成就。兴趣小组以“探究空间站水和氧气”为主题开展项目式学习。
【任务一】认识空间站氧气和水的再生
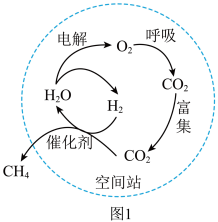
(1)空间站通过收集航天员尿液、汗液和呼出的水汽,深度净化,再生为饮用水。利用太阳能电池板供电,实现氧气和水的再生(如图1)。下列分析不正确的是___________(填字母序号)。
(2)实验室用加热高锰酸钾固体制氧气,该方法不适用于空间站提供氧气,理由是________ 。
【任务二】探究不同电解液和电极对水电解的影响
兴趣小组选择生活中材料做电极,在相同时间内做了一系列的对比实验,实验数据如下
(3)在上述实验条件下,实验数据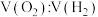 接近1:2的电解液和电极材料最佳组合是
接近1:2的电解液和电极材料最佳组合是________ 。
(4)稀硫酸做电解液时,铁丝不能做电极原因是___________ (用化学方程式解释)。
(5)影响电解水速率除上述因素外,还有___________ (写1点即可)。
【任务三】深度探究【任务二】中电解液稀硫酸和电极材料碳棒得到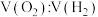 的比值比理论值偏小原因
的比值比理论值偏小原因
(6)兴趣小组在老师指导下,用CO2传感器测得图2烧杯上方CO2浓度随时间的变化曲线如图3。___________ 。
②由图3分析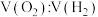 的比值比理论值偏小可能的原因
的比值比理论值偏小可能的原因___________ ;130s电解结束后CO2浓度继续变化的原因___________ 。
【任务一】认识空间站氧气和水的再生
(1)空间站通过收集航天员尿液、汗液和呼出的水汽,深度净化,再生为饮用水。利用太阳能电池板供电,实现氧气和水的再生(如图1)。下列分析不正确的是___________(填字母序号)。
| A.空间站中氧气的主要来源是水电解 |
| B.水循环系统利用催化剂可增加水的质量 |
| C.空间站水循环系统中氢原子利用率没有达到100% |
| D.可用过滤方法除去尿液浓缩后析出的固体 |
(2)实验室用加热高锰酸钾固体制氧气,该方法不适用于空间站提供氧气,理由是
【任务二】探究不同电解液和电极对水电解的影响
兴趣小组选择生活中材料做电极,在相同时间内做了一系列的对比实验,实验数据如下
| 电解液(浓度0.2kg/L) | 不同电极材料产生的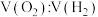 | ||||
| 碳棒 | 铜棒 | 保险丝 | 电阻丝 | 铁丝 | |
| NaOH溶液 | 1.09:6.9 | 3.35:7.7 | 2.95:6.9 | 3.4:7.3 | 3.2:6.51 |
| 稀硫酸 | 1.10:6.9 | 阳极产生的氧气很少 | 1.95:7.6 | 3.45:7.5 | 铁丝溶解 |
(3)在上述实验条件下,实验数据
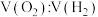 接近1:2的电解液和电极材料最佳组合是
接近1:2的电解液和电极材料最佳组合是(4)稀硫酸做电解液时,铁丝不能做电极原因是
(5)影响电解水速率除上述因素外,还有
【任务三】深度探究【任务二】中电解液稀硫酸和电极材料碳棒得到
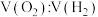 的比值比理论值偏小原因
的比值比理论值偏小原因(6)兴趣小组在老师指导下,用CO2传感器测得图2烧杯上方CO2浓度随时间的变化曲线如图3。

②由图3分析
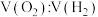 的比值比理论值偏小可能的原因
的比值比理论值偏小可能的原因
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐1】对于金属材料,我们应该从多角度了解。
Ⅰ.金属冶炼。《大治赋》记载由磁化铜矿(主要成分 ,杂质不与酸反应,也不溶于水)制取
,杂质不与酸反应,也不溶于水)制取 溶液,再用铁片浸取得到铜的方法.磁化铜矿中
溶液,再用铁片浸取得到铜的方法.磁化铜矿中 转化的流程如图:
转化的流程如图:______ 。
(2)写出滤液中加入Fe后一定发生反应的化学方程式______ 。
Ⅱ.金属的活动性。为比较金属M与Fe、Zn的金属活动性强弱,实验小组设计了如下图1装置(金属片均足量)的实验。待甲中充分反应后打开 ,使甲中溶液全部进入乙中,乙中无明显现象,打开
,使甲中溶液全部进入乙中,乙中无明显现象,打开 使乙中溶液全部进入丙中,观察到Zn片表面变黑。回答下列问题:
使乙中溶液全部进入丙中,观察到Zn片表面变黑。回答下列问题:
(4)如图2所示,向一定量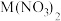 溶液中加入铁和锌的混合物粉末,充分反应过滤,得到溶液甲和固体乙。已知
溶液中加入铁和锌的混合物粉末,充分反应过滤,得到溶液甲和固体乙。已知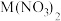 溶液呈无色。若溶液甲是无色,则溶液甲一定含有的金属阳离子是
溶液呈无色。若溶液甲是无色,则溶液甲一定含有的金属阳离子是______ 。(填离子符号)
Ⅰ.金属冶炼。《大治赋》记载由磁化铜矿(主要成分
 ,杂质不与酸反应,也不溶于水)制取
,杂质不与酸反应,也不溶于水)制取 溶液,再用铁片浸取得到铜的方法.磁化铜矿中
溶液,再用铁片浸取得到铜的方法.磁化铜矿中 转化的流程如图:
转化的流程如图: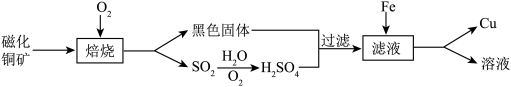
(2)写出滤液中加入Fe后一定发生反应的化学方程式
Ⅱ.金属的活动性。为比较金属M与Fe、Zn的金属活动性强弱,实验小组设计了如下图1装置(金属片均足量)的实验。待甲中充分反应后打开
 ,使甲中溶液全部进入乙中,乙中无明显现象,打开
,使甲中溶液全部进入乙中,乙中无明显现象,打开 使乙中溶液全部进入丙中,观察到Zn片表面变黑。回答下列问题:
使乙中溶液全部进入丙中,观察到Zn片表面变黑。回答下列问题: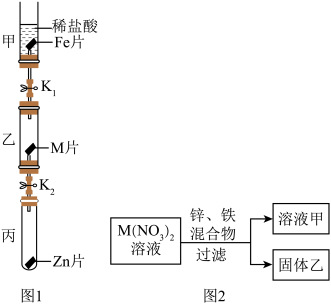
| A.甲中反应后得到黄色溶液 |
B.乙中现象证明金属活动性 |
| C.丙中反应后溶液质量增大 |
| D.将M片和Zn片互换位置仍能达到实验目的 |
(4)如图2所示,向一定量
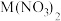 溶液中加入铁和锌的混合物粉末,充分反应过滤,得到溶液甲和固体乙。已知
溶液中加入铁和锌的混合物粉末,充分反应过滤,得到溶液甲和固体乙。已知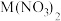 溶液呈无色。若溶液甲是无色,则溶液甲一定含有的金属阳离子是
溶液呈无色。若溶液甲是无色,则溶液甲一定含有的金属阳离子是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】金属及其制品是现代生活中不可缺少的材料和工具。
①某同学在实验室用6.5g粗锌(假设杂质不参与反应)和稀盐酸制取H2。
I.配制稀盐酸需要市售37%的浓盐酸稀释。“37%”的含义是_____ ;配制中需要用到的仪器除烧杯、胶头滴管、试剂瓶外,还需要_____ 。
Ⅱ.6.5g粗锌完全反应共产生H20.08mol,该粗锌中锌的质量分数为_____ (根据化学方程式计算)
②在“探究金属的性质”实验时,将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。若将所得滤渣放入稀盐酸中,有气泡产生,则滤液中可能含有的溶质是_____ ,滤渣中一定含有的金属是_____ 。
①某同学在实验室用6.5g粗锌(假设杂质不参与反应)和稀盐酸制取H2。
I.配制稀盐酸需要市售37%的浓盐酸稀释。“37%”的含义是
Ⅱ.6.5g粗锌完全反应共产生H20.08mol,该粗锌中锌的质量分数为
②在“探究金属的性质”实验时,将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。若将所得滤渣放入稀盐酸中,有气泡产生,则滤液中可能含有的溶质是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】金属及化合物是工农业生产及日常生活中应用广泛的物质。
(1)金属铝既可以与酸反应,又可以与碱反应。铝与NaOH溶液反应生成 NaAlO2和H2,写出反应的化学方程式_____________________ 。
(2)化学小组在Al(NO3)3、 Cu(NO3)2和AgNO3的混合溶液甲中加入一定量的锌粉,充分反应后过滤,得到固体乙和溶液丙,且溶液甲和溶液丙的质量相等。

写出一个有关反应的化学方程式_____________________ ;溶液丙中一定含有的金属离子(写化学符号)________________ 。若液体丙为蓝色,向固体乙上滴加盐酸____________________ (填“一定有”“可能有”或“一定没有”)气泡产生。
(3)在实验室里,可以利用如图装置制得铁。
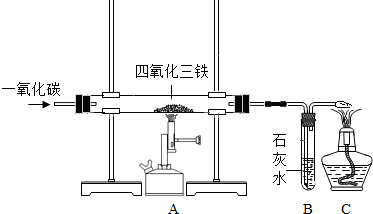
A处玻璃管内所发生反应的化学方程式为_________________________________ ;B处可观察到的现象是____________________ ;待四氧化三铁完全反应后,停止加热A处,在断开A、B之前应继续通入一氧化碳至A处玻璃管冷却。若不继续通入一氧化碳,可能出现的后果是____________________ 。
(1)金属铝既可以与酸反应,又可以与碱反应。铝与NaOH溶液反应生成 NaAlO2和H2,写出反应的化学方程式
(2)化学小组在Al(NO3)3、 Cu(NO3)2和AgNO3的混合溶液甲中加入一定量的锌粉,充分反应后过滤,得到固体乙和溶液丙,且溶液甲和溶液丙的质量相等。

写出一个有关反应的化学方程式
(3)在实验室里,可以利用如图装置制得铁。

A处玻璃管内所发生反应的化学方程式为
您最近一年使用:0次



