如图是某浓盐酸试剂瓶上标签的部分内容。
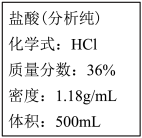
(1)将浓盐酸敞口放置,其质量分数会变小,这是由于浓盐酸具有较强的 ,所以,浓盐酸必须密封保存。
(2)将该瓶浓盐酸全部配制成溶质质量分数为11.8%(密度约为1.06g/mL)的盐酸,需加入水 mL。(需写出步骤)
(3)含杂质40%的石灰石100g与足量的稀盐酸充分反应,理论上可得到CO2多少克;(假设杂质不与稀盐酸反应,也不溶于水)(第三问写步骤)

(1)将浓盐酸敞口放置,其质量分数会变小,这是由于浓盐酸具有较强的 ,所以,浓盐酸必须密封保存。
(2)将该瓶浓盐酸全部配制成溶质质量分数为11.8%(密度约为1.06g/mL)的盐酸,需加入水 mL。(需写出步骤)
(3)含杂质40%的石灰石100g与足量的稀盐酸充分反应,理论上可得到CO2多少克;(假设杂质不与稀盐酸反应,也不溶于水)(第三问写步骤)
更新时间:2020-12-22 19:31:44
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】有一瓶较长时间敞口放置的熟石灰粉末试剂,为确定其变质情况,对该试剂进行如下定量测定:称取25g样品放入锥形瓶中,加入适量水充分振荡,再向锥形瓶中分步滴加一定浓度盐酸充分反应,测得数据如下表,已知
(1)m的值为_______ 。
(2)求出样品中所含变质产物碳酸钙的质量分数是多少?

| 加入盐酸的总质量/g | 20 | 40 | 60 | 80 | 100 | 120 |
| 产生气体的总质量/g | 0 | 2.2 | 4.4 | 6.6 | m | 8.8 |
(2)求出样品中所含变质产物碳酸钙的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为某钙片的商品标签,为测定钙片中钙元素的质量分数(假设钙片中其他物质不含钙元素,且不溶于水,也不与任何物质发生反应),某化学兴趣小组取20片钙片,进行如下实验:
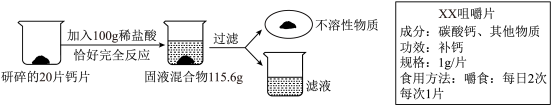
(1)上述实验过程中发生反应的化学方程式为______ ;
(2)根据已知条件列出求解钙片中参加反应的物质质量(x)的比例式______ ;
(3)钙片中钙元素的质量分数______ 。

(1)上述实验过程中发生反应的化学方程式为
(2)根据已知条件列出求解钙片中参加反应的物质质量(x)的比例式
(3)钙片中钙元素的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(已知:氯化钠在 20℃时的溶解度是36g,在90℃的溶解度是39g)
(1)将26%的氯化钠溶液与10%的氯化钠溶液等质量混合后升温至90℃溶质质量分数是________
(2)取上述溶液10g与28%的氯化钠溶液90g混合后降温到20℃,此时溶液的溶质质量分数是_________ (精确到0.1%)
(1)将26%的氯化钠溶液与10%的氯化钠溶液等质量混合后升温至90℃溶质质量分数是
(2)取上述溶液10g与28%的氯化钠溶液90g混合后降温到20℃,此时溶液的溶质质量分数是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】甲醛( )是一种防腐剂,同时也是一种有毒物质。为了测定溶液中甲醛的含量。某同学取含甲醛的溶液
)是一种防腐剂,同时也是一种有毒物质。为了测定溶液中甲醛的含量。某同学取含甲醛的溶液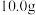 ,滴加过量酸性
,滴加过量酸性 溶液
溶液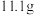 ,(反应的方程式为:
,(反应的方程式为: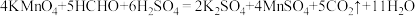 );整个过程中无沉淀产生。将产生的气体用
);整个过程中无沉淀产生。将产生的气体用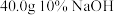 溶液恰好完全吸收,吸收后溶液的总质量为
溶液恰好完全吸收,吸收后溶液的总质量为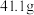 ;试计算。(已知
;试计算。(已知 的相对分子质量为151)
的相对分子质量为151)
(1)甲醛中碳氢元素的质量比_____ 。
(2)若用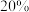 的溶液配制
的溶液配制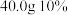 的
的 ,需要加入水的质量。
,需要加入水的质量。
(3)所得溶液中 的质量分数。
的质量分数。
 )是一种防腐剂,同时也是一种有毒物质。为了测定溶液中甲醛的含量。某同学取含甲醛的溶液
)是一种防腐剂,同时也是一种有毒物质。为了测定溶液中甲醛的含量。某同学取含甲醛的溶液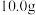 ,滴加过量酸性
,滴加过量酸性 溶液
溶液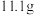 ,(反应的方程式为:
,(反应的方程式为: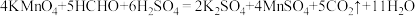 );整个过程中无沉淀产生。将产生的气体用
);整个过程中无沉淀产生。将产生的气体用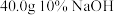 溶液恰好完全吸收,吸收后溶液的总质量为
溶液恰好完全吸收,吸收后溶液的总质量为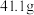 ;试计算。(已知
;试计算。(已知 的相对分子质量为151)
的相对分子质量为151)(1)甲醛中碳氢元素的质量比
(2)若用
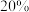 的溶液配制
的溶液配制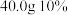 的
的 ,需要加入水的质量。
,需要加入水的质量。(3)所得溶液中
 的质量分数。
的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将一定质量的浓盐酸盛于烧杯中,敞口放置在实验室安全之处。
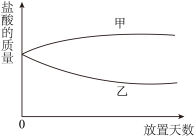
(1)浓盐酸的质量和放置天数关系的曲线(见如图)正确的是______ (填写“甲”或“乙”)。
(2)随着放置天数的增加,浓盐酸的质量发生变化的主要原因是______ 。
(3)称取1.6gFe2O3于烧杯中,与一定量稀盐酸恰好完全反应。
在反应过程中可以看到的现象是①______ ;②______ ;请写出化学方程式并计算参加反应的HCl的质量______ 。

(1)浓盐酸的质量和放置天数关系的曲线(见如图)正确的是
(2)随着放置天数的增加,浓盐酸的质量发生变化的主要原因是
(3)称取1.6gFe2O3于烧杯中,与一定量稀盐酸恰好完全反应。
在反应过程中可以看到的现象是①
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】如图是某硫酸试剂瓶的标签。该硫酸敞口放置一段时间,溶质质量分数会___________ (填“增大”“减小”或“不变”);实验室要用该浓硫酸配制1840g质量分数为9.8%的稀硫酸,需要该硫酸的体积为___________ mL。


您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】请完成下列填空。
(1)如图信息,瓶中溶液长期放置后溶质质量分数变小,是因为该物质具有____ 性。

(2)某探究小组的同学对某工业废水(含有H2SO4、HNO3)中H2SO4的含量进行测定。取50g废水于烧杯中,加入足量BaCl2溶液、过滤、洗涤、干燥,得BaSO4固体11.65g。请解答下列问题:
①计算50g废水中H2SO4的溶质质量分数___ ;
②若改用KOH溶液(利用消耗的KOH的质量)测定50g废水中H2SO4的含量,结果可能会________ (选填“偏低”、“偏高”或“不变”),原因是 ____________________ 。
(1)如图信息,瓶中溶液长期放置后溶质质量分数变小,是因为该物质具有

(2)某探究小组的同学对某工业废水(含有H2SO4、HNO3)中H2SO4的含量进行测定。取50g废水于烧杯中,加入足量BaCl2溶液、过滤、洗涤、干燥,得BaSO4固体11.65g。请解答下列问题:
①计算50g废水中H2SO4的溶质质量分数
②若改用KOH溶液(利用消耗的KOH的质量)测定50g废水中H2SO4的含量,结果可能会
您最近一年使用:0次



