16. 小红同学进行酸碱中和反应的实验(如图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液颜色没有变化。于是她对烧杯中的溶液进行了以下探究:

(1)实验过程中,玻璃棒的作用是
____。写出氢氧化钠和盐酸反应的方程式
____(2)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸过量。小明同学却断定不可能“氢氧化钠有剩余”,他的理由是:
____;
(3)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写如表:
| 实验方法 | 可观察到的现象 | 结论 |
| 将少量锌粒放入试管中,然后从烧杯中取出适量溶液至试管中 | ____ | 盐酸过量 |
| 无明显现象 | 盐酸与氢氧化钠恰好完全反应 |
(4)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的。你认为其中不正确的是
_(填序号)。
A 生锈的铁钉
B 氢氧化铜
C 硫酸钠粉末
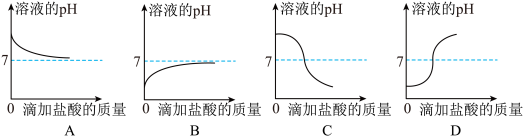
(5)如图曲线能够表示小红所做实验中溶液pH变化趋势的是
___(填序号)。
(6)氢氧化钠是实验室常用的药品,下列相关说法中,正确的是
_______A 称量:可将氢氧化钠固体直接放在天平左边托盘上进行称量。
B 溶解:氢氧化钠固体溶于水放出大量的热。
C 应急:氢氧化钠沾到皮肤上,先用大量水冲洗,再涂上3%—5%的稀盐酸。
D 保存:氢氧化钠固体易潮解和变质,应密封保存。