某实验小组拟利用相同条件下等质量的同种酸溶液与金属反应来探究“金属活动性与反应放出热量”之间的关系。实验装置如“1图”;实验完成后,根据传感器探头测量的从反应开始到反应停止时的数值绘制的曲线图如“2图”;实验所用酸与金属粉末的种类和质量如下表。请回答问题并进行相关计算。
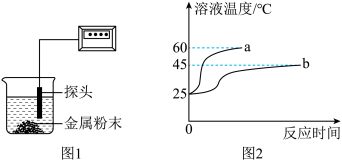
(1)根据实验探究目的,对比曲线a、b,可得出的结论是_____。
(2)计算6.5g锌粉充分反应时,产生氢气的质量,写出具体计算过程。
(3)三组实验反应完成后,烧杯底部有金属粉末剩余的是_____(填实验编组号)。
(4)在“2图”中画出曲线c的大致位置及趋势。

| 实验编组 | 等质量稀硫酸 | 金属粉末质量/种类 | 对应曲线 |
| ① | 含H2SO49.8g | 6.5g/镁 | a |
| ② | 含H2SO49.8g | 6.5g/锌 | b |
| ③ | 含H2SO49.8g | 6.5g/铁 | c(待绘制) |
(2)计算6.5g锌粉充分反应时,产生氢气的质量,写出具体计算过程。
(3)三组实验反应完成后,烧杯底部有金属粉末剩余的是_____(填实验编组号)。
(4)在“2图”中画出曲线c的大致位置及趋势。
20-21九年级上·广东佛山·期末 查看更多[12]
广东省佛山市顺德区2020-2021学年九年级上学期期末化学试题(已下线)2021中考广东省化学模拟试题(五)广东省佛山市南海区桂城街道映月中学2020-2021学年九年级下学期第一次月考化学试题广东省韶关市新丰县2020-2021学年九年级下学期3月月考化学试题(已下线)化学-(重庆卷)【试题猜想】2021年中考考前最后一卷2021年广东省珠海市香洲区文园中学中考三模化学试题2021年广东省韶关市新丰县中考化学模拟试题(3月份)广东省惠州市2021-2022学年九年级上学期期末化学试题广东省汕头市金平区金园实验中学2021-2022学年九年级上学期第三阶段限时训练化学试题(已下线)卷3-备战2022年中考化学【名校地市好题必刷】全真模拟卷(重庆专用)·第一辑广东省韶关市乐昌市第一中学2021-2022学年九年级下学期开学质量检测化学试题广东省佛山市禅城区佛山市外国语学校2022-2023学年九年级上学期第十六周诊断性练习化学试题
更新时间:2021-01-21 12:38:16
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】化学研究小组利用加热后的废旧铜丝与100g 9.8%的稀硫酸溶液完全反应制备硫酸铜,再对溶液加热、冷却结晶得到硫酸铜晶体,并测定晶体中结晶水的含量。请回答下列问题:
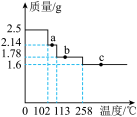
(1)完全反应能制得多少g硫酸铜。
(2)取2.5g硫酸铜晶体加热失水,得到不同温度下固体的质量曲线(又叫热重曲线):
①通过计算确定硫酸铜晶体的化学式_________ 。
②通过计算确定b点固体物质的化学式_________ 。

(1)完全反应能制得多少g硫酸铜。
(2)取2.5g硫酸铜晶体加热失水,得到不同温度下固体的质量曲线(又叫热重曲线):
①通过计算确定硫酸铜晶体的化学式
②通过计算确定b点固体物质的化学式
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】为测定混有Na2CO3的食盐纯度,做了4次测定,每次都取一定质量的样品和200g溶质质量分数为3.65%的盐酸(溶质为HCl),将样品配制成溶液后逐滴滴加到所取盐酸中发生反应Na2CO3 +HCl→NaCl+H2O+CO2↑(未配平),产生的气体质量与所用的样品质量关系如下表所示:
求样品中Na2CO3的纯度(保留一位小数,写出解题过程)。__________
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 盐酸质量(g) | 200 | 200 | 200 | 200 |
| 样品质量(g) | 10.6 | 53 | 265 | 300 |
| 气体质量(g) | 0.44 | 2.2 | 4.4 | 4.4 |
求样品中Na2CO3的纯度(保留一位小数,写出解题过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】小明在实验室发现一瓶未知浓度的氢氧化钡溶液,为方便以后使用,他对其浓度进行了测定。取20.0g此氢氧化钡溶液于烧杯中,逐滴滴加溶质质量分数为7.3%的稀盐酸,并随时对反应后的溶液用pH计(一种测定溶液pH的仪器)测定溶液的pH,所得数据如表:
试回答:
(1)当滴加稀盐酸的质量为9.8g时,溶液中的溶质是___________ ;
(2)计算所测氢氧化钡溶液中溶质的质量分数。(写出过程)
| 加入稀盐酸的质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| 溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
(1)当滴加稀盐酸的质量为9.8g时,溶液中的溶质是
(2)计算所测氢氧化钡溶液中溶质的质量分数。(写出过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】黄铜是由铜和锌组成的合金,常用于制造阀门、水管等。化学小组利用某黄铜片样品进行了如下实验。
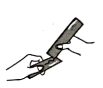
(1)按如图所示操作将黄铜片和纯铜片进行相互刻画,只有纯铜片上留下明显的划痕。据此得出的结论是______。
(2)证明此黄铜样品不是黄金,下列方法可行的是______(选填字母序号)。
A.直接观察颜色
B.在空气中灼烧后观察颜色
C.放入盐酸中观察是否被腐蚀
(3)将该样品加工成粉末,取一定质量的粉末加入硝酸银溶液中,充分反应后过滤,得到蓝色滤液和滤渣。则滤渣中一定有______,可能有______。
(4)利用如图所示装置测定该黄铜样品中铜的质量分数。取10g该黄铜粉末于烧杯中,分4次向其中加入稀盐酸。每次充分反应后称量烧杯及反应剩余物总质量,实验数据见下表。
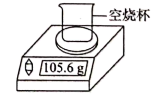
请计算该黄铜样品中铜的质量分数______(写出计算过程)。

(1)按如图所示操作将黄铜片和纯铜片进行相互刻画,只有纯铜片上留下明显的划痕。据此得出的结论是______。
(2)证明此黄铜样品不是黄金,下列方法可行的是______(选填字母序号)。
A.直接观察颜色
B.在空气中灼烧后观察颜色
C.放入盐酸中观察是否被腐蚀
(3)将该样品加工成粉末,取一定质量的粉末加入硝酸银溶液中,充分反应后过滤,得到蓝色滤液和滤渣。则滤渣中一定有______,可能有______。
(4)利用如图所示装置测定该黄铜样品中铜的质量分数。取10g该黄铜粉末于烧杯中,分4次向其中加入稀盐酸。每次充分反应后称量烧杯及反应剩余物总质量,实验数据见下表。

| 实验序号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀盐酸质量/g | 10 | 10 | 10 | 10 |
| 烧杯及反应剩余物质量/g | 125.56 | 135.52 | 145.50 | 155.50 |
请计算该黄铜样品中铜的质量分数______(写出计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐2】取锌、铜的混合物8g与154.7g稀硫酸恰好完全反应,称得剩余物质的总质量为162.5g。请计算:
(1)产生氢气的质量是多少?_______
(2)反应后所得溶液中溶质的质量分数是多少?_______
(1)产生氢气的质量是多少?_______
(2)反应后所得溶液中溶质的质量分数是多少?_______
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】往100.0g含有硝酸铜和硝酸银的混合溶液中加入镁粉,加入镁粉的质量与溶液质量变化如图所示。请分析计算:
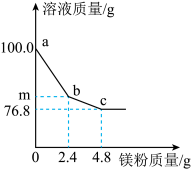
(1)图中a→b段表示镁粉与混合溶液中的 反应(填化学式),m的值为 。
(2)原混合溶液中硝酸铜的质量分数是多少?(写出计算过程,精确到0.1%)

(1)图中a→b段表示镁粉与混合溶液中的 反应(填化学式),m的值为 。
(2)原混合溶液中硝酸铜的质量分数是多少?(写出计算过程,精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】徐州地区石灰石资源丰富。某化学兴趣小组称取8.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
请计算:
(1)8.0g石灰石样品中碳酸钙的质量是______ 。
(2)10g稀盐酸能与_____ g碳酸钙正好完全反应:
(3)40g稀盐酸中含HCl的质量。(写出计算过程)
| 稀盐酸用量g | 剩余固体的质量g | |
| ① | 10 | 6 |
| ② | 10 | 4 |
| ③ | 10 | 2 |
| ④ | 10 | 1.2 |
请计算:
(1)8.0g石灰石样品中碳酸钙的质量是
(2)10g稀盐酸能与
(3)40g稀盐酸中含HCl的质量。(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】一水草酸钙(CaC2O4·H2O,相对分子质量为146)可用作分离稀有金属的载体。为研究一水草酸钙的热分解性质,进行如下实验:准确称取36.5g样品加热,,样品的固体质量随温度的变化如图所示。(相对分子质量:CaC2O4·H2O -146、CaC2O4-128、CaCO3-100、CaO-56)
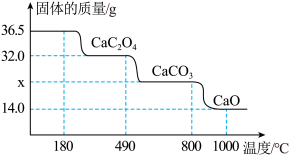
(1)CaC2O4·H2O中钙元素和氧元素的质量比为_______ 。
(2)温度加热到______ ℃时一水草酸钙开始分解;温度由490℃升高到800℃时分解生成的气体能燃烧且有毒,该气体名称为________ 。
(3)计算图中 的值是多少?(写出计算过程)
的值是多少?(写出计算过程)
(4)理论上等质量的下列物质所含钙元素最多的是_______ (填字母序号)。
a. CaC2O4·H2O b. CaC2O4 c. CaCO3 d.CaO
(5)研究表明CaC2O4·H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。据图分析,CaO捕捉CO2的反应温度应______ (填“高于”或“低于”)800℃。

(1)CaC2O4·H2O中钙元素和氧元素的质量比为
(2)温度加热到
(3)计算图中
 的值是多少?(写出计算过程)
的值是多少?(写出计算过程)(4)理论上等质量的下列物质所含钙元素最多的是
a. CaC2O4·H2O b. CaC2O4 c. CaCO3 d.CaO
(5)研究表明CaC2O4·H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。据图分析,CaO捕捉CO2的反应温度应
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】二氧化锰因应用广泛而备受关注。仁杰研究小组采用下图装置通过焙烧 MnCO3制取 MnO2,发生反应的化学方程式为:
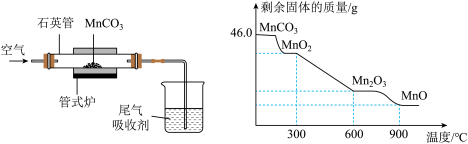
(1)实验过程中,石英管内剩余固体的质量和成分随温度的变化如上图所示,则焙烧MnCO3制取 MnO2应该控制反应的温度不高于___________ ℃。
(2)若加热到 300—900℃时,锰的氧化物会分解产生一种常见气体,该气体为__________ (填化学式)。
(3)试根据化学方程式求 46.0gMnCO3通过熔烧最多制得的 MnO2的质量是多少?(请写出计算过程)


(1)实验过程中,石英管内剩余固体的质量和成分随温度的变化如上图所示,则焙烧MnCO3制取 MnO2应该控制反应的温度不高于
(2)若加热到 300—900℃时,锰的氧化物会分解产生一种常见气体,该气体为
(3)试根据化学方程式求 46.0gMnCO3通过熔烧最多制得的 MnO2的质量是多少?(请写出计算过程)
您最近一年使用:0次



