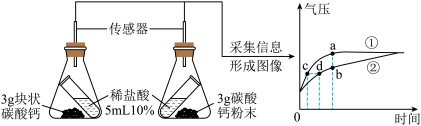
利用数据传感技术可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。某同学倾斜锥形瓶,使试管内的稀盐酸流入瓶中与碳酸钙发生反应,测得瓶内气压随时间的变化如图所示。_______ (填“①”或“②”)表示块状碳酸钙与稀盐酸的反应,b点所得溶液中的溶质是_______ (填化学式)。
(2)通过上述实验可得影响反应速率的因素之一是_______ 。
(3)上述对比实验产生的二氧化碳质量关系_______ 。
(2)通过上述实验可得影响反应速率的因素之一是
(3)上述对比实验产生的二氧化碳质量关系
更新时间:2021/01/29 15:26:20
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】某化学研究小组对蜡烛(主要由碳、氢元素组成)燃烧进行了如下探究。

(1)设计图1所示实验,锥形瓶中发生反应的化学方程式为__________ ;请推测靠近三通管__________ (填“上口”或“下口”)的火柴火焰熄灭,理由是____________________ 。
(2)某同学用大烧杯将高低2支燃烧的蜡烛罩住(如图2所示),观察到高的蜡烛先熄灭,低的蜡烛后熄灭。
【提出问题】导致高的蜡烛先熄灭的原因是什么?
【猜想与假设】假设1:可能是高蜡烛火焰附近的二氧化碳浓度过高导致其先熄灭;
假设2:可能是高蜡烛火焰附近的氧气浓度过低导致其先熄灭。
【设计实验】甲同学按图2装置进行实验,点燃蜡烛,用大烧杯罩住。一段时间后,发现贴在烧杯内上部的滤纸条先褪色(石灰水能使酚酞变红,碳酸钙不能使酚酞变红),说明此时高蜡烛附近的二氧化碳浓度比低蜡烛附近的二氧化碳浓度__________ (填“高”或“低”)。
(3)为进一步验证假设1,乙同学收集一瓶含20%氧气和80%二氧化碳的气体,将点燃的蜡烛慢慢伸入瓶中并密闭,蜡烛燃烧一段时间后慢慢熄灭,根据实验现象可知,假设1__________ (填“合理”或“不合理”),原因是____________________ 。
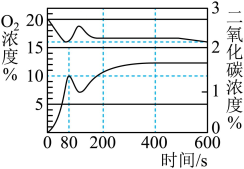
(4)丙同学使用传感器测得密闭装置内蜡烛从燃烧到熄灭的过程中(80s时蜡烛熄灭)装置内氧气和二氧化碳含量的变化曲线如图3。则可得出蜡烛燃烧的条件是氧气的浓度__________ 。
(5)【得出结论】经过以上实验可知,假设__________ 成立。

(1)设计图1所示实验,锥形瓶中发生反应的化学方程式为
(2)某同学用大烧杯将高低2支燃烧的蜡烛罩住(如图2所示),观察到高的蜡烛先熄灭,低的蜡烛后熄灭。
【提出问题】导致高的蜡烛先熄灭的原因是什么?
【猜想与假设】假设1:可能是高蜡烛火焰附近的二氧化碳浓度过高导致其先熄灭;
假设2:可能是高蜡烛火焰附近的氧气浓度过低导致其先熄灭。
【设计实验】甲同学按图2装置进行实验,点燃蜡烛,用大烧杯罩住。一段时间后,发现贴在烧杯内上部的滤纸条先褪色(石灰水能使酚酞变红,碳酸钙不能使酚酞变红),说明此时高蜡烛附近的二氧化碳浓度比低蜡烛附近的二氧化碳浓度
(3)为进一步验证假设1,乙同学收集一瓶含20%氧气和80%二氧化碳的气体,将点燃的蜡烛慢慢伸入瓶中并密闭,蜡烛燃烧一段时间后慢慢熄灭,根据实验现象可知,假设1
(4)丙同学使用传感器测得密闭装置内蜡烛从燃烧到熄灭的过程中(80s时蜡烛熄灭)装置内氧气和二氧化碳含量的变化曲线如图3。则可得出蜡烛燃烧的条件是氧气的浓度

(5)【得出结论】经过以上实验可知,假设
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】小明在查阅资料时得知CO2在高温时能与木炭反应生成CO,他决定对该反应进行探究。
【提出问题】CO2与木炭在高温条件下反应是否生成CO?
【实验探究】小明设计了下图的实验方案,并进行实验。
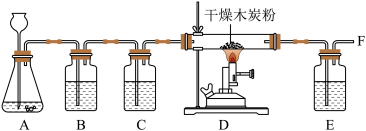
(1)A中用石灰石与稀盐酸反应的化学方程式为___________________ 。
(2)检查装置A气密性的方法是__________________________________________ 。
(3)B中装有饱和碳酸氢钠溶液,其作用是除去CO2气体中混有的少量HCl气体。C中装有浓硫酸,其作用是__________________ 。
(4)E中氢氧化钠溶液的作用是__________________ 。
【实验结论】经检验F处的气体为CO。结论:CO2在高温条件下与木炭反应生成了CO。
【实验反思】
有同学对A装置作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中,改进后的优点是_________________ 。
【实验拓展】
撤去B,按A→C→D→E顺序连接。然后A中用二氧化锰和过氧化氢溶液混合生成O2,反应的化学方程式为_________________ 。此时要检验该实验条件下D中木炭所发生反应的所有生成物,除在F处点燃并检验生成物外,还需要补充和完善的实验是 ________________ 。
【提出问题】CO2与木炭在高温条件下反应是否生成CO?
【实验探究】小明设计了下图的实验方案,并进行实验。

(1)A中用石灰石与稀盐酸反应的化学方程式为
(2)检查装置A气密性的方法是
(3)B中装有饱和碳酸氢钠溶液,其作用是除去CO2气体中混有的少量HCl气体。C中装有浓硫酸,其作用是
(4)E中氢氧化钠溶液的作用是
【实验结论】经检验F处的气体为CO。结论:CO2在高温条件下与木炭反应生成了CO。
【实验反思】
有同学对A装置作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中,改进后的优点是
【实验拓展】
撤去B,按A→C→D→E顺序连接。然后A中用二氧化锰和过氧化氢溶液混合生成O2,反应的化学方程式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】牙膏中常用碳酸钙、二氧化硅等物质作为摩擦剂。某同学对牙膏中摩擦剂碳酸钙的含量进行探究。
【实验原理】测定C装置中生成的BaCO3沉淀的质量,通过计算确定牙膏中CaCO3的质量分数。
【查阅资料】CO2+Ba(OH)2===BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生。
【实验装置】
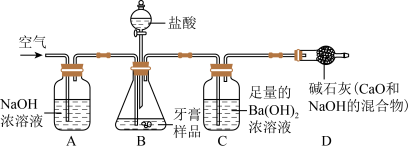
根据探究过程回答下列问题:
(1)装置B中发生反应的化学方程式_____ ;
(2)实验过程中需持续缓缓通入空气,其作用有:①搅拌B、C中的反应物,使其充分反应;②____ ;
(3)从C中过滤出BaCO3沉淀所需的玻璃仪器有烧杯、____ 和玻璃棒;
(4)若没有A装置,直接通入空气,则测得CaCO3的质量分数______ (填“偏大”、“偏小”或“不变”)。
【实验原理】测定C装置中生成的BaCO3沉淀的质量,通过计算确定牙膏中CaCO3的质量分数。
【查阅资料】CO2+Ba(OH)2===BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生。
【实验装置】

根据探究过程回答下列问题:
(1)装置B中发生反应的化学方程式
(2)实验过程中需持续缓缓通入空气,其作用有:①搅拌B、C中的反应物,使其充分反应;②
(3)从C中过滤出BaCO3沉淀所需的玻璃仪器有烧杯、
(4)若没有A装置,直接通入空气,则测得CaCO3的质量分数
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
【推荐1】某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素。(实验装置如图所示,夹持仪器已略去)
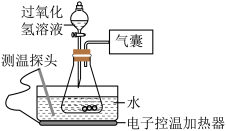
【猜想与假设】
影响过氧化氢分解速率的因素可能有温度、
溶液的浓度、催化剂种类。
【实验记录】同学们进行6组实验,实验记录如下:
【解释与结论】
(1)实验②中应加入过氧化氢溶液的体积x是______ mL。
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定______ 来比较过氧化氢的分解速率。
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是_____ (填序号)。
(4)通过实验①、②、④可得出的结论是______ 。
【反思与评价】
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是______ (答两点)。

【猜想与假设】
影响过氧化氢分解速率的因素可能有温度、
溶液的浓度、催化剂种类。
【实验记录】同学们进行6组实验,实验记录如下:
| 实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 过氧化氢溶液的浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
| 过氧化氢溶液的体积 | 6 | x | 6 | 6 | 6 | 6 |
| 水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
| 锥形瓶中的物质 | ……. | ……. | ……… | …….. | 0.5gNaCl | 0.5gFeCl3 |
| 60min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(1)实验②中应加入过氧化氢溶液的体积x是
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是
(4)通过实验①、②、④可得出的结论是
【反思与评价】
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室常用过氧化氢溶液和二氧化锰制取氧气,过氧化氢的分解速率受多种因素的影响。
查阅资料:将新制的浓度 5%的过氧化氢溶液加热到 80℃时就有较多氧气产生。
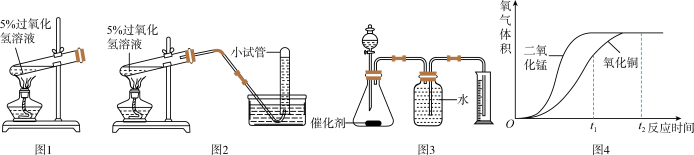
(1)请写出实验室用过氧化氢溶液和二氧化锰制取氧气的文字表达式___________ 。
(2)小红按图1装置进行实验,当试管中有大量气泡出现时,伸入带火星的木条,木条并未复燃,为此,她利用图2装置收集气体,再用带火星的木条检验,木条复燃,那么图1实验中带火星木条未复燃的原因是___________ 。
(3)下表是某小组同学探究影响过氧化氢分解速率部分因素的相关实验数据。
通过对比实验___________ (填序号)可知,过氧化氢分解速率与过氧化氢溶液的浓度有关。若x_____ 49.21(填“>”、“=”或“<”)可知温度越高,过氧化氢分解速率越快。
(4)某化学兴趣小组设计了实验来比较二氧化锰和氧化铜对过氧化氢分解的催化效果。
采用图3所示的装置,在常温下将两份等体积等浓度的过氧化氢溶液分别以同样速度快速滴入等质量的二氧化锰和氧化铜中,通过测量排出水的体积得到氧气的体积,同时记录下时间,得到氧气的体积和反应时间的关系如图4所示
结论:对过氧化氢分解催化效果较好的催化剂是___________ 。
拓展:由氧化铜催化的反应,t1-t2时间段反应速率逐渐变慢,原因是___________ 。
查阅资料:将新制的浓度 5%的过氧化氢溶液加热到 80℃时就有较多氧气产生。

(1)请写出实验室用过氧化氢溶液和二氧化锰制取氧气的文字表达式
(2)小红按图1装置进行实验,当试管中有大量气泡出现时,伸入带火星的木条,木条并未复燃,为此,她利用图2装置收集气体,再用带火星的木条检验,木条复燃,那么图1实验中带火星木条未复燃的原因是
(3)下表是某小组同学探究影响过氧化氢分解速率部分因素的相关实验数据。
| 实验序号 | 过氧化氢溶液的浓度/% | 过氧化氢溶液的体积/mL | 温度/℃ | 二氧化锰的用量/g | 收集氧气的体积/mL | 反应所需的时间/s |
| ① | 5 | 5 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 5 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 0 | 2 | 49.21 |
| ④ | 30 | 5 | 55 | 0 | 2 | x |
(4)某化学兴趣小组设计了实验来比较二氧化锰和氧化铜对过氧化氢分解的催化效果。
采用图3所示的装置,在常温下将两份等体积等浓度的过氧化氢溶液分别以同样速度快速滴入等质量的二氧化锰和氧化铜中,通过测量排出水的体积得到氧气的体积,同时记录下时间,得到氧气的体积和反应时间的关系如图4所示
结论:对过氧化氢分解催化效果较好的催化剂是
拓展:由氧化铜催化的反应,t1-t2时间段反应速率逐渐变慢,原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰。该小组同学进行了如下探究。
(1)铁丝在氧气中燃烧的符号表达式:_____ ,实验时要在瓶底放水的目的_____ ;
(2)探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。此可知:蜡烛燃烧产生的火焰是由_____ (填“固态”或“气态”)物质燃烧形成的;

(3)探究二:物质燃烧产生火焰的根本原因是什么?
【查阅资料】
由上表可知:物质燃烧能否产生火焰与其_____ (填“熔点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时,_____ (填“有”或“没有”)火焰产生。
(1)铁丝在氧气中燃烧的符号表达式:
(2)探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。此可知:蜡烛燃烧产生的火焰是由

(3)探究二:物质燃烧产生火焰的根本原因是什么?
【查阅资料】
| 物质 | 熔点/℃ | 沸点/℃ | 燃烧时温度/℃ |
| 石蜡 | 50—70 | 300—550 | 约600 |
| 铁 | 1535 | 2750 | 约1800 |
| 钠 | 97.8 | 883 | 约1400 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】小明同学在做家庭实验时,不小心将过氧化氢溶液溅到妈妈刚刚切好的土豆丝上,发现土豆丝上立即冒气泡,激发了小明的探究欲望,请你参与小明的探究。
(猜想)土豆丝可作过氧化氢分解的催化剂
(实验)设计并完成下表所示的探究实验:
(1)请你帮小明同学填写上表中未填完的空格。
(2)在小明的探究实验中,“实验二”起的作用是_____________ 。
(3)写出此实验中过氧化氢溶液分解的文字表达式_____________ 。
(答出以下问题每空奖励1分,试卷总分不超过40分)
(反思)
(4)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完全证明猜想是正确的,她补充的两个方面的实验是:_____________ 。
第一补充实验:______________________ 。
第二补充实验:_______________________ 。
(结论)通过上述同学所做的实验,我们知道了土豆丝可以作为过氧化氢制取氧气的催化剂。
(猜想)土豆丝可作过氧化氢分解的催化剂
(实验)设计并完成下表所示的探究实验:
(1)请你帮小明同学填写上表中未填完的空格。
| 实验操作 | 实验现象 | 实验结论 | 总结 | |
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是 | 土豆丝可作过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入土豆丝,伸入带火星的木条 | 没有明显现象 | 水和土豆丝不能放出氧气 | |
| 实验三 | 取5mL5%的过氧化氢溶液于试管中,加入土豆丝,伸入带火星的木条 | 土豆丝能加快过氧化氢的分解 |
(2)在小明的探究实验中,“实验二”起的作用是
(3)写出此实验中过氧化氢溶液分解的文字表达式
(答出以下问题每空奖励1分,试卷总分不超过40分)
(反思)
(4)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完全证明猜想是正确的,她补充的两个方面的实验是:
第一补充实验:
第二补充实验:
(结论)通过上述同学所做的实验,我们知道了土豆丝可以作为过氧化氢制取氧气的催化剂。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
Ⅰ.不稳定性
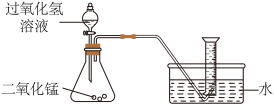
(1)如上图所示进行实验,过氧化氢分解的化学方程式为______ 。
(2)能用排水法收集O2的原因是______ 。
(3)探究温度对过氧化氢分解速率的影响。
同学们进行了如下的实验,实验数据如下表:
由此得出的结论是______ 。
Ⅱ.腐蚀性
【查阅资料】H2O2溶液有腐蚀性。
【进行实验】
同学们用铜片设计实验验证H2O2溶液的腐蚀性。(各组实验中H2O2溶液和稀硫酸所用浓度均相同)
将铜片分别浸泡在3种溶液中进行实验,如下表。
【解释与结论】
(4)实验①的作用是______ 。
(5)能说明铜片被腐蚀与H2O2溶液和稀硫酸均有关的实验组是______ 。
(6)铜片被腐蚀的反应如下,补全该反应的化学方程式。Cu + H2O2+ H2SO4=CuSO4 +□_______
Ⅰ.不稳定性

(1)如上图所示进行实验,过氧化氢分解的化学方程式为
(2)能用排水法收集O2的原因是
(3)探究温度对过氧化氢分解速率的影响。
同学们进行了如下的实验,实验数据如下表:
| 实验序号 | ① | ② | ③ |
| H2O2溶液的浓度 % | 30 | 30 | 30 |
| H2O2溶液的体积/mL | 6 | 6 | 6 |
| 温度/℃ | 20 | 35 | 55 |
| MnO2的用量/g | 0 | 0 | 0 |
| 收集O2的体积/mL | 0 | 1.9 | 7.8 |
| 反应时间 | 40 min | 40 min | 40 min |
Ⅱ.腐蚀性
【查阅资料】H2O2溶液有腐蚀性。
【进行实验】
同学们用铜片设计实验验证H2O2溶液的腐蚀性。(各组实验中H2O2溶液和稀硫酸所用浓度均相同)
将铜片分别浸泡在3种溶液中进行实验,如下表。
| 编号 | ① | ② | ③ |
| 实验 | 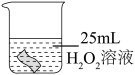 | 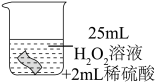 |  |
| 一段时间后的现象 | 无明显变化 | 铜片变小,溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
(4)实验①的作用是
(5)能说明铜片被腐蚀与H2O2溶液和稀硫酸均有关的实验组是
(6)铜片被腐蚀的反应如下,补全该反应的化学方程式。Cu + H2O2+ H2SO4=CuSO4 +□
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
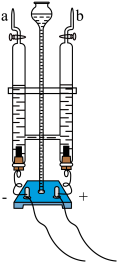
【推荐3】用如图所示装置探究水的组成。_______ 。
(2)用燃着的木条检验b中产生的气体,可观察到的现象是_________ 。
(3)该实验中,能证明“水中含有氢、氧元素”的依据是_________ 。
继续用该装置探究影响电解水反应快慢的因素。
【查阅资料】Ⅰ.向水中加入少量 可增强导电性:
可增强导电性:
Ⅱ.通常状况下,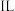 水中能溶解氧气约
水中能溶解氧气约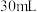 、氢气约
、氢气约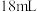 。
。
【进行实验】在不同条件下进行实验,数据记录如下:
【解释与结论】
(4)设计④⑤⑧的目的是_________ 。
(5)对比⑥~⑨,可得出的结论是_________ 。
(6)探究产生等量氢气时,电极种类对电解水反应快慢影响的实验是_______ (填序号)。
(7)通过本实验得出,影响电解水反应快慢的因素有_________ 。
【反思与评价】
(8)部分实验中,产生 氢气时,产生氧气的体积略小于
氢气时,产生氧气的体积略小于 ,其原因可能是
,其原因可能是________ 。
(2)用燃着的木条检验b中产生的气体,可观察到的现象是
(3)该实验中,能证明“水中含有氢、氧元素”的依据是
继续用该装置探究影响电解水反应快慢的因素。
【查阅资料】Ⅰ.向水中加入少量
 可增强导电性:
可增强导电性:Ⅱ.通常状况下,
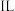 水中能溶解氧气约
水中能溶解氧气约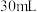 、氢气约
、氢气约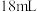 。
。【进行实验】在不同条件下进行实验,数据记录如下:
| 实验序号 | 电极种类 |  溶液浓度 溶液浓度 | 电压(V) | 氢气体积( ) ) | 所需时间('表示分,"表示秒) |
| ① | 锡棒 | 2.5% | 12 | 20 | 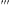 |
| ② | 锡棒 | 5% | 8 | 20 | 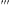 |
| ③ | 锡棒 | 10% | 16 | 20 | 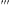 |
| ④ | 镀镍回形针 | 10% | 8 | 20 | 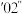 |
| ⑤ | 镀镍回形针 | 10% | 12 | 20 | 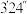 |
| ⑥ | 镀镍回形针 | 2.5% | 16 | 20 | 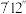 |
| ⑦ | 镀镍回形针 | 5% | 16 | 20 | 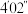 |
| ⑧ | 镀镍回形针 | 10% | 16 | 20 | 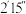 |
| ⑨ | 镀镍回形针 | 15% | 16 | 20 |  |
(4)设计④⑤⑧的目的是
(5)对比⑥~⑨,可得出的结论是
(6)探究产生等量氢气时,电极种类对电解水反应快慢影响的实验是
(7)通过本实验得出,影响电解水反应快慢的因素有
【反思与评价】
(8)部分实验中,产生
 氢气时,产生氧气的体积略小于
氢气时,产生氧气的体积略小于 ,其原因可能是
,其原因可能是
您最近一年使用:0次



