可燃冰是甲烷与水在低温、高压的条件下形成的无色冰状固体,极易燃烧,其主要成分是CH4⋅nH2O。在可燃冰开采过程中,甲烷容易泄漏,会加重温室效应。某化学小组的同学对甲烷燃烧的产物产生兴趣,进行了如下探究。
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质充分燃烧生成CO2,不充分燃烧生成CO;CO与人体内的血红蛋白结合,会造成人体缺氧和中毒;无水CuSO4遇水变蓝。
【猜想与假设】猜想一:CO、H2O;猜想二:___ ;猜想三:CO2、CO、H2O。
【实验探究】为了验证上述猜想与假设。将甲烷在一定量纯净氧气中燃烧的产物,依次通过如图所示装置进行验证。
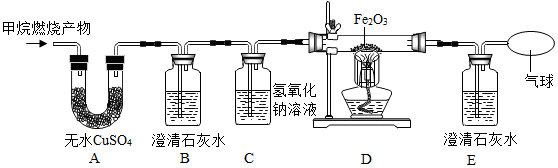
(1)实验开始时,先进行的操作是_______ (填序号)。
①通入甲烷燃烧产物
②加热
(2)实验中观察到A中____ ,B、E中澄清石灰水变浑浊,D中红色粉末变成黑色,由此推断猜想____ 成立。
(3)B装置中发生反应的化学方程式是_____ 。
(4)实验过程中C装置的作用是____ 。
【反思与交流】日常生活中,使用燃气热水器一定要注意通风,防止_____ 中毒。
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质充分燃烧生成CO2,不充分燃烧生成CO;CO与人体内的血红蛋白结合,会造成人体缺氧和中毒;无水CuSO4遇水变蓝。
【猜想与假设】猜想一:CO、H2O;猜想二:
【实验探究】为了验证上述猜想与假设。将甲烷在一定量纯净氧气中燃烧的产物,依次通过如图所示装置进行验证。

(1)实验开始时,先进行的操作是
①通入甲烷燃烧产物
②加热
(2)实验中观察到A中
(3)B装置中发生反应的化学方程式是
(4)实验过程中C装置的作用是
【反思与交流】日常生活中,使用燃气热水器一定要注意通风,防止
2020·江苏·中考真题 查看更多[4]
江苏省宿迁市2020年中考化学试题2021年江西省赣州市寻乌县中考模拟化学试题(已下线)2022江苏中考风向标-燃烧、灭火和爆炸江西省宜春市实验中学2020-2021学年九年级下学期第二段考试(联考)化学试题
更新时间:2021-03-21 09:06:54
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】天然气的主要成分是CH4,是一种使用广泛的化石能源,
(1)请写出甲烷燃烧的反应方程式:______ 。
【实验探究】某化学兴趣小组想对甲烷气体的其他相关知识进行深入研究。
【提出问题】他们发现甲烷的性质与氢气、一氧化碳有很多相似之处,那么甲烷有没有还原性呢?
【查阅资料】无水硫酸铜是白色固体,吸收水分后变为蓝色。
【实验探究】为探究上述问题,设计如下图装置并进行实验。

(2)实验开始时,先通一段时间甲烷的目的是______ 。
(3)加热一段时间后,观察到:
【结论】甲烷有还原性,能够还原金属氧化物,生成金属单质,以及种常见的非金属氧化物。
(4)请你根据上述反应的规律,写出甲烷在加热条件下还原氧化铜的化学方程式:______ 。
(1)请写出甲烷燃烧的反应方程式:
【实验探究】某化学兴趣小组想对甲烷气体的其他相关知识进行深入研究。
【提出问题】他们发现甲烷的性质与氢气、一氧化碳有很多相似之处,那么甲烷有没有还原性呢?
【查阅资料】无水硫酸铜是白色固体,吸收水分后变为蓝色。
【实验探究】为探究上述问题,设计如下图装置并进行实验。

(2)实验开始时,先通一段时间甲烷的目的是
(3)加热一段时间后,观察到:
| 实验现象 | 实验结论 | |
| 加热A处硬质试管 | 管中的固体粉末由红色全部变成黑色 | / |
| 取少量黑色粉末于试管中,加入适量稀硫酸 | 观察到 | 说明有铁生成 |
| 观察B装置 | 发现白色固体变 | 说明有水生成 |
| 观察C装置 | 观察到澄清石灰水变浑浊 | 说明有 |
【结论】甲烷有还原性,能够还原金属氧化物,生成金属单质,以及种常见的非金属氧化物。
(4)请你根据上述反应的规律,写出甲烷在加热条件下还原氧化铜的化学方程式:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室现有氯酸钾、二氧化锰、石灰石、蜡烛、火柴及以下仪器(如图),请回答:

(1)仪器⑦的名称是____________ ;
(2)若补充一种常见仪器,并利用上述部分仪器和药品可制取一种气体,该反应的化学方程式是_______________ 。
(3)若补充一种药品,还能制取二氧化碳,并探究其性质(如图)
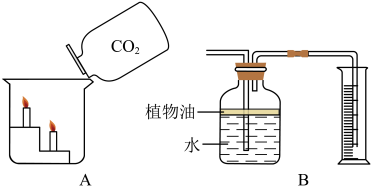
①补充的药品是_________________ ;
②图A观察到的现象说明二氧化碳具有的化学性质是______________ ;B中可用来测量生成二氧化碳气体的体积,其中在水面上放一层植物油的原因是______ 。
(4)2018年4月28日某媒体题为“排污工程施工,毒气放倒三人”的报道,引起某兴趣小组同学的思考。
【提出问题】排污管道中的毒气有什么成分?
【查阅资料】
I.排污管道中的大部分有机物在一定条件下发酵会产生CO、CO2、H2S、CH4等。
II.H2S气体能与CuSO4溶液反应生成黑色沉淀。
【提出猜想】小组同学对排污管道气含有上述气体中最少3种成分的猜想如下:
猜想1:有CO、CO2、H2S; 猜想2:有CO、CO2、CH4;
猜想3:有CO、H2S、CH4; 猜想4:有CO、CO2、H2S、CH4。
【实验方案】小组同学共同设计了如图所示的装置并进行探究(夹持仪器已省略)。

【问题讨论】
①如果A装置没有明显变化,则猜想__________ 成立;如果B装置没有明显变化,则猜想_________ 成立。
②要确证猜想4中是否有CH4,某同学认为图示装置有不足之处,需要在装置C与D之间加一个____________ 装置。改进后,若气体燃烧,且D装置内壁出现__________ ,证明气体中一定含有CH4。

(1)仪器⑦的名称是
(2)若补充一种常见仪器,并利用上述部分仪器和药品可制取一种气体,该反应的化学方程式是
(3)若补充一种药品,还能制取二氧化碳,并探究其性质(如图)

①补充的药品是
②图A观察到的现象说明二氧化碳具有的化学性质是
(4)2018年4月28日某媒体题为“排污工程施工,毒气放倒三人”的报道,引起某兴趣小组同学的思考。
【提出问题】排污管道中的毒气有什么成分?
【查阅资料】
I.排污管道中的大部分有机物在一定条件下发酵会产生CO、CO2、H2S、CH4等。
II.H2S气体能与CuSO4溶液反应生成黑色沉淀。
【提出猜想】小组同学对排污管道气含有上述气体中最少3种成分的猜想如下:
猜想1:有CO、CO2、H2S; 猜想2:有CO、CO2、CH4;
猜想3:有CO、H2S、CH4; 猜想4:有CO、CO2、H2S、CH4。
【实验方案】小组同学共同设计了如图所示的装置并进行探究(夹持仪器已省略)。

【问题讨论】
①如果A装置没有明显变化,则猜想
②要确证猜想4中是否有CH4,某同学认为图示装置有不足之处,需要在装置C与D之间加一个
您最近一年使用:0次
【推荐3】小明通过学习“蜡烛及其燃烧的探究”后,对蜡烛性质、家庭使用的天然气燃烧等产生了兴趣,于是开始了一系列实验。
实验一:探究石蜡的物理、化学性质。
(1)对于本实验使用的蜡烛有以下描述:①白色圆柱形固体;②有轻微的气味;③质地较软;④密度比水小;⑤有可燃性;⑥受热易熔化;⑦难溶于水;上述描述中属于蜡烛的化学性质的是_______ (填序号)。
实验二:对天然气及其燃烧的探究。
(2)用一支木筷迅速插入天然气火焰中片刻取出,观察到木筷表面出现的现象和蜡烛燃烧出现的现象相同:在最外层呈圆弧状黑斑,说明液化气燃烧的火焰_______ (填“是”或“不是”)分层的,做饭时应用_______ (填“内焰”“外焰”或“焰心”)对准锅所在位置加热。
(3)天然气的主要成分是甲烷,为了探究甲烷燃烧的生成物,小明将一个干冷的烧杯罩在天然气的火焰上方,烧杯内壁出现水雾,证明天然气燃烧有_______ 生成;取下烧杯,迅速向烧杯内倒入少量澄清石灰水,振荡,澄清石灰水变浑浊,证明天然气燃烧有_______ 生成。
【延伸拓展】化学变化中常伴随有发光、放热的现象。小明认为有发光、放热现象的变化不一定是化学变化,兴趣小组的同学对此展开了讨论和验证。
提出问题:有发光、放热现象的变化都是化学变化吗?
猜想1:都是化学变化
猜想2:不一定都是化学变化
【实验4】观察白炽灯内钨丝在通电前后的变化:
(4)①讨论:通电前后,钨丝本身没有发生变化,灯泡通电发光、放热属于_______ 变化,蜡烛燃烧属于_______ 变化。
②结论:猜想_______ (填“1”或“2”)正确。
实验一:探究石蜡的物理、化学性质。
(1)对于本实验使用的蜡烛有以下描述:①白色圆柱形固体;②有轻微的气味;③质地较软;④密度比水小;⑤有可燃性;⑥受热易熔化;⑦难溶于水;上述描述中属于蜡烛的化学性质的是
实验二:对天然气及其燃烧的探究。
(2)用一支木筷迅速插入天然气火焰中片刻取出,观察到木筷表面出现的现象和蜡烛燃烧出现的现象相同:在最外层呈圆弧状黑斑,说明液化气燃烧的火焰
(3)天然气的主要成分是甲烷,为了探究甲烷燃烧的生成物,小明将一个干冷的烧杯罩在天然气的火焰上方,烧杯内壁出现水雾,证明天然气燃烧有
【延伸拓展】化学变化中常伴随有发光、放热的现象。小明认为有发光、放热现象的变化不一定是化学变化,兴趣小组的同学对此展开了讨论和验证。
提出问题:有发光、放热现象的变化都是化学变化吗?
猜想1:都是化学变化
猜想2:不一定都是化学变化
【实验4】观察白炽灯内钨丝在通电前后的变化:
| 通电前 | 通电中 | 断电后 |
| 灯丝为银白色固体 | 发出白光,手摸灯泡感觉发热 | 灯丝为银白色固体 |
②结论:猜想
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】某实验小组用pH传感器探究盐酸和氢氧化钠的反应。测定结果如图所示。

(1)向烧瓶中缓慢注入稀盐酸,请写出能说明盐酸与氢氧化钠发生化学反应的曲线信息_____ 。
(2)该实验小组同学认为氢氧化钠溶液久置在空气中容易变质,如何证明某氢氧化钠溶液已经部分变质_____ ?(请简要写出实验步骤及现象)

(1)向烧瓶中缓慢注入稀盐酸,请写出能说明盐酸与氢氧化钠发生化学反应的曲线信息
(2)该实验小组同学认为氢氧化钠溶液久置在空气中容易变质,如何证明某氢氧化钠溶液已经部分变质
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某校化学兴趣小组在探究“酸碱盐的相关性质”时,做了如图一所示的两个实验,实验结束后,小组同学将两支试管中的废液同时倒入一个洁净的烧杯中(如图所示),观察到有气泡产生,为确认烧杯内溶液中溶质的成分,同学们进行了如下探究。

【查阅资料】Na2SO4溶液、NaCl溶液呈中性。
【提出猜想】猜想1:Na2SO4、NaCl;
猜想2:Na2SO4、NaCl和Na2CO3;
猜想3:Na2SO4、NaCl和____________ ;
猜想4:Na2SO4、NaCl、H2SO4和Na2CO3。
【交流讨论】小强同学认为猜想4一定是错误的,他的理由是______________ (用化学方程式表示)。
【进行实验】小明同学设计如下两个实验方案:
请写出方案二中有关反应的化学方程式:____________ 。

【查阅资料】Na2SO4溶液、NaCl溶液呈中性。
【提出猜想】猜想1:Na2SO4、NaCl;
猜想2:Na2SO4、NaCl和Na2CO3;
猜想3:Na2SO4、NaCl和
猜想4:Na2SO4、NaCl、H2SO4和Na2CO3。
【交流讨论】小强同学认为猜想4一定是错误的,他的理由是
【进行实验】小明同学设计如下两个实验方案:
| 实验步骤 | 实验现象 | 实验结论 | |
| 方案一 | 取少量烧杯中的溶液于洁净的试管中,加入几滴紫色石蕊溶液 | 猜想3正确 | |
| 方案二 | 取少量烧杯中的溶液于洁净的试管中,加入少量铁粉 |
请写出方案二中有关反应的化学方程式:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某“氧系茶垢清洁剂”外观为白色粉末,主要成分为过碳酸钠(2Na2CO3·3H2O2),能快速清洁茶具上附着的茶垢。某兴趣小组对该茶垢清洁剂展开探究。
资料:过碳酸钠具有Na2CO3与H2O2的双重性质,遇酸产生CO2,受热或遇水易分解;
【问题一】使用时,将产品倒入茶具中,加入60℃~70℃的热水,立即产生大量气泡。
探究该气泡成分:
提出猜想:猜想一:O2;猜想二:CO2;猜想三:……
实验验证:取少量该茶垢清洁剂于试管中,向其中加入适量60℃~70℃的热水,塞上带导管的橡皮塞,将生成的气体通入澄清石灰水,发现澄清石灰水_____ ;打开橡皮塞,向其中伸入_____ ,观察到预期的现象,证实猜想一正确。
(1)该实验中,H2O2产生O2的化学方程式为_____ 。
(2)该“氧系茶垢清洁剂”除了清除茶垢外,还可杀菌消毒。原理是使用过程中产生的活性氧具有很强的氧化性,可以使细菌、病毒中的蛋白质_____ 。
【问题二】同样的产品价格不同,可能是因为产品的纯度不同等。测定样品的纯度(过碳酸钠的含量):
方案一:测定CO2质量
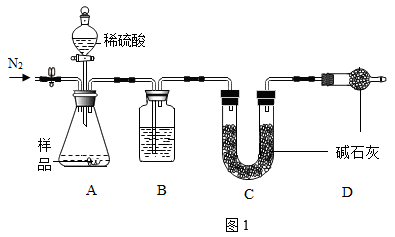
按图1取一定质量样品于锥形瓶中,向装置中通入一段时间N2,滴加足量稀硫酸。装置A中产生的气体经装置B干燥,进入装置C被吸收;反应结束后继续通入一段时间N2;称量装置C在反应前后的质量。(提示:碱石灰是NaOH和CaO的固体混合物)
(1)装置B中试剂的名称_____ 。
(2)装置D的作用_____ 。
(3)反应结束后继续通入N2的目的是_____ 。
方案二:测定O2的体积
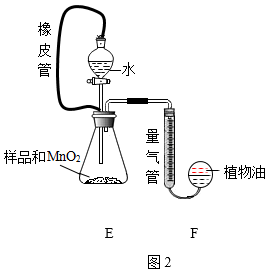
按图2取一定质量样品和MnO2于锥形瓶中,滴加适量水,利用装置F测定产生O2的体积。(提示:①读数时需等装置冷却至室温;②实验前后均需要调整量气管两边液面相平)
(1)从能量变化的角度考虑,H2O2在MnO2催化下分解的反应属于_____ 反应。
(2)若装置E中没有使用橡皮管,会导致测得的氧气体积偏大,原因是_____ ;本实验中,橡皮管还可以起到平衡压强,有利于液体顺利流下的作用。
方案三:测定沉淀质量
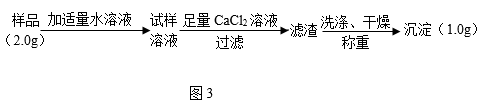
按图3将Na2CO3转化为CaCO3沉淀。
(1)加入“足量”CaCl2溶液的目的是_____ 。
(2)判断Na2CO3是否已完全转化为沉淀的方法_____ 。
(3)根据沉淀质量为1.0g,计算样品中Na2CO3的质量_____ g。
【总结提升】测定物质含量的一般方法如图4。
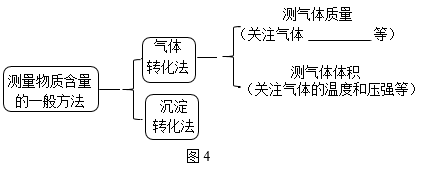
上述测量物质含量的方法中“测气体质量”时需关注的事项是_____ (答一条即可)。
资料:过碳酸钠具有Na2CO3与H2O2的双重性质,遇酸产生CO2,受热或遇水易分解;
【问题一】使用时,将产品倒入茶具中,加入60℃~70℃的热水,立即产生大量气泡。
探究该气泡成分:
提出猜想:猜想一:O2;猜想二:CO2;猜想三:……
实验验证:取少量该茶垢清洁剂于试管中,向其中加入适量60℃~70℃的热水,塞上带导管的橡皮塞,将生成的气体通入澄清石灰水,发现澄清石灰水
(1)该实验中,H2O2产生O2的化学方程式为
(2)该“氧系茶垢清洁剂”除了清除茶垢外,还可杀菌消毒。原理是使用过程中产生的活性氧具有很强的氧化性,可以使细菌、病毒中的蛋白质
【问题二】同样的产品价格不同,可能是因为产品的纯度不同等。测定样品的纯度(过碳酸钠的含量):
方案一:测定CO2质量
按图1取一定质量样品于锥形瓶中,向装置中通入一段时间N2,滴加足量稀硫酸。装置A中产生的气体经装置B干燥,进入装置C被吸收;反应结束后继续通入一段时间N2;称量装置C在反应前后的质量。(提示:碱石灰是NaOH和CaO的固体混合物)
(1)装置B中试剂的名称
(2)装置D的作用
(3)反应结束后继续通入N2的目的是


方案二:测定O2的体积
按图2取一定质量样品和MnO2于锥形瓶中,滴加适量水,利用装置F测定产生O2的体积。(提示:①读数时需等装置冷却至室温;②实验前后均需要调整量气管两边液面相平)
(1)从能量变化的角度考虑,H2O2在MnO2催化下分解的反应属于
(2)若装置E中没有使用橡皮管,会导致测得的氧气体积偏大,原因是
方案三:测定沉淀质量

按图3将Na2CO3转化为CaCO3沉淀。
(1)加入“足量”CaCl2溶液的目的是
(2)判断Na2CO3是否已完全转化为沉淀的方法
(3)根据沉淀质量为1.0g,计算样品中Na2CO3的质量
【总结提升】测定物质含量的一般方法如图4。

上述测量物质含量的方法中“测气体质量”时需关注的事项是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验。(提示:本实验所用汽油与KMnO4、碘均不发生化学反应)
【实验1】KMnO4晶体在不同溶剂中的溶解实验,根据实验步骤、实验操作图示填写相关实验现象。
【实验2】碘在不同溶剂中的溶解实验,根据实验操作图示回答相关问题。
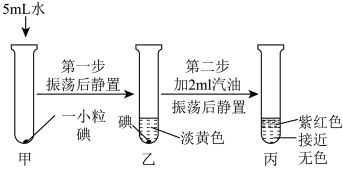
【实验结论】由上述实验可得出___________ 、___________ (写出两点)。
【反思与应用】(5)①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体___________ (填“分层”或“不分层”)。
②“从稀碘水中提取碘”是“海带提碘”工艺中的一个重要步骤,其原理类似【实验2】中第二步操作。工业上实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是___________ 。
【实验1】KMnO4晶体在不同溶剂中的溶解实验,根据实验步骤、实验操作图示填写相关实验现象。
| 实验步骤 | 实验操作图 | 实验操作及现象 |
| 步骤1 |  | 向A、B试管中分别加入5mL水和无色汽油,振荡后静置; (1)A试管中晶体全部溶解,溶液呈 |
| 步骤2 |  | (2)将步骤1中A试管内溶液倒入B试管中,振荡后静置;(2)B试管中观察到的现象为: |

【实验结论】由上述实验可得出
【反思与应用】(5)①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体
②“从稀碘水中提取碘”是“海带提碘”工艺中的一个重要步骤,其原理类似【实验2】中第二步操作。工业上实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组的同学在老师的带领下进行如下实验来探究和验证CO2的部分性质,请你一起参与探究:
实验一:探究CO2能否与水发生反应?
【设计实验】分别用石蕊溶液染成紫色的干燥纸花进行如下实验:
【分析讨论】实验④中紫花变红的原因是______ (用化学方程式表示)。
【实验结论】依据实验①~④的现象,可得出的结论是______ 。
实验二:验证CO2和NaOH溶液发生了反应。
【方案设计】
【反思交流】小明指出根据上述方案1中的实验现象不能得出CO2一定与NaOH发生了反应,其理由可能是______ 。
【拓展应用】对于无明显现象的化学反应,可通过检验某种反应物的消失或减少或验证______ 的方法来证明反应的发生。
实验一:探究CO2能否与水发生反应?
【设计实验】分别用石蕊溶液染成紫色的干燥纸花进行如下实验:
| 序号 | ① | ② | ③ | ④ |
| 实验示意图 | 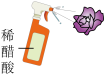 |  |  |  |
| 实验现象 | 紫花变红 | 紫花 | 紫花不变色 | 紫花变红 |
【实验结论】依据实验①~④的现象,可得出的结论是
实验二:验证CO2和NaOH溶液发生了反应。
【方案设计】
| 实验步骤和方法 | 实验现象 | 实验结论 | |
| 方案1 | 向充满CO2气体的软质塑料瓶中加入少量NaOH溶液,盖紧瓶盖,上下振动软质塑料瓶 | 塑料瓶变瘪 | CO2和NaOH溶液发生反应 |
| 方案2 | 向充满CO2气体的集气瓶中倒入适量的NaOH溶液,振荡,再向其中加入适量的CaCl2溶液 | 产生 |
【拓展应用】对于无明显现象的化学反应,可通过检验某种反应物的消失或减少或验证
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小佳同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体。但她在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体。
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小佳查阅资料,记录了下列几种物质的颜色:
其他同学认为不必查阅氯化镁的颜色,理由_____ ;
【提出猜想】分析资料,小佳认为淡黄色固体可能是由镁与空气中的_____ 反应生成的;
【实验探究】佳设计实验证实了自己的猜想,她的方案可能是:将点燃的镁条伸入充满_____ 的集气瓶中,观察是否生成_____ 色固体。
【实验结论】根据小佳的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式_____ 、_____ 。
【反思与评价】通过上述实验,你对燃烧有什么新的认识?_____ 。
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小佳查阅资料,记录了下列几种物质的颜色:
| 物质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜色 | 白色 | 白色 | 浅黄色 | 白色 | 白色 | 白色 |
其他同学认为不必查阅氯化镁的颜色,理由
【提出猜想】分析资料,小佳认为淡黄色固体可能是由镁与空气中的
【实验探究】佳设计实验证实了自己的猜想,她的方案可能是:将点燃的镁条伸入充满
【实验结论】根据小佳的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式
【反思与评价】通过上述实验,你对燃烧有什么新的认识?
您最近一年使用:0次



