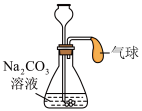
如图,向两个相同容积的锥形瓶中分别注入等体积的蒸馏水和NaOH溶液,用压强传感器测得瓶中气体压强变化的曲线如图所示。
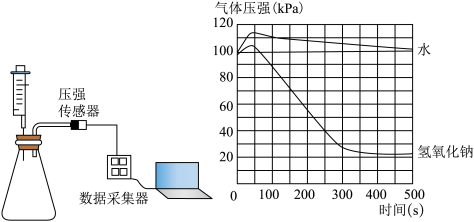
(1)结合曲线说明CO2确实与NaOH发生了反应,而不是溶解在NaOH溶液中______ 。
(2)等到锥形瓶中气压不再改变时,测得注入水的锥形瓶中的气压与0s时的气压相同,说明在该条件下1体积的水最多能溶解______ 体积的二氧化碳。
(3)实验结束后,请设计实验证明注入NaOH溶液锥形瓶的溶质中还含有NaOH______ 。(写出操作、现象和结论)

(1)结合曲线说明CO2确实与NaOH发生了反应,而不是溶解在NaOH溶液中
(2)等到锥形瓶中气压不再改变时,测得注入水的锥形瓶中的气压与0s时的气压相同,说明在该条件下1体积的水最多能溶解
(3)实验结束后,请设计实验证明注入NaOH溶液锥形瓶的溶质中还含有NaOH
更新时间:2021-04-08 14:18:37
|
相似题推荐
【推荐1】某化学兴趣小组设计了一组“吹气球”实验,三套装置如图:

(1)甲装置:
①仪器a的名称为________________________ ;
②向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性__________ ;
(2)乙装置:
①若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是__________ ;
②若生成H2使气球胀大,则反应的化学方程式为___________ ;
③若锥形瓶中装有NaOH固体,分液漏斗中加入少量水,则气球胀大的主要原因是___________ ;
(3)丙装置:
若锥形瓶中盛满CO2,欲使气球胀大,则分液漏斗中的液体可以是__________ ,锥形瓶中发生反应的化学方程式是___________ 。

(1)甲装置:
①仪器a的名称为
②向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性
(2)乙装置:
①若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是
②若生成H2使气球胀大,则反应的化学方程式为
③若锥形瓶中装有NaOH固体,分液漏斗中加入少量水,则气球胀大的主要原因是
(3)丙装置:
若锥形瓶中盛满CO2,欲使气球胀大,则分液漏斗中的液体可以是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】二氧化碳是种温室气体。某化学兴趣小组利用如图所示装置对二氧化碳的性质进行验证:
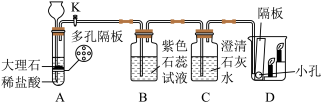
当打开K,反应一段时间后:
①D烧杯中_____ (填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的物理性质是_____ ,具有的化学性质是_____ 。上述结论可以推断二氧化碳的重要用途之一是_____ 。
②B处紫色石蕊试液变成红色。C处澄清石灰水变浑浊。B处使紫色石蕊溶液变红的物质是_____ ;写出C处发生变化的化学方程式_____ 。

当打开K,反应一段时间后:
①D烧杯中
②B处紫色石蕊试液变成红色。C处澄清石灰水变浑浊。B处使紫色石蕊溶液变红的物质是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐3】根据下列实验装置图,回答下列有关问题:
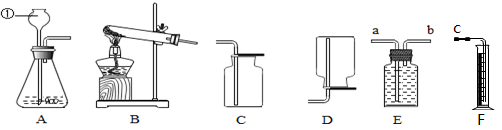
(1)图中标有①的仪器名称是______ 。
(2)如果用A装置制取二氧化碳,检查气密性后在锥形瓶内加入的物质是_____ ,写出用A装置制取二氧化碳的化学方程式:____ 。
(3)用KClO3和MnO2制取O2,可选用发生装置____ (填字母),用排水法收集并测量产生O2的体积,则应该让____ 导管与c连接。所测定的O2体积比理论计算值小,可能的原因是_____ (填序号)。
①部分氧气溶于水 ②集气瓶中有空气 ③氯酸钾未完全分解
(4)实验室常用氯化铵固体与熟石灰共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。
①制取氨气反应的化学方程式:_______ 。
②NH3的收集装置选择_____ ,检验氨气是否收集满可以使用______ 试纸。
③干燥氨气可以选用下列干燥剂中的_____ (填字母)。
a.固体氢氧化钠 b.浓硫酸 c.生石灰
(5)用实验证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳也能发生反应。如图所示进行实验(装置气密性良好,实验前活塞和弹簧夹K处于关闭状态)。
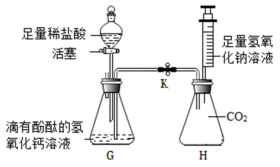
实验一:证明氢氧化钙溶液与稀盐酸发生反应
打开分液漏斗的活塞,使稀盐酸逐滴滴加入G锥形瓶中,观察到_______ 的现象时,关活塞,证明氢氧化钙溶液与稀盐酸发生反应。
实验二:证明氢氧化钠与二氧化碳反应
将注射器中的氢氧化钠溶液推入H锥形瓶中,过一段时间后,打开弹簧夹K,观察到_____ 的现象并且溶液呈红色,证明氢氧化钠溶液与二氧化碳确实发生了反应。请写出二氧化碳与氢氧化钠溶液反应的化学方程式是______ 。锥形瓶H中溶液最后呈红色______ (填“能”或“不能”)证明氢氧化钠有剩余。

(1)图中标有①的仪器名称是
(2)如果用A装置制取二氧化碳,检查气密性后在锥形瓶内加入的物质是
(3)用KClO3和MnO2制取O2,可选用发生装置
①部分氧气溶于水 ②集气瓶中有空气 ③氯酸钾未完全分解
(4)实验室常用氯化铵固体与熟石灰共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。
①制取氨气反应的化学方程式:
②NH3的收集装置选择
③干燥氨气可以选用下列干燥剂中的
a.固体氢氧化钠 b.浓硫酸 c.生石灰
(5)用实验证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳也能发生反应。如图所示进行实验(装置气密性良好,实验前活塞和弹簧夹K处于关闭状态)。

实验一:证明氢氧化钙溶液与稀盐酸发生反应
打开分液漏斗的活塞,使稀盐酸逐滴滴加入G锥形瓶中,观察到
实验二:证明氢氧化钠与二氧化碳反应
将注射器中的氢氧化钠溶液推入H锥形瓶中,过一段时间后,打开弹簧夹K,观察到
您最近一年使用:0次
【推荐1】化学是一门以实验为基础的科学。根据下列图示回答问题。

(1)写出序号②仪器的名称:_______ 。
(2)若从图中选择A装置制取氧气,反应的化学方程式为_______ 。
(3)实验室若要制取较纯净而干燥的二氧化碳还应添加图中F和G装置,气体经过两装置导管口的正确连接顺序是:a→___ →____ →____ →____ →集气装置(在括号内用导管口字母填写),其中G装置发生反应的化学方程式为_______ 。
(4)实验室用固体氯化铵和碱石灰共热制取氦气(NH3),发生装置应选____ ,收集氨气仅能选择上图中的E装置,是因为氨气具有_______ 物理性质,但用该法收集氨气存在的不足之处是___ 。

(1)写出序号②仪器的名称:
(2)若从图中选择A装置制取氧气,反应的化学方程式为
(3)实验室若要制取较纯净而干燥的二氧化碳还应添加图中F和G装置,气体经过两装置导管口的正确连接顺序是:a→
(4)实验室用固体氯化铵和碱石灰共热制取氦气(NH3),发生装置应选
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】家庭生活中食品制作(如面条、馒头等)经常用到食用碱,食用碱的主要成分是碳酸钠,可能含有少量氯化钠。小莉将家中食用碱带到实验室进行探究,请设计实验验证小莉提供的食用碱样品是否含有氯化钠。
| 实验步骤 | 实验现象 | 结论与解释 |
| 1取一定量的食用碱样品放入试管,加入蒸馏水、振荡 | 样品溶解 | 食用碱溶于水 |
| 2向食用碱溶液的试管中,滴加几滴 | ||
| 3 |
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】如图是实验室常用的部分实验装置图,请按要求回答问题。
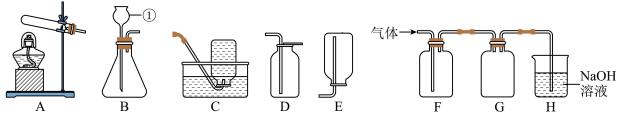
(1)写出仪器①的名称______ 。
(2)实验室用加热高锰酸钾的方法制取较纯净的氧气,所选择的发生装置和收集装置是______ (填字母序号),写出该反应的化学方程式______ 。
(3)SO2是一种有刺激性气味的气体,能溶于水,且与水反应。实验室可用Na2SO3固体和浓硫酸反应制得,发生装置可以选择______ ;某同学用如图F、G、H组合收集SO2,F装置用于收集SO2,G装置的作用是______ ,H装置的作用是防止空气污染。

(1)写出仪器①的名称
(2)实验室用加热高锰酸钾的方法制取较纯净的氧气,所选择的发生装置和收集装置是
(3)SO2是一种有刺激性气味的气体,能溶于水,且与水反应。实验室可用Na2SO3固体和浓硫酸反应制得,发生装置可以选择
您最近一年使用:0次
【推荐2】用如图所示装置可以制备初中常见的气体。并进行相关性质的实验。请回答下列问题:

(1)①装置中仪器a的名称为______ 。
②图一中,装置B中蜡烛熄灭,同时装置C中溶液变浑浊,则装置A中化学反应方程式为______ 。从图二中选择收集A产生的气体,可选择的装置有______ (填字母)。
③装置A中小试管的作用是______ 。(填字母)
a.打开或关闭K时,可以使装置A中的反应随时发生或停止
b.形成液封,防止装置A中产生的气体从长颈漏斗逸出,且节约药品
(2)现要配制7.5%NaCl溶液100.0g,按图三操作顺序进行(注意:1g以下用游码)。请回答:
①计算:需要氯化钠质量______ g。
②称量:调节平衡后,分别在天平左右两盘放上纸片,应先放______ (填写“砝码”或“药品”),用托盘天平称量所需的氯化钠时。发现托盘天平的指针偏向左盘,应______ 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体
③溶解:玻璃棒的作用是______ 。
④反思:下列操作不会引起溶液中氯化钠的质量分数偏小的是______ (填字母)。
A.把氯化钠放在右边托盘上进行称量
B.配制溶液时,烧杯先用少量蒸馏水润洗
C.氯化钠晶体不纯
D.转移已配好的溶液时,有少量溶液溅出

(1)①装置中仪器a的名称为
②图一中,装置B中蜡烛熄灭,同时装置C中溶液变浑浊,则装置A中化学反应方程式为
③装置A中小试管的作用是
a.打开或关闭K时,可以使装置A中的反应随时发生或停止
b.形成液封,防止装置A中产生的气体从长颈漏斗逸出,且节约药品
(2)现要配制7.5%NaCl溶液100.0g,按图三操作顺序进行(注意:1g以下用游码)。请回答:
①计算:需要氯化钠质量
②称量:调节平衡后,分别在天平左右两盘放上纸片,应先放
A.增加适量氯化钠固体 B.减少适量氯化钠固体
③溶解:玻璃棒的作用是
④反思:下列操作不会引起溶液中氯化钠的质量分数偏小的是
A.把氯化钠放在右边托盘上进行称量
B.配制溶液时,烧杯先用少量蒸馏水润洗
C.氯化钠晶体不纯
D.转移已配好的溶液时,有少量溶液溅出
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组用氯酸钾和二氧化锰制取氧气。可能用到实验装置如图所示:

请回答下列问题:
(1)a仪器的名称________ 。
(2)写出用该方法制取氧气的化学方程式________ ,其中二氧化锰的作用是________ ,制取并收集干燥的氧气应选用________ (填实验装置图字母序号)。
(3)氯酸钾完全分解后,为了回收二氧化锰和氯化钾,又进行了如下实验操作:

实验操作中,加入足量的水的目的是________ ;实验操作②应选择上述图中的________ (填实验装置图字母序号)。
(4)实验结束后,同学们在拆卸装置时闻到刺激性气味。他们将回收得到的MnO2称量,发现其质量小于加热前MnO2的质量。查阅资料后发现。加热KC1O3和MnO2混合物的反应过程如下:
第一步:
第二步:
第三步:
拆卸装置时闻到刺激性气味的气体是________ ,根据以上信息写出加热后剩余固体中MnO2质量小于加热前MnO2质量的原因________ 。

请回答下列问题:
(1)a仪器的名称
(2)写出用该方法制取氧气的化学方程式
(3)氯酸钾完全分解后,为了回收二氧化锰和氯化钾,又进行了如下实验操作:

实验操作中,加入足量的水的目的是
(4)实验结束后,同学们在拆卸装置时闻到刺激性气味。他们将回收得到的MnO2称量,发现其质量小于加热前MnO2的质量。查阅资料后发现。加热KC1O3和MnO2混合物的反应过程如下:
第一步:

第二步:

第三步:

拆卸装置时闻到刺激性气味的气体是
您最近一年使用:0次