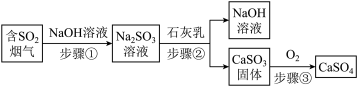
高纯碳酸钙广泛应用于医药、生活、生产中,工业上用石灰石(杂质SiO2不溶于水且不与酸反应)制备高纯碳酸钙工艺流程图如下:
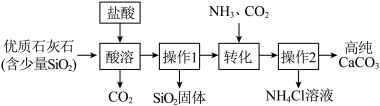
(1)“酸溶”过程中反应的化学方程式为_____ 。
(2)生产过程中可循环利用的物质是_____ 。
(3)“操作1”和“操作2”是常见的分离混合物的方法。其操作名称是_____ 。

(1)“酸溶”过程中反应的化学方程式为
(2)生产过程中可循环利用的物质是
(3)“操作1”和“操作2”是常见的分离混合物的方法。其操作名称是
更新时间:2021-02-08 11:02:20
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】氧化锌软膏可用于急性或亚急性皮炎、湿疹、痱子及轻度、小面积的皮肤溃疡。闪锌矿(主要成分是ZnS,含有少量CuS)是含锌的主要矿物质之一,高温煅烧闪锌矿生成氧化锌、氧化铜和SO2,以氧化锌粗品为原料制备纯氧化锌的生产工艺流程如下:
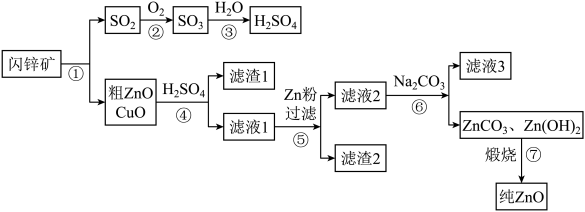
(I)步骤③中发生反应的化学方程式为_________ 。
(II)从除杂原理分析,滤渣2含有的金属有_______ 种.
(Ⅲ)步骤⑥的操作是______ (填操作名称);步骤_______ 发生的反应属于分解反应.
(IV)步骤④中ZnO发生反应的化学方程式为________ 。

(I)步骤③中发生反应的化学方程式为
(II)从除杂原理分析,滤渣2含有的金属有
(Ⅲ)步骤⑥的操作是
(IV)步骤④中ZnO发生反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】构建知识网络,可以帮助我们理解知识间的内在联系。如图是盐酸与不同类别物质之间反应的知识网络。
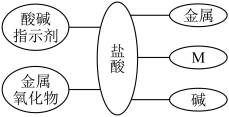
(1)实验室常用石灰石与稀盐酸反应制取 CO2,写出方程式______ 。
(2)写出金属铁与盐酸反应的化学方程式:______ 。
(3)用盐酸除铁锈(主要成分 Fe2O3)的化学方程式是______ 。
(4)学完“酸的化学性质”后,小林邀请你与他一起讨论:醋酸也是一种酸,和盐酸具有相似的化学性质,下列关于醋酸化学性质的说法正确的是______(填字母序号)。
(5)反思:盐酸、硫酸、食醋具有相似化学性质的原因是它们水溶液中都含有______ 。由于不同种类的酸______ 不同,所以性质也存在差异。

(1)实验室常用石灰石与稀盐酸反应制取 CO2,写出方程式
(2)写出金属铁与盐酸反应的化学方程式:
(3)用盐酸除铁锈(主要成分 Fe2O3)的化学方程式是
(4)学完“酸的化学性质”后,小林邀请你与他一起讨论:醋酸也是一种酸,和盐酸具有相似的化学性质,下列关于醋酸化学性质的说法正确的是______(填字母序号)。
| A.能使无色酚酞溶液变红色 |
| B.能与氢氧化钠溶液发生反应 |
| C.能与活泼金属发生反应 |
(5)反思:盐酸、硫酸、食醋具有相似化学性质的原因是它们水溶液中都含有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】青岛是一座临海城市,海洋资源丰富。化学兴趣小组模拟化工厂生产流程,利用海水获取化学资源,部分设计方案如下图所示。请回答问题。
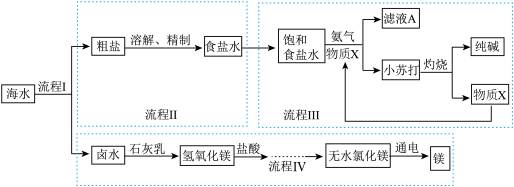
【流程I】海水“晒盐”
(1)观察下图,海水中含量最多的盐是______ (填化学式)。20℃时,氯化钠的溶解度为______ ,根据氯化钠的溶解度随温度变化情况,可得出从海水中获得粗盐的方法是______ 。
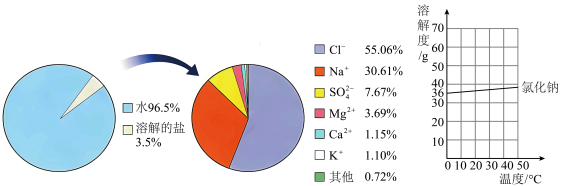
【流程II】粗盐精制
(2)由图可知,粗盐中通常含有泥沙等难溶性杂质和 、
、 和
和 等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解,并依次加入下列试剂:过量的
等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解,并依次加入下列试剂:过量的______ 溶液→过量的氢氧化钠溶液→过量的______ 溶液→适量稀盐酸。加入稀盐酸之前应进行的操作是______ 。
【流程III】海水“制碱”
(3)可循环利用的物质X是______ ,小苏打灼烧过程发生反应的基本反应类型是______ 。
【流程IV】海水提镁
(4)海水提镁过程中,发生的复分解反应的化学方程式为______ (写一个)。

【流程I】海水“晒盐”
(1)观察下图,海水中含量最多的盐是

【流程II】粗盐精制
(2)由图可知,粗盐中通常含有泥沙等难溶性杂质和
 、
、 和
和 等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解,并依次加入下列试剂:过量的
等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解,并依次加入下列试剂:过量的【流程III】海水“制碱”
(3)可循环利用的物质X是
【流程IV】海水提镁
(4)海水提镁过程中,发生的复分解反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】工业生产化工原料纯碱和化肥氯化铵的工艺流程示意图如图:

[生产原理]反应②:NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl
[问题讨论]
(1)操作I、Ⅱ的名称为_______ ;气体D的化学式为_______ 。
(2)反应①中发生了两个反应,写出其中发生中和反应的化学方程式:_______ 。
(3)反应③生成纯碱时,还生成另外两种氧化物,则该反应的化学方程式为_______ 。
(4)上述工艺流程中循环利用二氧化碳的目的是_______ 。
(5)通过操作Ⅱ得到的晶体A因缺少洗涤操作导致晶体不纯,能证明晶体A中含有某些杂质的正确操作方法是(填字母序号)。

[生产原理]反应②:NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl
[问题讨论]
(1)操作I、Ⅱ的名称为
(2)反应①中发生了两个反应,写出其中发生中和反应的化学方程式:
(3)反应③生成纯碱时,还生成另外两种氧化物,则该反应的化学方程式为
(4)上述工艺流程中循环利用二氧化碳的目的是
(5)通过操作Ⅱ得到的晶体A因缺少洗涤操作导致晶体不纯,能证明晶体A中含有某些杂质的正确操作方法是(填字母序号)。
| A.取少量晶体A于试管中,滴加稀盐酸 |
| B.取少量晶体A于研钵中,加熟石灰研磨 |
| C.取少量晶体A于试管中,加水溶解,滴加氯化钙溶液 |
| D.取少量晶体A于试管中,加水溶解,先滴加足量的稀硝酸,再滴加硝酸银溶液 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】请用化学用语回答生活中的下列问题。
(1)新鲜的苹果切开后因亚铁离子被氧化会很快变黄,亚铁离子的符号是______ 。
(2)工业盐因含亚硝酸钠(NaNO2)而有毒,标出亚硝酸钠中氮元素的化合价______ 。
(3)小苏打既可作发酵粉又可治疗胃酸,写出小苏打的化学式_____ 。
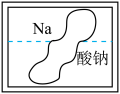
(4)某学习小组在帮助清理药品时,发现一瓶标签残缺盛有无色溶液(初中化学常用试剂)的试剂瓶(如图),你猜想这种试剂可能是____ 溶液。
(1)新鲜的苹果切开后因亚铁离子被氧化会很快变黄,亚铁离子的符号是
(2)工业盐因含亚硝酸钠(NaNO2)而有毒,标出亚硝酸钠中氮元素的化合价
(3)小苏打既可作发酵粉又可治疗胃酸,写出小苏打的化学式

(4)某学习小组在帮助清理药品时,发现一瓶标签残缺盛有无色溶液(初中化学常用试剂)的试剂瓶(如图),你猜想这种试剂可能是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】江西萍乡的安源煤和矿曾被誉为“江南煤都”,以下是某实验室设计的以煤为原料制备尿素的工艺流程图。
【查阅资料】氧化钙在高温下能与二氧化碳反应生成碳酸钙。

(1)气化室中煤(主要含碳元素)与水蒸气生成氢气和一种用于灭火的气体,写出此反应方程式___________ 。
(2)流程中,要将石灰石进行粉碎的目的___________ 。
(3)煅烧炉中石灰石发生反应的化学方程式是___________ 。
(4)整个流程中能循环利用的物质是___________ (写化学式)。
【查阅资料】氧化钙在高温下能与二氧化碳反应生成碳酸钙。

(1)气化室中煤(主要含碳元素)与水蒸气生成氢气和一种用于灭火的气体,写出此反应方程式
(2)流程中,要将石灰石进行粉碎的目的
(3)煅烧炉中石灰石发生反应的化学方程式是
(4)整个流程中能循环利用的物质是
您最近一年使用:0次
【推荐1】请回答下列问题。
(一)我国是茶文化的发源地。唐代陆羽《茶经》中记载:“风炉以铜铁铸之……底一窗以为通飚漏烬之所……风能兴火,火能熟水。”“漉水囊……其格以生铜铸之。”

(1)“风炉”属于_____ (填“纯净物”或“混合物”)。
(2)“飚”(即风)提供燃烧所需的_____ 。
(3)“火能熟水”说明燃烧_____ (填“吸收”或“放出”)热量。
(4)“漉水囊”可将茶叶与茶水分离,类似于基本实验操作中的_____ 。
(5)茶香四溢,从分子角度解释其原因是______ 。
(二)地球是一个美丽的“水球”,表面约71%被水覆盖,淡水仅占总水量的2.5%;其余是海水或咸水。海水淡化是解决人类淡水资源短缺的有效措施。全球海水淡化水用途如图1所示。海水淡化技术主要有热分离法和膜分离法,热分离法利用蒸发和冷凝分离水与非挥发性物质,能耗大、成本高;膜分离法利用薄膜的选择透过性实现海水淡化,但现有薄膜的水通量低,应用受到限制。有科学家提出,给石墨烯“打上”许多特定大小的孔,制成单层纳米孔二维薄膜,可进行海水淡化。石墨烯海水淡化膜工作原理如图2所示。

依据上文,回答下列问题。
(6)全球海水淡化水用途排在首位的是_____ 。
(7)热分离法中,水发生了_____ (填“物理变化”或“化学变化”)。限制热分离法大规模应用的原因是_____ 。
(8)石墨烯海水淡化膜允许_____ 通过。
(9)石墨烯、金刚石和C60均属于碳单质(由同种元素组成的纯净物称为单质),下列说法正确的是 (填字母)。
(10)提出爱护水资源的一条建议_________ 。
(一)我国是茶文化的发源地。唐代陆羽《茶经》中记载:“风炉以铜铁铸之……底一窗以为通飚漏烬之所……风能兴火,火能熟水。”“漉水囊……其格以生铜铸之。”

(1)“风炉”属于
(2)“飚”(即风)提供燃烧所需的
(3)“火能熟水”说明燃烧
(4)“漉水囊”可将茶叶与茶水分离,类似于基本实验操作中的
(5)茶香四溢,从分子角度解释其原因是
(二)地球是一个美丽的“水球”,表面约71%被水覆盖,淡水仅占总水量的2.5%;其余是海水或咸水。海水淡化是解决人类淡水资源短缺的有效措施。全球海水淡化水用途如图1所示。海水淡化技术主要有热分离法和膜分离法,热分离法利用蒸发和冷凝分离水与非挥发性物质,能耗大、成本高;膜分离法利用薄膜的选择透过性实现海水淡化,但现有薄膜的水通量低,应用受到限制。有科学家提出,给石墨烯“打上”许多特定大小的孔,制成单层纳米孔二维薄膜,可进行海水淡化。石墨烯海水淡化膜工作原理如图2所示。

依据上文,回答下列问题。
(6)全球海水淡化水用途排在首位的是
(7)热分离法中,水发生了
(8)石墨烯海水淡化膜允许
(9)石墨烯、金刚石和C60均属于碳单质(由同种元素组成的纯净物称为单质),下列说法正确的是 (填字母)。
| A.都由碳元素组成 | B.都由碳原子构成 |
| C.物理性质相似 | D.都由分子构成 |
(10)提出爱护水资源的一条建议
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】化学来源于生活,生活中处处离不开化学。
I.水是生命之源,是人类宝贵的自然资源,“生命吸管”可直接将污水净化为饮用水,主要处理步骤与自来水的生产过程相似,如图2所示:(③中离子交换树脂的主要作用是去除重金属离面子、软化水质)
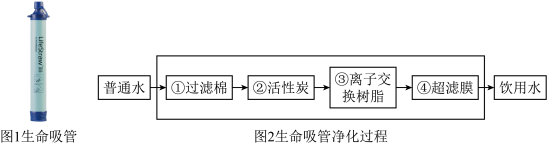
(1)②中活性炭的作用是_______ 。
(2)①中过滤棉的作用是_______ (填字母,下同),推测④中超滤膜的作用是_______ 。
a.去除有害菌和部分病毒 b.除去较大的不溶性杂质
(3)若无生命吸管,取用河水时,证明河水是硬水的方法_______ (写出操作方法、现象和结论),要降低河水的硬度和杀灭病原微生物,生活中常用_______ 的方法;欲使净化的水为纯水,则可采取的方法是_______ 。
II.富含淀粉的谷物、甘薯等可以酿酒。在酿酒过程中淀粉在酶的作用下转化为葡萄糖,葡萄糖发酵为酒精,香甜的酒酿就是利用该原理,用酒曲酶(俗称酒药)制作的。家庭一般制作酒酸的简单流程图如下:

(4)装入陶罐需密封,主要是防止空气中的_______ (填名称)进入。如保存不当,易导致乳酸量过多而味偏酸,乳酸的化学式为C3H6O3,则乳酸的相对分子质量为_______ 。
I.水是生命之源,是人类宝贵的自然资源,“生命吸管”可直接将污水净化为饮用水,主要处理步骤与自来水的生产过程相似,如图2所示:(③中离子交换树脂的主要作用是去除重金属离面子、软化水质)

(1)②中活性炭的作用是
(2)①中过滤棉的作用是
a.去除有害菌和部分病毒 b.除去较大的不溶性杂质
(3)若无生命吸管,取用河水时,证明河水是硬水的方法
II.富含淀粉的谷物、甘薯等可以酿酒。在酿酒过程中淀粉在酶的作用下转化为葡萄糖,葡萄糖发酵为酒精,香甜的酒酿就是利用该原理,用酒曲酶(俗称酒药)制作的。家庭一般制作酒酸的简单流程图如下:

(4)装入陶罐需密封,主要是防止空气中的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】侯德榜是我国著名的化学家,为纯碱和氮肥工业技术的发展作出了杰出的贡献,他发明的侯氏制碱法大大提高了原料的利用率,其工业流程大致如图:

(1)上述流程中,用到的原料有空气、焦炭、水、二氧化碳以及_____ 。
(2)若上述流程中,“一种氮肥”指的是一种铵态氮肥,则其化学式是_____ 。
(3)上述流程中,为了节约成本,可循环利用的物质是_______ 。

(1)上述流程中,用到的原料有空气、焦炭、水、二氧化碳以及
(2)若上述流程中,“一种氮肥”指的是一种铵态氮肥,则其化学式是
(3)上述流程中,为了节约成本,可循环利用的物质是
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐2】保障粮食安全是中国的永恒课题,阅读下面的科普短文并回答问题。
土豆是继水稻、小麦、玉米之后的第四大粮食作物,含淀粉、蛋白质、维生素C 等多种营养物质,是餐桌上的美味食材。表为鲜土豆中主要营养物质的含量(每100g)
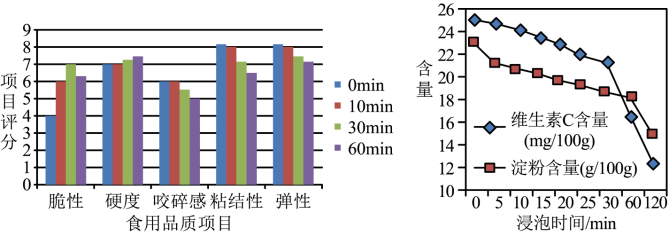
土豆切开后发生褐变,用水浸泡能防止褐变,但会引起营养物质流失。用土豆片进行实验, 测得其食用品质、淀粉含量和维生素C含量随浸泡时间的变化如下:土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒,就算是把变绿、发芽的部位削掉,也不宜食用。除食用外,土豆还可以作为原料广泛用于医药、化工、纺织、造纸等工业中。(原文作者宋国安、杨铭铎等,有删改)
(1)表中的“钙”指的是_____ (填“元素”或“原子”) ,人体每日必须摄入一定量的钙,幼儿及青少年摄入不足会患____ 和发育不良。
(2)由图可知:60min 内,_____ (填序号,下同)。
A 浸泡30min 比10min 脆性分值高
B 浸泡10min,硬度、咬碎感均无明显变化
C 随着浸泡时间的增加,粘结性、弹性分值均降低
(3)由图可知:土豆片的淀粉含量与浸泡时间的关系是_____ ,此图中维生素C含量与淀粉含量变化的快慢不同,可能原因是_________ 。
(4)下列说法正确的是_____ 。
A 土豆开发应用的前景广阔
B 土豆中维生素C 含量最高
C 用水泡可防止土豆片褐变
D 变绿、发芽的土豆把变色部位削掉后就能食用
土豆是继水稻、小麦、玉米之后的第四大粮食作物,含淀粉、蛋白质、维生素C 等多种营养物质,是餐桌上的美味食材。表为鲜土豆中主要营养物质的含量(每100g)
| 蛋白质/g | 脂肪/g | 淀粉/g | 钙/mg | 磷/mg | 维生素C/mg |
| 1.5-2.3 | 0.4-0.94 | 17.5-28.0 | 11-60 | 15-68 | 20-40 |
土豆切开后发生褐变,用水浸泡能防止褐变,但会引起营养物质流失。用土豆片进行实验, 测得其食用品质、淀粉含量和维生素C含量随浸泡时间的变化如下:土豆变绿、发芽时,龙葵素含量显著增高,而龙葵素多食可导致中毒,就算是把变绿、发芽的部位削掉,也不宜食用。除食用外,土豆还可以作为原料广泛用于医药、化工、纺织、造纸等工业中。(原文作者宋国安、杨铭铎等,有删改)

(1)表中的“钙”指的是
(2)由图可知:60min 内,
A 浸泡30min 比10min 脆性分值高
B 浸泡10min,硬度、咬碎感均无明显变化
C 随着浸泡时间的增加,粘结性、弹性分值均降低
(3)由图可知:土豆片的淀粉含量与浸泡时间的关系是
(4)下列说法正确的是
A 土豆开发应用的前景广阔
B 土豆中维生素C 含量最高
C 用水泡可防止土豆片褐变
D 变绿、发芽的土豆把变色部位削掉后就能食用
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】钇是人类1794年发现的第一种稀土金属元素,在工业中用途很广。稀土金属钇的氧化物(Y203)广 泛应用于航空航天涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含Y203约70%,含Fe203、Cu0、 Si02等约30%)生产大颗粒氧化钇的一种工艺如下:
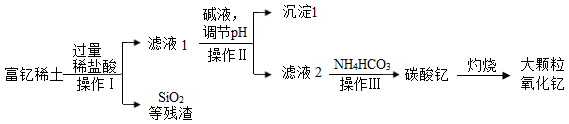
(1)操作I的名称为________ ,进行该操作时常使用到的玻璃容器有烧杯、玻璃棒、______ 。
(2)加稀盐酸的过程中,氧化钇与盐酸反应的化学方程式是_______ ,该反应的基本类型是_________ 。
(3)滤液1中含有的盐类物质有______________ 。(填化学式)
(4)已知一些氢氧化物沉淀的pH范围如下表:
调节pH时最先得到的沉淀是___________ ,调节pH的最佳值应是_______ 。
(5)碳酸钇灼烧分解的化学方程式是_______________ 。

(1)操作I的名称为
(2)加稀盐酸的过程中,氧化钇与盐酸反应的化学方程式是
(3)滤液1中含有的盐类物质有
(4)已知一些氢氧化物沉淀的pH范围如下表:
氢氧化物 | 开始沉淀和完全沉淀的pH |
Fe(OH)3 | 1.1~3.0 |
Cu(OH)2 | 4.2~6.7 |
Y(OH)3 | 6.0~8.2 |
(5)碳酸钇灼烧分解的化学方程式是
您最近一年使用:0次