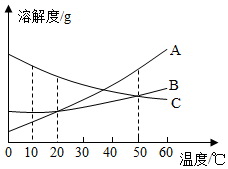
如图是a、b、c三种固体物质(均不含结晶水)的溶解度曲线图。请根据图示回答下列问题:
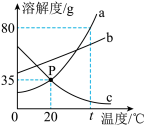
(1)20℃时,a、b、c三种固体物溶解度由大到小是___________ 。
(2)20℃时,向30g物质a中加入50g水,充分溶解并恢复到原温度,所得溶液的质量为___________ g。
(3)下列说法正确的是___________ 。
A 当a中混有少量b时,可用蒸发结晶的方法提纯a
B 20℃时,用a、b、c三种固体配制等质量的饱和溶液,所需水的质量大小关系是b>a=c
C 将20℃的a、b、c三种物质的饱和溶液升温至t℃,所得溶液中溶质的质量分数大小关系为b>a>c
D 把t℃a、b、c三种物质的饱和溶液降温至20℃时,析出晶体最多的是a

(1)20℃时,a、b、c三种固体物溶解度由大到小是
(2)20℃时,向30g物质a中加入50g水,充分溶解并恢复到原温度,所得溶液的质量为
(3)下列说法正确的是
A 当a中混有少量b时,可用蒸发结晶的方法提纯a
B 20℃时,用a、b、c三种固体配制等质量的饱和溶液,所需水的质量大小关系是b>a=c
C 将20℃的a、b、c三种物质的饱和溶液升温至t℃,所得溶液中溶质的质量分数大小关系为b>a>c
D 把t℃a、b、c三种物质的饱和溶液降温至20℃时,析出晶体最多的是a
更新时间:2021-05-14 21:57:13
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】“夏天晒盐,冬天捞碱”。下表是NaCl和Na2CO3在不同温度下的溶解度,请回答下列问题。
(1)20℃时,Na2CO3的溶解度是___________ g。
(2)20℃时,将8gNaCl加入到42g水中充分分解后所得液的质量分数是___________ ,若要将该溶液稀释到10%,需加水___________ g。
(3)我国很多的盐碱湖中有NaCl和Na2CO3,“夏天晒盐”是人们用___________ (填“蒸发结晶”或“降温结晶”)的方法获得粗盐,分析表中数据,说明冬天能“捞碱”的原因___________ 。
| 温度(℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度(g) | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 | 53.2 | |
(2)20℃时,将8gNaCl加入到42g水中充分分解后所得液的质量分数是
(3)我国很多的盐碱湖中有NaCl和Na2CO3,“夏天晒盐”是人们用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】甲、乙、丙三种物质的溶解度曲线如图所示。据图回答:
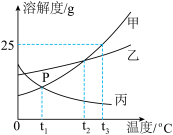
(1)P点的含义是____________________ 。
(2)t3℃时,将25g甲物质放入50g水中,充分溶解后,该溶液中溶质的质量分数为_______ 。
(3)乙物质中含有少量的甲物质,要提纯乙物质,通常采用的方法是________________ 。

(1)P点的含义是
(2)t3℃时,将25g甲物质放入50g水中,充分溶解后,该溶液中溶质的质量分数为
(3)乙物质中含有少量的甲物质,要提纯乙物质,通常采用的方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐1】下表是氢氧化钠和氢氧化钙的溶解度数据
(1)为测定X的值,取四份60℃的水各50g,分别进行实验,并记录数据如下:
实验结果分析,可知X的值为_____
(2)去除NaOH溶液中的Ca(OH)2,通过蒸发浓缩、_____ ,然后过滤、洗涤、干燥得到NaOH固体
(3)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复到20℃得到的溶液(乙溶液),此时溶液的溶质质量分数乙_____ 甲(填>、<、=).
(4)在20℃时,向盛有100g水的烧杯中加入111gNaOH,欲使其完全溶解变成不饱和溶液,下列说法中正确的是_____
A 溶液中溶质的质量分数可能不变 B 溶液中溶质的质量分数一定减小
C 溶液中溶质的质量一定增大 D 溶液中溶质的质量分数一定增大
E NaOH的溶解度一定变大 F 可以升温到40℃以上
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaOH | 31 | 91 | 111 | X | 313 | 336 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
(1)为测定X的值,取四份60℃的水各50g,分别进行实验,并记录数据如下:
| 实验编号 | 实验1 | 实验2 | 实验3 | 实验4 | |
| NaOH/g | 50 | 60 | 70 | 80 | |
| H2O/g | 50 | 50 | 50 | 50 | |
| 溶液质量g/ | 100 | 110 | 114.5 | 114.5 | |
实验结果分析,可知X的值为
(2)去除NaOH溶液中的Ca(OH)2,通过蒸发浓缩、
(3)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复到20℃得到的溶液(乙溶液),此时溶液的溶质质量分数乙
(4)在20℃时,向盛有100g水的烧杯中加入111gNaOH,欲使其完全溶解变成不饱和溶液,下列说法中正确的是
A 溶液中溶质的质量分数可能不变 B 溶液中溶质的质量分数一定减小
C 溶液中溶质的质量一定增大 D 溶液中溶质的质量分数一定增大
E NaOH的溶解度一定变大 F 可以升温到40℃以上
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是X、Y、Z三种物质的溶解度曲线图,认真阅读完成下列各小题
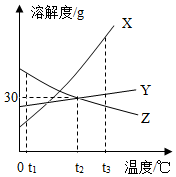
(1)在_____ ℃时,Y、Z两物质溶解度相等。
(2)t2℃时,将20gZ放入装有50g水的烧杯中,充分搅拌可能得到_______ gZ的饱和溶液。
(3)在t1℃时把质量均为mg的X、Y、Z三种固体溶于水中形成饱和溶液,需水质量最多的是_ 。
(4)下列说法正确的有_______ (只需填正确的选项序号)。
①Z物质有可能是气体
②若X中含有少量的Y,可用蒸发结晶提纯X
③将t3℃时等质量的X、Y饱和溶液同时降温到t1℃,析出晶体的质量是X>Y
④要将t1℃时接近饱和的X溶液变成饱和溶液,如不改变该溶液的组成,可选择降低温度的方法
⑤将t3℃时Z的饱和溶液降温至t2℃后,溶液的溶质质量分数会变大
(5)t2℃时,将X、Y、Z三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的顺序是_______ 。

(1)在
(2)t2℃时,将20gZ放入装有50g水的烧杯中,充分搅拌可能得到
(3)在t1℃时把质量均为mg的X、Y、Z三种固体溶于水中形成饱和溶液,需水质量最多的是
(4)下列说法正确的有
①Z物质有可能是气体
②若X中含有少量的Y,可用蒸发结晶提纯X
③将t3℃时等质量的X、Y饱和溶液同时降温到t1℃,析出晶体的质量是X>Y
④要将t1℃时接近饱和的X溶液变成饱和溶液,如不改变该溶液的组成,可选择降低温度的方法
⑤将t3℃时Z的饱和溶液降温至t2℃后,溶液的溶质质量分数会变大
(5)t2℃时,将X、Y、Z三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的顺序是
您最近一年使用:0次
【推荐3】KNO3是一种重要的化工原料。
(1)宋代《开宝本草》中记载了KNO3的提纯方法:“所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”“霜”指KNO3,“以水淋汁”是指溶解,“煎炼而成”是指______ (填化学实验基本操作)。
(2)20℃时在盛有100g水的烧杯中加入70g硝酸钾,充分溶解后,逐渐升温(不考虑水蒸发的影响),测定不同温度时剩余固体质量。测定结果记录如表:
20℃时,得到的是硝酸钾的______ (填“饱和”或“不饱和”)溶液。
(3)如图7为KNO3的溶解度曲线,a、b在溶解度曲线上。
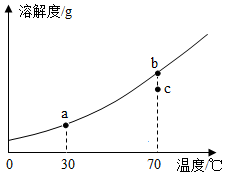
①将a点对应的溶液升温到70℃,其溶质质量分数______ (填“变大”“变小”或“不变”)。
②欲使KNO3溶液的状态从b点转化为c点,可采取的措施是______ 。
(1)宋代《开宝本草》中记载了KNO3的提纯方法:“所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”“霜”指KNO3,“以水淋汁”是指溶解,“煎炼而成”是指
(2)20℃时在盛有100g水的烧杯中加入70g硝酸钾,充分溶解后,逐渐升温(不考虑水蒸发的影响),测定不同温度时剩余固体质量。测定结果记录如表:
| 溶液温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 剩余固体质量/g | 38.4 | 24.2 | 6.1 | 0 | 0 |
(3)如图7为KNO3的溶解度曲线,a、b在溶解度曲线上。

①将a点对应的溶液升温到70℃,其溶质质量分数
②欲使KNO3溶液的状态从b点转化为c点,可采取的措施是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】物质的分离与提纯是利用物质的性质差异,可以通过物理方法或化学方法对混合物进行分离提纯,获取有用物质。
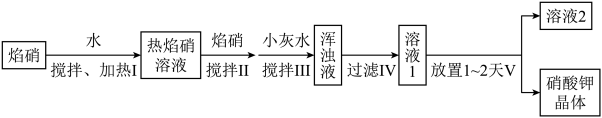
(1)我国古代提纯焰硝(含KNO3和少量NaCl、CaCl2等)获得农用硝酸钾,主要流程如下:___________ 。
②步骤Ⅲ加小灰水(含K2CO3)时,发生反应的化学方程式为___________ 。
(2)结合如图溶解度曲线分析:___________ 。
②趁热过滤后得到溶液1,后续操作主要包括___________ 、___________ 等。
③“溶液2”除了含有Na+、Cl-外,还含有的离子有___________ (填离子符号)。
(3)上述操作中搅拌常用的仪器是___________ 。
(1)我国古代提纯焰硝(含KNO3和少量NaCl、CaCl2等)获得农用硝酸钾,主要流程如下:
②步骤Ⅲ加小灰水(含K2CO3)时,发生反应的化学方程式为
(2)结合如图溶解度曲线分析:
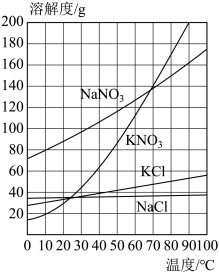
②趁热过滤后得到溶液1,后续操作主要包括
③“溶液2”除了含有Na+、Cl-外,还含有的离子有
(3)上述操作中搅拌常用的仪器是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐2】水是生命的源泉
(1)净化水常用的方法有沉淀、过滤等,活性炭在净水器中能起到过滤和______ 的作用。
(2)下列洗涤方法中,利用乳化原理的是____________ 。
A.用洗涤精清洗衣服上的油污 B.用酒精洗去试管中的碘 C.用汽油清洗油渍
(3)要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下的方法。其中可行的是______ (填序号)
①加入 CaO ②加入Ca(OH)2 ③升高温度 ④降低温度
(4)如图为甲、乙两种固体物质的溶解度曲线,请据图回答下列问题
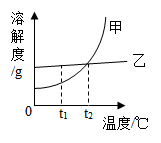
①t2℃时,甲、乙两种物质饱和溶液中的溶质质量分数的大小关系为:甲_____ 乙(填“>”、“<”或“=”)。
②要从乙的饱和溶液中获得较多的晶体,宜采用的结晶方法是____ 结晶。
③t1℃,取等质量的甲、乙两种固体分别配成饱和溶液,需水质量较多的是_______ (填“甲”或“乙”)。
(1)净化水常用的方法有沉淀、过滤等,活性炭在净水器中能起到过滤和
(2)下列洗涤方法中,利用乳化原理的是
A.用洗涤精清洗衣服上的油污 B.用酒精洗去试管中的碘 C.用汽油清洗油渍
(3)要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下的方法。其中可行的是
①加入 CaO ②加入Ca(OH)2 ③升高温度 ④降低温度
(4)如图为甲、乙两种固体物质的溶解度曲线,请据图回答下列问题

①t2℃时,甲、乙两种物质饱和溶液中的溶质质量分数的大小关系为:甲
②要从乙的饱和溶液中获得较多的晶体,宜采用的结晶方法是
③t1℃,取等质量的甲、乙两种固体分别配成饱和溶液,需水质量较多的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如图是a、b、c三种固体物质的溶解度曲线:请回答下列问题:
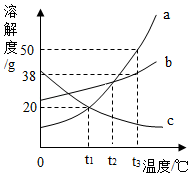
(1)t1℃时a物质的饱和溶液中溶液质量与溶剂质量的比(最简比)_____ 。
(2)三种物质的结晶方法与海水晒盐相同的是_____ (填“a”“b”或“c”)
(3)t3℃时,把10ga、b、c三种物质分别加入盛有25g水的烧杯中不断搅拌,充分溶解后恢复至t3℃,所得溶液的溶质质量分数大小关系为_____ (填字母,下同)再将溶液降低到t1℃时所得溶液质量由小到大的顺序为_____ 。
(4)t1℃时a、b、c三种物质的饱和溶液同时升温到t2℃此时溶液中溶质的质量分数大小关系是_____ 。

(1)t1℃时a物质的饱和溶液中溶液质量与溶剂质量的比(最简比)
(2)三种物质的结晶方法与海水晒盐相同的是
(3)t3℃时,把10ga、b、c三种物质分别加入盛有25g水的烧杯中不断搅拌,充分溶解后恢复至t3℃,所得溶液的溶质质量分数大小关系为
(4)t1℃时a、b、c三种物质的饱和溶液同时升温到t2℃此时溶液中溶质的质量分数大小关系是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】工业上用N2和H2合成NH3是人类科学技术的一项重大突破。
(1)①N2可通过分离液态空气获得,该方法利用了N2和O2沸点的差异。沸点属于物质的______ (选填“物理”或“化学”)性质。
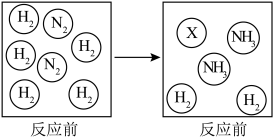
②一定条件下,向容器中充入一定量的N2和H2,充分反应生成NH3。反应前后物质的变化如图,图中X代表的分子为______ (填化学式)。
(2)NH3与氰酸(HOCN)反应生成尿素【CO(NH2)2】。
①尿素为农作物生长提供的主要营养元素为______ 。
②尿素可用于去除大气污染物中的NO,其化学反应为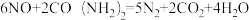 。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少?(请补全计算过程)
。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少?(请补全计算过程)
解:设需要10%的尿素溶液的溶质质量为x
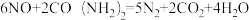
180______
6g x
列出比例式,求解______
x=4g。
求算10%的尿素溶液的质量m为______ (列式并计算出结果)。
答:略。
(1)①N2可通过分离液态空气获得,该方法利用了N2和O2沸点的差异。沸点属于物质的
②一定条件下,向容器中充入一定量的N2和H2,充分反应生成NH3。反应前后物质的变化如图,图中X代表的分子为

(2)NH3与氰酸(HOCN)反应生成尿素【CO(NH2)2】。
①尿素为农作物生长提供的主要营养元素为
②尿素可用于去除大气污染物中的NO,其化学反应为
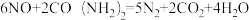 。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少?(请补全计算过程)
。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少?(请补全计算过程)解:设需要10%的尿素溶液的溶质质量为x
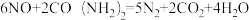
180
6g x
列出比例式,求解
x=4g。
求算10%的尿素溶液的质量m为
答:略。
您最近一年使用:0次
【推荐2】氯化钠和碳酸钠在不同温度下的溶解度如表所示,请回答下列问题:
(1)10℃时,两种物质的饱和溶液中,溶质质量分数较大的是_____ (填“NaCl”或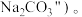
(2)在40℃时,取mg碳酸钠溶液进行如图所示实验:_____ (填“饱和”或“不饱和”)溶液。
②
_____ 。
(3)生活在盐湖附近的人们“夏天晒盐(NaCl)”、“冬天捞碱___________________ (填“蒸发结晶”或“降温结晶”)。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.`6 | 37.0 |
| Na2CO3 | 7.0 | 12.5 | 21.8 | 39.7 | 48.8 | 47.3 | |
(1)10℃时,两种物质的饱和溶液中,溶质质量分数较大的是
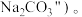
(2)在40℃时,取mg碳酸钠溶液进行如图所示实验:
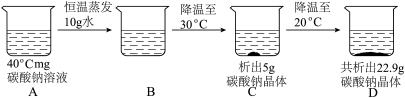
②

(3)生活在盐湖附近的人们“夏天晒盐(NaCl)”、“冬天捞碱
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】溶液在生产和生活中有重要意义。
(1)氯化钠溶液中溶质是______ ;硝酸钾溶液中的溶剂是 ______ 。
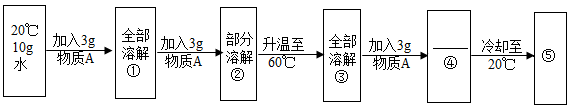
(2)某兴趣小组为了研究物质的溶解和结晶,做了如下所述过程的实验:
小资料:氯化钠和硝酸钾的溶解度数值:
①物质A是________ (填“氯化钠”或“硝酸钾”)
②状态“④”时,物质A_____ 溶解(填“部分”或“全部”)
③上述实验过程中所得溶液达到饱和的是_______ (填数字序号,下同);溶质质量分数最大的是 _______ 。
(1)氯化钠溶液中溶质是
(2)某兴趣小组为了研究物质的溶解和结晶,做了如下所述过程的实验:

小资料:氯化钠和硝酸钾的溶解度数值:
| 项目 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
| NaCl | 35.8g | 36.0g | 36.3g | 36.6g | 37.0g | 37.3g | 37.8g |
| KNO3 | 20.9g | 31.6g | 45.8g | 63.9g | 85.5g | 110g | 138g |
①物质A是
②状态“④”时,物质A
③上述实验过程中所得溶液达到饱和的是
您最近一年使用:0次