(一)金属及金属材料在生产、生活中有广泛的应用。
(1)近年来,我省多地纷纷开展文明城市创建工作,垃圾分类回收是其中一项重要举措。某市街道垃圾桶如图所示,请回答下列问题:

①图中标识的物质,属于金属材料的是______ (写出一种即可)。
②使用铝合金做内筒的优点是______ (写出一点即可)。某品牌饮料的空易拉罐应收入______ (填“可回收”或“不可回收”)筒中。
(2)《淮南万毕术》记载有“曾青(指硫酸铜溶液)得铁化为铜”,相关的化学方程式是______ ,该反应说明铁的金属活动性比铜______ (填“强”或“弱”)。
(3)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是______ (填字母)。
A.若滤液为蓝色,则滤渣中一定有银,可能有铜
B.若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、
C.若滤液为浅绿色,则滤渣中一定含银、铜、铝
D.若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
(二)2019 年 5 月湖南省第七届矿博会在郴州市隆重举行,展厅上展出了各种矿物,其中有一 枚黑色的陨石引起了大家的兴趣。查阅资料获知,陨石的主要成分是铁和铁的化合物。
(1)通常情况下碳粉和铁粉都是黑色,检验碳粉中是否含有铁粉既可用物理方法又可 用化学方法:
①物理方法是______ ;
②化学方法是______ 。
(2)常见铁的氧化物有 FeO、Fe2O3、______ 。(填化学式)
(3)铁制品在潮湿的空气中易生锈,实际上是铁与空气中的氧气、______ 等发生化 学反应的过程,请举出一例防止铁制品锈蚀的方法______ 。
实验员小明取一小块陨石进行了研究,研究过程如图所示:
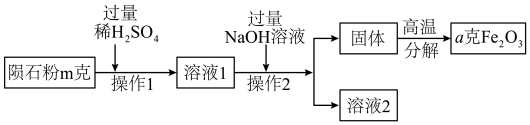
(4)图中操作 2的名称是______ 。
(5)溶液2中的溶质是______ 。(写化学式)
(6)陨石中含铁元素的质量分数为______ 。
(1)近年来,我省多地纷纷开展文明城市创建工作,垃圾分类回收是其中一项重要举措。某市街道垃圾桶如图所示,请回答下列问题:

①图中标识的物质,属于金属材料的是
②使用铝合金做内筒的优点是
(2)《淮南万毕术》记载有“曾青(指硫酸铜溶液)得铁化为铜”,相关的化学方程式是
(3)将一定质量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是
A.若滤液为蓝色,则滤渣中一定有银,可能有铜
B.若滤渣中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、

C.若滤液为浅绿色,则滤渣中一定含银、铜、铝
D.若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
(二)2019 年 5 月湖南省第七届矿博会在郴州市隆重举行,展厅上展出了各种矿物,其中有一 枚黑色的陨石引起了大家的兴趣。查阅资料获知,陨石的主要成分是铁和铁的化合物。
(1)通常情况下碳粉和铁粉都是黑色,检验碳粉中是否含有铁粉既可用物理方法又可 用化学方法:
①物理方法是
②化学方法是
(2)常见铁的氧化物有 FeO、Fe2O3、
(3)铁制品在潮湿的空气中易生锈,实际上是铁与空气中的氧气、
实验员小明取一小块陨石进行了研究,研究过程如图所示:

(4)图中操作 2的名称是
(5)溶液2中的溶质是
(6)陨石中含铁元素的质量分数为
2021九年级下·江苏镇江·专题练习 查看更多[1]
(已下线)必刷卷04-2021年中考化学考前信息必刷卷(镇江专用)
更新时间:2021-07-16 00:09:08
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】某氮肥厂用煤、空气和水为原料合成氨气(NH3),同时可得到副产品碳酸氢铵(NH4HCO3)。其工艺流程如图所示:

回答下列有关问题:
(1)煤加入煤气发生炉前需经过粉碎处理,其目的是___________ 。
(2)“合成塔”中发生反应的化学方程式是___________ ,该反应属于___________ (填基本反应类型)反应。
(3)部分氨气通入“碳化塔”的目的是___________ 。
(4)氨气被广泛认为是未来理想的零碳燃料,其燃烧的微观示意图如图所示。

参加反应的甲、乙分子个数比是___________ 。
(5)粮食安全是国家安全的重要基础,化肥对提高粮食产量有重要作用。尿素【CO(NH2)2】是常用的氮肥之一、已知: 。
。
①一个尿素分子中共有_______ 个原子,尿素中氮元素的质量分数为________ (只列计算式)。
②某农业合作社需要12t尿素,请计算合成这些尿素需要CO2的质量是___________ t。

回答下列有关问题:
(1)煤加入煤气发生炉前需经过粉碎处理,其目的是
(2)“合成塔”中发生反应的化学方程式是
(3)部分氨气通入“碳化塔”的目的是
(4)氨气被广泛认为是未来理想的零碳燃料,其燃烧的微观示意图如图所示。

参加反应的甲、乙分子个数比是
(5)粮食安全是国家安全的重要基础,化肥对提高粮食产量有重要作用。尿素【CO(NH2)2】是常用的氮肥之一、已知:
 。
。①一个尿素分子中共有
②某农业合作社需要12t尿素,请计算合成这些尿素需要CO2的质量是
您最近一年使用:0次
【推荐2】(一)化学实验:气体的制取和性质是初中化学的重要学习内容,根据下图所示装置回答问题。
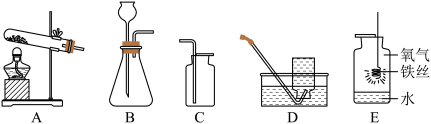
(1)如何验证一瓶无色气体为氧气。
(2)用H2O2溶液和MnO2制取O2的化学方程式为___________ ;实验室用该方法制取和收集一瓶干燥的O2,需选用的一套实验装置是___________ (填序号)。
(3)装置E中发生的化学反应方程式是:___________ ;装置中水的作用是___________ 。
(4)实验室也可用上图中部分装置制取氢气。已知锌粒和稀硫酸反应生成硫酸锌和氢气,请写出该反应的方程式___________ 。
(二)化学计算:
(5)原子核内有6个质子和6个中子的碳原子质量为A千克,若某原子的真实质量为M千克,则该原子的相对原子质量为___________ 。
(6)硝酸铵中氮元素、氢元素和氧元素的质量比为___________ (最简整数比);___________ g硝酸铵中所含氮元素的质量和76g的一种新型火箭燃料N(NO2)3中所含氮元素的质量相等。
(7)尿素【CO(NH2)2】中氮元素的质量分数为___________ (保留一位小数)。

(1)如何验证一瓶无色气体为氧气。
(2)用H2O2溶液和MnO2制取O2的化学方程式为
(3)装置E中发生的化学反应方程式是:
(4)实验室也可用上图中部分装置制取氢气。已知锌粒和稀硫酸反应生成硫酸锌和氢气,请写出该反应的方程式
(二)化学计算:
(5)原子核内有6个质子和6个中子的碳原子质量为A千克,若某原子的真实质量为M千克,则该原子的相对原子质量为
(6)硝酸铵中氮元素、氢元素和氧元素的质量比为
(7)尿素【CO(NH2)2】中氮元素的质量分数为
您最近一年使用:0次
【推荐3】回答下列问题:
(1)按要求从氮气、浓硫酸、氢氧化钙、氧化铜中选取合适的物质,将其化学式填写在下列横线上。
①延长食品保质期的气体_______ 。
②一种金属氧化物_______ 。
③常用作干燥剂的酸_______ 。
④改良酸性土壤的碱_______ 。
(2)2023年10月26日11时14分,搭载神舟十七号载人飞船的长征二号F遥十七运载火箭在酒泉卫星发射中心点火发射。_______ 。从环保的角度写一点氢气用作燃料的优点_______ 。
②为了保护航天器和航天员的安全,需要使用热保护材料。热保护材料一般含有机聚合物,其中一种聚合物为环氧树脂。其分子式为(C11H12O3)n。在环氧树脂[(C11H12O3)n]中,氢、氧两种原子的个数之比为_______ (最简整数比),质量分数最大的元素为_______ (填元素名称)。
③火箭发射使用的氢能源是高效的新能源。理想的氢能源循环体系是利用合适的光分解催化剂,使水在太阳光的照射下分解产生氢气。若要制取4kg氢气,理论上至少需要分解水_______ kg。
(1)按要求从氮气、浓硫酸、氢氧化钙、氧化铜中选取合适的物质,将其化学式填写在下列横线上。
①延长食品保质期的气体
②一种金属氧化物
③常用作干燥剂的酸
④改良酸性土壤的碱
(2)2023年10月26日11时14分,搭载神舟十七号载人飞船的长征二号F遥十七运载火箭在酒泉卫星发射中心点火发射。


②为了保护航天器和航天员的安全,需要使用热保护材料。热保护材料一般含有机聚合物,其中一种聚合物为环氧树脂。其分子式为(C11H12O3)n。在环氧树脂[(C11H12O3)n]中,氢、氧两种原子的个数之比为
③火箭发射使用的氢能源是高效的新能源。理想的氢能源循环体系是利用合适的光分解催化剂,使水在太阳光的照射下分解产生氢气。若要制取4kg氢气,理论上至少需要分解水
您最近一年使用:0次
综合应用题
|
适中
(0.65)
真题
解题方法
【推荐1】2017年4月,“航母”下水,开拓中国新蓝海。

(1)“航母”舰体材料为合金钢,国产航母使用的“超级钢”具有极佳的抗压性、延展性和焊接性。合金钢是__ (填序号)
a合成材料 b复合材料 c无机材料
(2)“航母”升降机可由铝合金制造,用石墨作电极在高温条件下电解熔融氧化铝,在阴极和阳极区分别得到A1和O2,阳极区使用的石墨易消耗的原因是__ 。
(3)“航母”螺旋桨可由铜合金制造。铜合金比铜的硬度__ (填“大”或“小”),铜比铁在海水中耐腐蚀的原因是__ 。
(4)由生铁炼钢时,硅(Si)与氧化亚铁在高温条件下反应生成二氧化硅和铁,该反应的化学方程式为__ 。

(1)“航母”舰体材料为合金钢,国产航母使用的“超级钢”具有极佳的抗压性、延展性和焊接性。合金钢是
a合成材料 b复合材料 c无机材料
(2)“航母”升降机可由铝合金制造,用石墨作电极在高温条件下电解熔融氧化铝,在阴极和阳极区分别得到A1和O2,阳极区使用的石墨易消耗的原因是
(3)“航母”螺旋桨可由铜合金制造。铜合金比铜的硬度
(4)由生铁炼钢时,硅(Si)与氧化亚铁在高温条件下反应生成二氧化硅和铁,该反应的化学方程式为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐2】金属用途广泛,其结构和性质等是化学的重要研究内容,人类文明的发展和社会的进步同金属材料关系十分密切。
(1)我国“蛟龙”号载人潜水器上使用了钛合金,钛合金放在海水中数年仍光亮如初,这是因为它______ (填字母代号)。
a易加工 b密度小 c熔点高 d耐腐蚀
(2)铝是活泼金属,为什么通常铝锅却很耐腐蚀?______
(3)向含有Cu(NO3)2和AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,所得固体的质量等于加入锌粉的质量。
①请分析所得固体的成分______ 。
②写出一个有关反应的化学方程式______ 。
(4)钢铁是基本的结构材料,称为“工业的骨骼”。实验室可利用如图装置模拟炼铁反应。

①写出a处V形管内发生反应的化学方程式______ 。
②请描述b处V形管内可观察到的现象______ 。
③请写出尾气处理的一条具体措施______ 。
(5)高铁的快速发展方便了人们的出行。工业上可利用铝和氧化铁在高温下发生置换反应制得铁来焊接钢轨,若用足量的铝与16kg氧化铁反应,理论上可制得铁的质量是多少?______
(1)我国“蛟龙”号载人潜水器上使用了钛合金,钛合金放在海水中数年仍光亮如初,这是因为它
a易加工 b密度小 c熔点高 d耐腐蚀
(2)铝是活泼金属,为什么通常铝锅却很耐腐蚀?
(3)向含有Cu(NO3)2和AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,所得固体的质量等于加入锌粉的质量。
①请分析所得固体的成分
②写出一个有关反应的化学方程式
(4)钢铁是基本的结构材料,称为“工业的骨骼”。实验室可利用如图装置模拟炼铁反应。

①写出a处V形管内发生反应的化学方程式
②请描述b处V形管内可观察到的现象
③请写出尾气处理的一条具体措施
(5)高铁的快速发展方便了人们的出行。工业上可利用铝和氧化铁在高温下发生置换反应制得铁来焊接钢轨,若用足量的铝与16kg氧化铁反应,理论上可制得铁的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】金属材料广泛应用于生产生活中。
(1)纯铁与不锈钢相比较,硬度较大的是______ 。
(2)除去铜粉中混有少量的铁粉,加入足量的硫酸铜溶液,过滤、洗涤、烘干。发生反应的化学方程式为______ 。
(3)用 含
含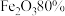 的赤铁矿石,理论上可以冶炼含铁
的赤铁矿石,理论上可以冶炼含铁 的生铁的质量是
的生铁的质量是______  计算结果精确至
计算结果精确至 。
。
(4)向AgNO3、Cu(NO3)2、Mg(NO3)2 的混合溶液中,加入一定量的铁粉,充分反应后过滤,滤液呈蓝色。下列判断正确的是 。
(1)纯铁与不锈钢相比较,硬度较大的是
(2)除去铜粉中混有少量的铁粉,加入足量的硫酸铜溶液,过滤、洗涤、烘干。发生反应的化学方程式为
(3)用
 含
含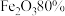 的赤铁矿石,理论上可以冶炼含铁
的赤铁矿石,理论上可以冶炼含铁 的生铁的质量是
的生铁的质量是 计算结果精确至
计算结果精确至 。
。(4)向AgNO3、Cu(NO3)2、Mg(NO3)2 的混合溶液中,加入一定量的铁粉,充分反应后过滤,滤液呈蓝色。下列判断正确的是 。
| A.向滤渣中加入稀盐酸,可能有气泡产生 |
| B.滤液中一定含有Fe(NO3)2、Mg(NO3)2 和Cu(NO3)2 |
| C.与原溶液相比,滤液质量可能增大 |
| D.向滤液中滴入稀盐酸,可能会有白色沉淀出现 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】《天工开物》记载“凡钟为金乐之首”,在古代的金属乐器之中,钟是最重要的乐器。铸钟的材料,铜为上等,铁为下等。金属和金属材料在生产和生活中有着广泛的应用。请完成有关金属性质的实验。
Ⅰ.金属的物理性质
(1)铁是应用最广泛的金属.生活中用铁锅做饮具,主要利用铁的______ 性;
Ⅱ.金属的化学性质
(2)将稀盐酸滴加到装有铁、铜的试管中
①一种金属和酸不反应的理由______ ;
②另一种金属与酸反应的现象______ 。
Ⅲ.探究金属的活动性强弱
(3)①有X、Y、Z三种金属,它们具有如下性质:
a.X、Z均不与稀盐酸反应
b.
c.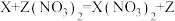
则X、Y、Z三种金属活动性由强到弱的顺序是______ ;
②在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,得到滤渣和滤液,向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是______ (填化学式)。
Ⅳ.某工厂欲从含有 的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:
的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:______ 。
(5)加入过量A物质的化学式是______ 。
(6)加入适B物质时反应的化学方程式是______ 。
Ⅴ.据有关资料报道,世界上每年因腐蚀而报废的金属设备或材料相当于年产量的20%~40%。
(7)炼铁时焦炭的作用______ ,回收报废金属的意义______ 。
(8)请写出自行车链条防止生锈的方法______ 。
Ⅰ.金属的物理性质
(1)铁是应用最广泛的金属.生活中用铁锅做饮具,主要利用铁的
Ⅱ.金属的化学性质
(2)将稀盐酸滴加到装有铁、铜的试管中
①一种金属和酸不反应的理由
②另一种金属与酸反应的现象
Ⅲ.探究金属的活动性强弱
(3)①有X、Y、Z三种金属,它们具有如下性质:
a.X、Z均不与稀盐酸反应
b.

c.
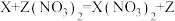
则X、Y、Z三种金属活动性由强到弱的顺序是
②在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,得到滤渣和滤液,向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是
Ⅳ.某工厂欲从含有
 的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:
的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:
(5)加入过量A物质的化学式是
(6)加入适B物质时反应的化学方程式是
Ⅴ.据有关资料报道,世界上每年因腐蚀而报废的金属设备或材料相当于年产量的20%~40%。
(7)炼铁时焦炭的作用
(8)请写出自行车链条防止生锈的方法
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】整理和归纳、探究是有效的学习方法。下面是某中学化学学习小组的同学对Al、Fe、Mn、Cu、Hg等金属相关知识的归纳复习,请你参与并回答问题:
(1)从物理性质上看,每种金属都有自己的特性。你认为汞与其它金属的不同之处是________ ;
(2)铝的化学性质比铁要活泼,但是铝制品却很耐腐蚀,其原因是(用化学方程式表示)____________________________ ;
(3)该化学兴趣小组的同学为了探究铁(Fe)、锰(Mn)和铜(Cu)三种金属的活动性顺序,进行下列探究。
①同学们将等大小的三种金属同时放入等质量、等质量分数的稀硫酸中,发现锰表面冒出气泡的速率比铁快,而铜表面无现象。请将三种金属的元素符号填入下表:

_________________
如果金属锰与稀硫酸反应生成的盐是硫酸锰(MnSO4),请你写出锰与稀硫酸反应的化学方程式_____________________________ ;
②兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液。他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:

1.甲同学提出X可用金属铁,乙同学认为X可用金属锰,你认为_______ (选填“甲”或“乙”)同学的意见是正确的,加入过量的金属X的目的是___________ ;
2.操作a、b的名称是_______ ,步骤Ⅱ中发生反应的化学方程式为______ ;
(1)从物理性质上看,每种金属都有自己的特性。你认为汞与其它金属的不同之处是
(2)铝的化学性质比铁要活泼,但是铝制品却很耐腐蚀,其原因是(用化学方程式表示)
(3)该化学兴趣小组的同学为了探究铁(Fe)、锰(Mn)和铜(Cu)三种金属的活动性顺序,进行下列探究。
①同学们将等大小的三种金属同时放入等质量、等质量分数的稀硫酸中,发现锰表面冒出气泡的速率比铁快,而铜表面无现象。请将三种金属的元素符号填入下表:

如果金属锰与稀硫酸反应生成的盐是硫酸锰(MnSO4),请你写出锰与稀硫酸反应的化学方程式
②兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液。他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:

1.甲同学提出X可用金属铁,乙同学认为X可用金属锰,你认为
2.操作a、b的名称是
您最近一年使用:0次
【推荐3】2019年7月1日《上海市生活垃圾管理条例》正式开始实施。实行垃圾分类关系到广大人民群众的生活环境,是社会文明水平的一个重要体现。垃圾分类回收,可减少垃圾量达50%以上,减少占地。据悉,1吨废弃塑料可回炼600千克的柴油;1吨易拉罐熔化后,可少开采20吨铝矿。请回答:
(1)实行垃圾分类可以节约资源,某废品回收站回收了5吨废弃塑料,可回炼______ 吨柴油。
(2)琳琳是积极参与垃圾分类回收的一员,她对垃圾分类回收的做法或想法正确的是______。
(3)某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下图:

资料1:垃圾焚烧产生的烟气中含有SO2等有害气体。资料2:FeSO4容易被空气中O2氧化。
资料3:Fe+Fe2(SO4)3=3FeSO4
①SO2与CO2具有相似的化学性质,则石灰浆吸收烟气的化学反应方程式为______ 。
②将所得FeSO4溶液在氮气环境中蒸发浓缩、降温结晶、过滤,得到FeSO4晶体,其中氮气的作用是______ 。
③稀硫酸溶解生锈的铁制品过程中发生的化学反应有______ 个。
(1)实行垃圾分类可以节约资源,某废品回收站回收了5吨废弃塑料,可回炼
(2)琳琳是积极参与垃圾分类回收的一员,她对垃圾分类回收的做法或想法正确的是______。
| A.吃剩的午餐属于有害垃圾 |
| B.喝剩的矿泉水瓶将水倒掉后,将瓶子放入可回收垃圾箱中 |
| C.建议回收废弃医疗垃圾制作餐具 |
| D.为了节省盛放垃圾的塑料袋,将所有的垃圾堆积在一起 |
(3)某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下图:

资料1:垃圾焚烧产生的烟气中含有SO2等有害气体。资料2:FeSO4容易被空气中O2氧化。
资料3:Fe+Fe2(SO4)3=3FeSO4
①SO2与CO2具有相似的化学性质,则石灰浆吸收烟气的化学反应方程式为
②将所得FeSO4溶液在氮气环境中蒸发浓缩、降温结晶、过滤,得到FeSO4晶体,其中氮气的作用是
③稀硫酸溶解生锈的铁制品过程中发生的化学反应有
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】共享单车可实现绿色出行。

(1)在如图中所标示的共享单车各部件中,属于金属材料的是______ 。(填序号)
(2)防止自行车链条生锈的有效措施是______ 。
(3)自行车有些零件选用了铝合金材料,其优点是质量轻、硬度大和______ 。
(4)废弃的生锈铁制品可以制取氯化铁,用于工业废水的处理,由部分锈蚀的铁制品制备氯化铁晶体的主要过程如图所示。
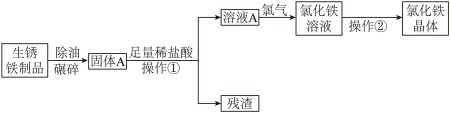
①操作1是______ 。
②操作2中需要用玻璃棒搅拌的目的是______ 。
③固体A与稀盐酸发生置换反应的化学方程式为______ 。

(1)在如图中所标示的共享单车各部件中,属于金属材料的是
(2)防止自行车链条生锈的有效措施是
(3)自行车有些零件选用了铝合金材料,其优点是质量轻、硬度大和
(4)废弃的生锈铁制品可以制取氯化铁,用于工业废水的处理,由部分锈蚀的铁制品制备氯化铁晶体的主要过程如图所示。

①操作1是
②操作2中需要用玻璃棒搅拌的目的是
③固体A与稀盐酸发生置换反应的化学方程式为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】钢铁的生产和使用是人类文明和社会进步的一个重要标志。某炼铁厂以焦炭(主要成分为C)、赤铁矿、空气等为主要原料炼铁,反应过程如下:

(1)①写出步骤③中发生反应的化学方程式______ 。
②实验室模拟炼铁过程中,点燃酒精喷灯之前,先通入CO气体的原因是______ 。
③每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。试举一种减缓钢铁锈蚀的方法______ 。
(2)海水中蕴藏着丰富的资源,海水综合利用的流程图如下:

分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品,产品中常常含有Mg(OH)2。某兴趣小组为了探究粗产品中MgCl2的含量,进行如下实验:在一烧杯中盛有Mg(OH)2和MgCl2的固体粉末20g,向其中加入50水,经充分溶解后,再逐滴加入溶质质量分数为10%的稀盐酸。烧杯中溶质的总质量与加入稀盐酸的质量关系如图所示。请回答下列问题:

①当滴入稀盐酸100g时(即图中C点时),烧杯内溶液中一定存在的阳离子是______ (写离子符号)。
②当滴入稀盐酸73g时(即图中B点时),试通过计算,求固体粉末中MgCl2的质量______ (计算结果精确至0.1g)。

(1)①写出步骤③中发生反应的化学方程式
②实验室模拟炼铁过程中,点燃酒精喷灯之前,先通入CO气体的原因是
③每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。试举一种减缓钢铁锈蚀的方法
(2)海水中蕴藏着丰富的资源,海水综合利用的流程图如下:

分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品,产品中常常含有Mg(OH)2。某兴趣小组为了探究粗产品中MgCl2的含量,进行如下实验:在一烧杯中盛有Mg(OH)2和MgCl2的固体粉末20g,向其中加入50水,经充分溶解后,再逐滴加入溶质质量分数为10%的稀盐酸。烧杯中溶质的总质量与加入稀盐酸的质量关系如图所示。请回答下列问题:

①当滴入稀盐酸100g时(即图中C点时),烧杯内溶液中一定存在的阳离子是
②当滴入稀盐酸73g时(即图中B点时),试通过计算,求固体粉末中MgCl2的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】金属材料在生产、生活中有广泛的应用。
(1)“沉睡三千年、一醒惊天下”。2021年3月20日,三星堆遗址重大发现,出土巨青铜面具、青铜神树等重要文物。该青铜器被称之为磷铜,磷铜和纯铜相比,硬度较大的是_________ 。
(2)根据有关报道,现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量20%~40%。钢铁在常温下同时接触氧气和水容易生锈,请写出一种铁的防锈措施:_________ 。
(3)将锌粉加入到一定量的Mg(NO3)2、Cu(NO3)2、AgNO3的混合溶液中,充分反应后过滤。
①若向过滤后所得固体中滴加盐酸有气泡产生,则该固体中含有的金属有哪些_______ (写化学式)
②请写出该过程中使溶液质量减小的反应的化学方程式_______ 。
(4)某同学设计了用CO还原该铁片的实验如图所示。
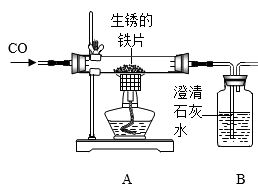
①从环保角度来看,该实验装置存在缺陷,其改进方法是_______ 。
②A装置中玻璃管内发生反应的化学方程式为_______ 。
③B装置的作用为________ 。
(5)工业上常采用铝热反应来制取铁,原理是铝粉与四氧化三铁在高温下发生置换反应,生成铁和氧化铝。用铝粉与足量四氧化三铁反应,若制取56kg的铁,理论上需要铝粉的质量为多少?
(1)“沉睡三千年、一醒惊天下”。2021年3月20日,三星堆遗址重大发现,出土巨青铜面具、青铜神树等重要文物。该青铜器被称之为磷铜,磷铜和纯铜相比,硬度较大的是
(2)根据有关报道,现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量20%~40%。钢铁在常温下同时接触氧气和水容易生锈,请写出一种铁的防锈措施:
(3)将锌粉加入到一定量的Mg(NO3)2、Cu(NO3)2、AgNO3的混合溶液中,充分反应后过滤。
①若向过滤后所得固体中滴加盐酸有气泡产生,则该固体中含有的金属有哪些
②请写出该过程中使溶液质量减小的反应的化学方程式
(4)某同学设计了用CO还原该铁片的实验如图所示。

①从环保角度来看,该实验装置存在缺陷,其改进方法是
②A装置中玻璃管内发生反应的化学方程式为
③B装置的作用为
(5)工业上常采用铝热反应来制取铁,原理是铝粉与四氧化三铁在高温下发生置换反应,生成铁和氧化铝。用铝粉与足量四氧化三铁反应,若制取56kg的铁,理论上需要铝粉的质量为多少?
您最近一年使用:0次



