水和溶液与人类的生活、生产密切相关。
(1)电解水实验可证明水的组成,其反应的化学方程式为______ 。
(2)天然水通过①沉淀、②过滤、③蒸馏等操作可以得到不同程度的净化。综合运用上述操作净水效果会更好,运用的先后顺序是______ (填序号)。
(3)图一是硝酸钾的溶解度曲线。图二是探究物质溶解过程中能量变化的实验示意图。
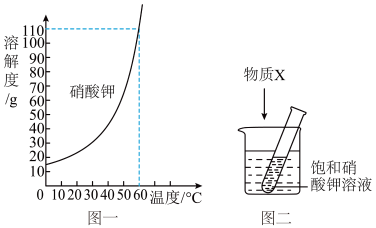
①由图一获得,硝酸钾的溶解度随温度升高而______ ; 60℃时,硝酸钾饱和溶液中溶质质量分数的表达式为______ 。
②图二实验,在盛有水的烧杯中放入一支装有饱和硝酸钾溶液的试管,向水中加入足量物质X,搅拌。物质X为______ 固体,试管中有晶体析出。
(1)电解水实验可证明水的组成,其反应的化学方程式为
(2)天然水通过①沉淀、②过滤、③蒸馏等操作可以得到不同程度的净化。综合运用上述操作净水效果会更好,运用的先后顺序是
(3)图一是硝酸钾的溶解度曲线。图二是探究物质溶解过程中能量变化的实验示意图。

①由图一获得,硝酸钾的溶解度随温度升高而
②图二实验,在盛有水的烧杯中放入一支装有饱和硝酸钾溶液的试管,向水中加入足量物质X,搅拌。物质X为
2021·辽宁阜新·中考真题 查看更多[5]
专题四 水和溶液-【备考】2023中考化学总复习(人教版)(已下线)2023年中考风向标-辽宁-溶解度曲线(已下线)2023年中考风向标-辽宁-溶液(已下线)2023年中考风向标-辽宁-水和水资源辽宁省阜新市2021年中考化学试题
更新时间:2021-07-27 22:07:04
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某自来水厂从贛江取水生产自来水,其生产流程如下图所示,请据此回答有关问题:

(1)自来水厂净水过程主要有沉淀、过滤、吸附和___________ 。
(2)加入絮凝剂的作用是___________ 。
(3)过滤时除去的杂质是___________ ,判断吸附池中发生的变化属于物理变化的依据是___________ 。
(4)目前自来水生产中常投入二氧化氯对水消毒,二氧化氯的化学式为___________ 。

(1)自来水厂净水过程主要有沉淀、过滤、吸附和
(2)加入絮凝剂的作用是
(3)过滤时除去的杂质是
(4)目前自来水生产中常投入二氧化氯对水消毒,二氧化氯的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】水是生命之源。我们应该了解水,爱护水资源。某实践小组参观本地矿泉水厂,其生产流程示意图如下。

(1)活性炭过滤器中活性炭的作用是___________ 。
(2)臭氧灭菌过程属于___________ 变化。(填“物理”或“化学”)
(3)超滤是利用薄膜(仅允许小分子和离子通过)进行物质分离的技术。经过超滤后得到的水是___________ (选填“纯净物”或“混合物”)。

(1)活性炭过滤器中活性炭的作用是
(2)臭氧灭菌过程属于
(3)超滤是利用薄膜(仅允许小分子和离子通过)进行物质分离的技术。经过超滤后得到的水是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】水是“生命之源”,是人类生活离不开的重要物质。
(1)①固态水和气态水的名称分别是________ 。
②用来盛放蒸馏水的玻璃仪器是_______ (填“细”或“广”)口瓶。
③氢气燃烧会生成水,反应的文字表达式为________ 。
(2)已知:①通常水的密度为1.0g/mL;②用胶头滴管滴20滴水约为1mL;③用胶头滴管滴下的1滴水中约有1.7×1021个水分子。则1个水分子的质量约是_____ 千克(结果用科学计数法且保留整数)。
(3)同学收集到一瓶浑浊的河水,在实验室利用如图流程来净化水,最终制成蒸馏水。

①静置时,为了使悬浮颗粒物快速沉降,常加入的物质X是________ 。
②操作a是过滤,其中用到玻璃棒的作用是_______ 。
③过滤须考虑过滤器材质孔径大小。某微粒的直径为10um,下列过滤网能把该微粒“筛”出来的是_______ (填字母)。
A.孔径20um过滤网 B.孔径10μm过滤网 C.孔径6um过滤网
④操作b是加入活性炭后再过滤。这是利用活性炭具有良好的_______ 性,来除去液体Y中的色素和异味。
⑤操作c是蒸馏。加热液体Z时有白色固体生成,说明液体Z中还含有______ (填“可溶”或“不溶”)性杂质。
(4)节约用水是每个公民的义务,下列做法不应该提倡的是________ (填字母)。
(5)清洗文物表面的氯化钠,可用蒸馏水多次浸泡除去。蒸馏水的导电能力很弱,氯化钠溶于水,会使蒸馏水的导电性增强。将文物多次浸泡,当最后一次的浸出液的导电性与_____ 基本相同时,可判断文物表面氯化钠基本除尽。
(1)①固态水和气态水的名称分别是
②用来盛放蒸馏水的玻璃仪器是
③氢气燃烧会生成水,反应的文字表达式为
(2)已知:①通常水的密度为1.0g/mL;②用胶头滴管滴20滴水约为1mL;③用胶头滴管滴下的1滴水中约有1.7×1021个水分子。则1个水分子的质量约是
(3)同学收集到一瓶浑浊的河水,在实验室利用如图流程来净化水,最终制成蒸馏水。

①静置时,为了使悬浮颗粒物快速沉降,常加入的物质X是
②操作a是过滤,其中用到玻璃棒的作用是
③过滤须考虑过滤器材质孔径大小。某微粒的直径为10um,下列过滤网能把该微粒“筛”出来的是
A.孔径20um过滤网 B.孔径10μm过滤网 C.孔径6um过滤网
④操作b是加入活性炭后再过滤。这是利用活性炭具有良好的
⑤操作c是蒸馏。加热液体Z时有白色固体生成,说明液体Z中还含有
(4)节约用水是每个公民的义务,下列做法不应该提倡的是
| A.不污染空的饮用水水桶 | B.不间断地边流水边洗衣服 |
| C.用淘米水、洗菜水浇花 | D.用喷灌、滴灌的方法代替漫灌浇灌农田 |
(5)清洗文物表面的氯化钠,可用蒸馏水多次浸泡除去。蒸馏水的导电能力很弱,氯化钠溶于水,会使蒸馏水的导电性增强。将文物多次浸泡,当最后一次的浸出液的导电性与
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】KNO3和KCl的溶解度曲线如图1所示:

(1)t3℃时,KNO3的溶解度为_________________ 。
(2)将t3℃时KCl的饱和溶液70.0g稀释成溶质质量分数为20.0%的KCl溶液,需加水__________ g(精确到0.1g)。查阅相关物质的密度后,在实验室完成该实验通常需要的仪器有烧杯、量筒、___________ (填字母标号)。
A 托盘天平 B 药匙 C 胶头滴管 D 玻璃棒
(3)现有t2℃时KNO3的饱和溶液m1g和KCl的饱和溶液m2g。不考虑水的蒸发,下列关系一定成立的是______________ (填字母标号)。
A 两溶液中溶质的质量分数相等
B 分别降温到t1℃,析出KNO3的质量大于析出KCl的质量
C 分别升温至t3℃,所得溶液中溶质的质量分数相等
D 保持t2℃不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等
(4)若硝酸钾中混有少量的氯化钾,提纯硝酸钾的方法是_______________________ 。
(5)探究温度对溶解度的影响,如图2所示。固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2烧杯中盛放20℃Y的饱和溶液(有少量Y的固体剩余),往试管中滴入适量水,烧杯中固体逐渐消失,写出X与Y可能的组合_________________ 、_________________ 。

(1)t3℃时,KNO3的溶解度为
(2)将t3℃时KCl的饱和溶液70.0g稀释成溶质质量分数为20.0%的KCl溶液,需加水
A 托盘天平 B 药匙 C 胶头滴管 D 玻璃棒
(3)现有t2℃时KNO3的饱和溶液m1g和KCl的饱和溶液m2g。不考虑水的蒸发,下列关系一定成立的是
A 两溶液中溶质的质量分数相等
B 分别降温到t1℃,析出KNO3的质量大于析出KCl的质量
C 分别升温至t3℃,所得溶液中溶质的质量分数相等
D 保持t2℃不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等
(4)若硝酸钾中混有少量的氯化钾,提纯硝酸钾的方法是
(5)探究温度对溶解度的影响,如图2所示。固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2烧杯中盛放20℃Y的饱和溶液(有少量Y的固体剩余),往试管中滴入适量水,烧杯中固体逐渐消失,写出X与Y可能的组合
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是碳酸钠的部分溶解度数据:
(1)同学们配制100g40℃的碳酸钠饱和溶液,溶解时需要用到的玻璃仪器有__________ 。
(2)由表中数据可知,碳酸钠的溶解度随温度的升高__________ 。
(3)如下图,向烧杯内加入某固体物质,试管底部的少量粉末消失,则加入的是__________ (选填“NaOH”或“NH4NO3”)。
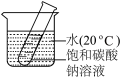
(4)50℃时,将一定量的碳酸钠溶液(含100g水)按图示进行操作:
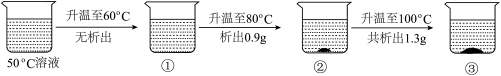
根据实验数据(实验过程中不考虑水蒸发)推测,原溶液的质量是__________ g,烧杯①、②和③中属于饱和溶液的是__________ 。
温度/℃ | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
溶解度/g | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 | 45.1 | 44.7 |
(1)同学们配制100g40℃的碳酸钠饱和溶液,溶解时需要用到的玻璃仪器有
(2)由表中数据可知,碳酸钠的溶解度随温度的升高
(3)如下图,向烧杯内加入某固体物质,试管底部的少量粉末消失,则加入的是

(4)50℃时,将一定量的碳酸钠溶液(含100g水)按图示进行操作:

根据实验数据(实验过程中不考虑水蒸发)推测,原溶液的质量是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】NaCl和Na2CO3的溶解度表和溶度曲线如图所示。
______ (填“氢氧化钠”或“硝酸铵”)固体。_______ (填“10-20”“20-30”或“30-40”)℃。
(3)将40℃时等质量的Na2CO3和NaCl饱和溶液降温至t℃,所得溶液中溶质的质量:Na2CO3_______ (填“大于”“小于”或“等于”)NaCl。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2CO3 | 7.0 | 12.2 | 21.8 | 39.7 | 49.0 | |


(3)将40℃时等质量的Na2CO3和NaCl饱和溶液降温至t℃,所得溶液中溶质的质量:Na2CO3
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】硝酸钾和氯化钾的溶解度曲线如图所示,请回答下列问题:

(1)t1℃时,硝酸钾的溶解度为______ 。
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为______ 。
(3)将t3℃时硝酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t2℃,过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是______ 。
A 都是饱和溶液 B 溶质质量a=b C 溶质的质量分数a=b

(1)t1℃时,硝酸钾的溶解度为
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为
(3)将t3℃时硝酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t2℃,过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是
A 都是饱和溶液 B 溶质质量a=b C 溶质的质量分数a=b
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐2】a、b两物质的溶解度曲线如图1所示,请根据图回答:

(1)30℃时,a的溶解度是____ g。
(2)a的溶解度小于b的溶解度的温度范围是_________ 。
(3)如图2所示,现有20℃时等质量的a、b两物质的饱和溶液,试管底部有等质量的a、b剩余,向烧杯的水中加入氢氧化钠固体,则对相关变化判断正确的是____ (不考虑溶剂的蒸发,析出的固体不含水)
A a溶液中溶质质量增多,b溶液中溶质质量减少
B a溶液中溶质质量分数小于b溶液中溶质质量分数
C a溶液中溶剂质量小于b溶液中溶剂质量
D 试管底部a固体的质量小于b固体的质量

(1)30℃时,a的溶解度是
(2)a的溶解度小于b的溶解度的温度范围是
(3)如图2所示,现有20℃时等质量的a、b两物质的饱和溶液,试管底部有等质量的a、b剩余,向烧杯的水中加入氢氧化钠固体,则对相关变化判断正确的是
A a溶液中溶质质量增多,b溶液中溶质质量减少
B a溶液中溶质质量分数小于b溶液中溶质质量分数
C a溶液中溶剂质量小于b溶液中溶剂质量
D 试管底部a固体的质量小于b固体的质量
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐1】20℃时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量,绘制成如图所示的斜线,回答下列问题:

(1)20℃时,该固体物质的溶解度为____________ 。
(2)C点所对应的溶液是____________ (填“饱和溶液”或“不饱和溶液”)。
(3)若从D点溶液得到A点溶液,需增加该溶质___________ g。
(4)图中四点所对应的溶液质量分数大小关系为_________________ 。

(1)20℃时,该固体物质的溶解度为
(2)C点所对应的溶液是
(3)若从D点溶液得到A点溶液,需增加该溶质
(4)图中四点所对应的溶液质量分数大小关系为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】 和
和 的溶解度曲线如图1所示;某化学兴趣小组同学进行了如图2所示实验(忽略水的损失)。根据图示回答下列问题。
的溶解度曲线如图1所示;某化学兴趣小组同学进行了如图2所示实验(忽略水的损失)。根据图示回答下列问题。 时,
时, 的溶解度是
的溶解度是______ g。
(2)烧杯②中的 溶液是
溶液是______ (填“饱和”或“不饱和”)溶液。烧杯④中析出固体的质量是______ g。
(3)下列有关说法正确的是______。
 和
和 的溶解度曲线如图1所示;某化学兴趣小组同学进行了如图2所示实验(忽略水的损失)。根据图示回答下列问题。
的溶解度曲线如图1所示;某化学兴趣小组同学进行了如图2所示实验(忽略水的损失)。根据图示回答下列问题。
 时,
时, 的溶解度是
的溶解度是(2)烧杯②中的
 溶液是
溶液是(3)下列有关说法正确的是______。
A. 固体中含有少量 固体中含有少量 ,可用降温结晶的方法提纯 ,可用降温结晶的方法提纯 |
B.分别将 时 时 和 和 的饱和溶液升温至 的饱和溶液升温至 ,所得溶液中 ,所得溶液中 的质量分数更大 的质量分数更大 |
C. 时,分别用两种固体配制质量相等的饱和溶液, 时,分别用两种固体配制质量相等的饱和溶液, 中加水更多 中加水更多 |
您最近一年使用:0次



 时,将15g氯化钠固体加入50g水中充分溶解,可得到该温度下氯化钠的
时,将15g氯化钠固体加入50g水中充分溶解,可得到该温度下氯化钠的

