金属在生产、生活中应用广泛,金属的回收利用有利于保护环境、节约资源。
(1)用体温计测量体温时,水银柱会上升。用微观知识解释产生该现象的原因________ 。
(2)我国古代典籍中有“银针验毒”的记载。“银针验毒”的反应原理之一是:4Ag+2H2S+O2=2X+2H2O,X的化学式为________ 。
(3)钢窗表面喷漆不仅美观,而且可有效防止铁与________ 接触而生锈。
(4)某工厂欲从溶质是AgNO3和Cu(NO3)2的生产废液中回收Ag和Cu.实验员取样,向其中加入一定量的锌,充分反应后过滤,得到滤渣和滤液。
①若所得滤液为蓝色,则滤液中一定含有金属离子________ (填离子符号)。
②若向所得滤渣中加入一定量稀硫酸产生气泡,则滤液中的溶质有_______ (填化学式)。
(1)用体温计测量体温时,水银柱会上升。用微观知识解释产生该现象的原因
(2)我国古代典籍中有“银针验毒”的记载。“银针验毒”的反应原理之一是:4Ag+2H2S+O2=2X+2H2O,X的化学式为
(3)钢窗表面喷漆不仅美观,而且可有效防止铁与
(4)某工厂欲从溶质是AgNO3和Cu(NO3)2的生产废液中回收Ag和Cu.实验员取样,向其中加入一定量的锌,充分反应后过滤,得到滤渣和滤液。
①若所得滤液为蓝色,则滤液中一定含有金属离子
②若向所得滤渣中加入一定量稀硫酸产生气泡,则滤液中的溶质有
更新时间:2022-01-14 08:56:42
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】(1)二氧化氮进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此必须对 含有二氧化氮的废气进行处理。
①可以用 NaOH 溶液吸收:反应的化学方程式如下:2NO2+2NaOH==NaNO2+NaNO3+X,则 X 的化学式 为_______________ 。
②配制 200Kg 溶质质量分数为 5%的 NaOH 溶液,需要溶质质量分数为 20%的 NaOH 溶液___________ Kg,需要加水________________ Kg。
(2)某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,测得 烧杯中溶液 pH 的变化如图所示。
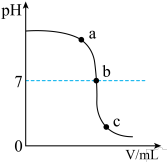
①经测定 a 点溶液中的溶质为__________ 、__________ (填化学式)。
②写出b点硫酸和氢氧化钠溶液反应的化学方程式__________ 。
③取 c 点溶液蒸发得到二种盐,它们是硫酸钠和硫酸氢钠。现若将 15g10%的硫酸氢钠溶液和 10g10% 的氢氧化钡溶液混合,请你写出该反应的化学方程式______________ 。
①可以用 NaOH 溶液吸收:反应的化学方程式如下:2NO2+2NaOH==NaNO2+NaNO3+X,则 X 的化学式 为
②配制 200Kg 溶质质量分数为 5%的 NaOH 溶液,需要溶质质量分数为 20%的 NaOH 溶液
(2)某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,测得 烧杯中溶液 pH 的变化如图所示。

①经测定 a 点溶液中的溶质为
②写出b点硫酸和氢氧化钠溶液反应的化学方程式
③取 c 点溶液蒸发得到二种盐,它们是硫酸钠和硫酸氢钠。现若将 15g10%的硫酸氢钠溶液和 10g10% 的氢氧化钡溶液混合,请你写出该反应的化学方程式
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐2】应用所学知识,分析有关信息,回答下列问题:
(1)已知金属镁可以在某种气体中燃烧,用化学方程式表示为:2Mg+X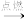 2MgO+C,则X的化学式为
2MgO+C,则X的化学式为_____ ;
(2)镁不仅能与氧气、二氧化碳反应,还能与氮气反应。空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却远大于Mg3N2的质量,请给出合理的解释__________ ;
(3)在密闭容器中,某反应在点燃的条件下发生,涉及甲、乙、丙和丁四种物质,它们的微观示意图和反应前后的质量如下表所示。
①表中的四种物质中,属于氧化物是__________ (填物质序号)。
②上述反应的化学方程式为______________________________________ 。
(1)已知金属镁可以在某种气体中燃烧,用化学方程式表示为:2Mg+X
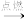 2MgO+C,则X的化学式为
2MgO+C,则X的化学式为(2)镁不仅能与氧气、二氧化碳反应,还能与氮气反应。空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却远大于Mg3N2的质量,请给出合理的解释
(3)在密闭容器中,某反应在点燃的条件下发生,涉及甲、乙、丙和丁四种物质,它们的微观示意图和反应前后的质量如下表所示。
| 物质序号 | 甲 | 乙 | 丙 | 丁 |  |
| 微观示意图 |  |  | 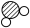 |  | |
| 反应前质量/g | 34 | 50 | 1 | 0 | |
| 反应后质量/g | 0 | 2 | 19 | z |
②上述反应的化学方程式为
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】酸碱度与人体健康
我们知道许多物质具有酸性或碱性。其实,人体的体液也有一定的酸碱性,且其酸碱度保持在一个相对稳定的范围内,这样才能维持人体正常的生命活动。人体血液的量较多,分布广,正常人体血浆pH为7.35﹣7.45。氧气充足时,人体摄取的糖类、脂肪、蛋白质会被彻底氧化分解,最终生成CO2和H2O,在组织细胞与血液之间进行气体交换时,CO2扩散到血液中,会引起血浆的pH略有改变。
人体胃液担负着食物的消化,pH为0.9﹣1.5。20世纪初科学家在人体胃内发现了幽门螺杆菌,幽门螺旋杆菌能引起慢性胃炎,它主要是通过其产生的脲酶分解尿素产生氨而中和人体胃酸,导致人体胃内酸碱失衡,胃液分泌异常。
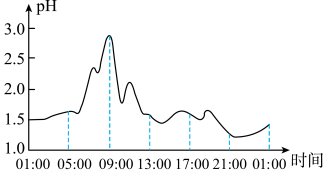
如图是一组胃病患者在空腹状态下24小时胃液pH的变化曲线。科学家发现人体胃液的pH影响人体对药物的吸收,胃液pH低时,胃液分泌多,胃对弱酸性类药物的吸收相对多;胃液pH高时,胃液分泌少,有利于弱碱性类药物的吸收。
依据文章内容回答下列问题:
(1)正常人体血浆呈
(2)CO2扩散到血液,血浆的pH会
(3)脲酶分解尿素反应的化学方程式为CO(NH2)2+H2O
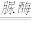 X+2NH3↑,则X的化学式
X+2NH3↑,则X的化学式(4)分析上图,患者服用含氢氧化铝的胃药时,最适宜的用药时间为
(5)下列说法正确的是
A.胃酸能帮助消化食物,胃酸分泌越多越有利于人体健康
B.患者的用药时间也会影响到药效
C.患者在上午九点左右服用弱酸性类药物时吸收最好
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】从微观角度回答下列问题。
(1)未盖紧瓶盖的酒精体积会减少;
(2)一壶水烧开后,壶盖会被顶开;
(3)液态的氢气和气态的氢气都能燃烧。
(1)未盖紧瓶盖的酒精体积会减少;
(2)一壶水烧开后,壶盖会被顶开;
(3)液态的氢气和气态的氢气都能燃烧。
您最近一年使用:0次
【推荐2】“砂锅鱼头”汤鲜汁浓,其烹饪方法为:将鱼头下油锅煎黄后,放入砂锅中加适量食盐、葱段、生姜、香菜、矿泉水等,在火上煨煮数小时即成。
(1)鱼头中的蛋白质进入人体后会逐步分解成被人体吸收的________ 。
(2)用洗洁精清洗油腻的砂锅是利用洗洁精的_______ 作用。
(3)用液化气灶煨制砂锅鱼头时,砂锅外壁出现黑灰,此时可将灶具的进风口_______ (填“调大”或“调小”)。液化气的主要成分之一是丙烷(C3H8),丙烷完全燃烧的化学方程式________ 。
(4)使用液化气灶一定要注意安全,如果液化气一旦泄漏,遇到明火就可能发生爆炸。从微观角度解释发生爆炸的原因是_______ 。
(1)鱼头中的蛋白质进入人体后会逐步分解成被人体吸收的
(2)用洗洁精清洗油腻的砂锅是利用洗洁精的
(3)用液化气灶煨制砂锅鱼头时,砂锅外壁出现黑灰,此时可将灶具的进风口
(4)使用液化气灶一定要注意安全,如果液化气一旦泄漏,遇到明火就可能发生爆炸。从微观角度解释发生爆炸的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】附加题:
(1).将一定量的锌粉加入硫酸亚铁、硫酸铜和硫酸镁的混合溶液中,过一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述正确的是____________
①滤渣中一定含有锌
②滤渣中一定含有铜,可能含有锌
③向滤渣中加入一定量的稀盐酸,最后溶液一定变成浅绿色
④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色
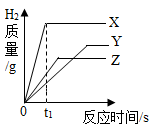
(2). 将等质量、颗粒大小相同的X、Y、Z三种金属分别投入到相同浓度的足量的稀硫酸中,生成氢气的质量与时间的关系如图所示。已知它们在化合物中均显+2价,则下列说法正确的是__________
A 在时间为t1时,生成氢气的质量为:X>Z>Y
B 金属活动性:X>Z>Y
C 相对原子质量:X>Y>Z
D X、Y和Z可能分别是常见金属中的Mg、Fe、Zn
(1).将一定量的锌粉加入硫酸亚铁、硫酸铜和硫酸镁的混合溶液中,过一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述正确的是
①滤渣中一定含有锌
②滤渣中一定含有铜,可能含有锌
③向滤渣中加入一定量的稀盐酸,最后溶液一定变成浅绿色
④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色
(2). 将等质量、颗粒大小相同的X、Y、Z三种金属分别投入到相同浓度的足量的稀硫酸中,生成氢气的质量与时间的关系如图所示。已知它们在化合物中均显+2价,则下列说法正确的是

A 在时间为t1时,生成氢气的质量为:X>Z>Y
B 金属活动性:X>Z>Y
C 相对原子质量:X>Y>Z
D X、Y和Z可能分别是常见金属中的Mg、Fe、Zn
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】取一定量的Zn放入到Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,得到固体和蓝色滤液。固体中一定存在的金属为_______ (填化学式);写出该过程中一定发生的反应的化学方程式_______ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】2020年11月28日8时30分许,一阵汽笛声响,创造了10909米中国载人深潜新纪录的“奋斗者”号胜利返航。最新的“奋斗者”号载人潜水器采用了安全稳定、动力强劲的能源系统,最引人注目的是中国科学院金属研究所钛合金团队采用自主发明的Ti62A钛合金新材料,为“奋斗者”号建造了世界最大、搭载人数最多的潜水器载人舱球壳。根据你的所学知识回答:
(1) 下列能源不属于新能源的是______ (填序号)
A.氢能 B.核能 C.石油 D.风能
(2) 下列钛合金与金属钛的性能对比中说法错误的是______ (填序号)
A.钛合金的强度更大 B.钛合金的硬度更小
C.钛合金的熔点更高 D.钛合金的抗腐蚀性能更优良
(3)已知金属钛的活动性在镁和氢之间,钛在化合物中通常显+2价。请你设计实验证明钛和铜的金属活动性,实验步骤为______ ;反应的化学方程式为______ 。
(1) 下列能源不属于新能源的是
A.氢能 B.核能 C.石油 D.风能
(2) 下列钛合金与金属钛的性能对比中说法错误的是
A.钛合金的强度更大 B.钛合金的硬度更小
C.钛合金的熔点更高 D.钛合金的抗腐蚀性能更优良
(3)已知金属钛的活动性在镁和氢之间,钛在化合物中通常显+2价。请你设计实验证明钛和铜的金属活动性,实验步骤为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属在生活、生产中有着广泛的应用,种类繁多的金属材料已成为社会发展的重要物质基础。做饭时使用的铁锅主要利用了铁的______ 性。农业生产中的铁质具容易生锈,可用稀盐酸除去,其化学方程式可表示为______ ,写出工业生产者防止机器生锈的一种方法______ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】随着首艘国产航母山东舰正式入列,中国海军正式迈入双航母时代。
(1)建造航母用到了钛合金,构成金属钛的粒子是______ (填“原子”、“分子” 或“离子”)。
(2)舰载机发动机叶片使用钛合金的优点是______ (填序号)。
a密度小 b熔点低 c强度小
(3)航母外壳用涂料覆盖,是为了防止钢铁材料与______ 接触而锈蚀。
(4)建造航母时,常用氮气或稀有气体作焊接金属保护气,因为它们的化学性质______ 。
(5)某合金中含有金属钪(Sc)。相同条件下,取相同状态的金属钪和锌分别与相同浓度的盐酸反应,钪产生气泡速率明显更快。根据上述结论,下列说法正确的是______ (填序号)。
a将Sc投入CuSO4溶液中有红色物质析出
b仅用Fe(NO3)2溶液、Sc(NO3)3溶液和Ag能验证钪和铁的活动性强弱
c仅用Fe、Sc、稀H2SO4溶液能验证钪和铁的活动性强弱
(6)已知金属钪(Sc)与稀盐酸发生置换反应,生成+3价化合物。写出该反应的化学方程式______ 。
(1)建造航母用到了钛合金,构成金属钛的粒子是
(2)舰载机发动机叶片使用钛合金的优点是
a密度小 b熔点低 c强度小
(3)航母外壳用涂料覆盖,是为了防止钢铁材料与
(4)建造航母时,常用氮气或稀有气体作焊接金属保护气,因为它们的化学性质
(5)某合金中含有金属钪(Sc)。相同条件下,取相同状态的金属钪和锌分别与相同浓度的盐酸反应,钪产生气泡速率明显更快。根据上述结论,下列说法正确的是
a将Sc投入CuSO4溶液中有红色物质析出
b仅用Fe(NO3)2溶液、Sc(NO3)3溶液和Ag能验证钪和铁的活动性强弱
c仅用Fe、Sc、稀H2SO4溶液能验证钪和铁的活动性强弱
(6)已知金属钪(Sc)与稀盐酸发生置换反应,生成+3价化合物。写出该反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属在生活、生产中应用广泛。
(1)日常生活中,手机的充电器插头是运用了金属的___________ 性。生铁和钢相比较,含碳量较高的是___________ 。
(2)世界上每年因被腐蚀而报废的金属设备和材料相当于年产量的20%~40%。金属的腐蚀给人类带来了巨大的损失。铁制品的锈蚀主要是铁与空气中的___________ 、___________ (填名称)发生化学反应,为了防止铁制品锈蚀,可采取的措施有___________ (列举一条)。
(3)我们还可以将已经发生锈蚀的金属进行除锈,具体做法是用稀盐酸将其表面的铁锈除去,生成氯化铁和水,写出此过程的化学方程式:___________ 。
(1)日常生活中,手机的充电器插头是运用了金属的
(2)世界上每年因被腐蚀而报废的金属设备和材料相当于年产量的20%~40%。金属的腐蚀给人类带来了巨大的损失。铁制品的锈蚀主要是铁与空气中的
(3)我们还可以将已经发生锈蚀的金属进行除锈,具体做法是用稀盐酸将其表面的铁锈除去,生成氯化铁和水,写出此过程的化学方程式:
您最近一年使用:0次




