制取气体是初中化学实验的重要内容。
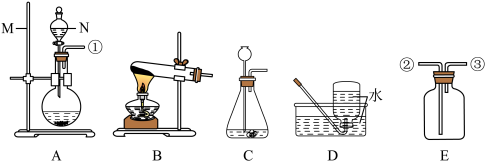
(1)仪器M的名称是_____ 。
(2)实验室选用B装置制备氧气,其反应的化学方程式为_____ 。
(3)C装置中的一处明显错误为_____ 。
(4)某气体只能用D装置收集,则该气体具有的性质为_____ (填序号)。
a.能与水反应 b.能与空气反应 c.密度与空气接近
(5)若用A、E装置制取H2,反应的化学方程式为______ 按气体流向,导管口连接顺序为___ (填序号)

(1)仪器M的名称是
(2)实验室选用B装置制备氧气,其反应的化学方程式为
(3)C装置中的一处明显错误为
(4)某气体只能用D装置收集,则该气体具有的性质为
a.能与水反应 b.能与空气反应 c.密度与空气接近
(5)若用A、E装置制取H2,反应的化学方程式为
更新时间:2022-02-07 15:41:14
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
【推荐1】图中A-G表示初中化学常见的物质,A、B、G为氧化物,其中A和B的组成元素相同,C、D、E和F为单质,其中F为红色固体;图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
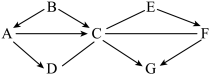
(1)C的化学式为____________ ,G的化学式为____________ 。
(2)写出E→F反应的化学方程式_______________________ 。
(3)A和B的组成元素相同,但是其化学性质不同的原因是__________________ 。

(1)C的化学式为
(2)写出E→F反应的化学方程式
(3)A和B的组成元素相同,但是其化学性质不同的原因是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】“我们比历史上任何时期都更需要建设世界科技强国!”习近平同志在两院院士大会上再次强调了建设世界科技强国的奋斗目标,为我们大力发展科学技术指明了方向。“科技梦”助推“中国梦”,都离不开化学。

(1)北斗导航卫星系统用铷原子钟提供精确时间。铷元素在元素周期表中的相关信息及原子结构示意图如图,则氯化铷的化学式为______ 。
(2)2021年3月,我国两会通过的“十四五”规划纲要,提出了力争2060年前实现“碳中和”的目标。目前科学家已将从空气中捕获的二氧化碳与氢气混合后,在高温条件下用金属钌催化将其转化为新能源甲醇(CH3OH),同时有水生成。则该反应的化学方程式为______ 。
(3)抗击新冠肺炎(2019-nCoV)疫情期间,我国政府颁布了公共场所必须戴口罩的通知,生产N95口罩的主要原料是聚丙烯,它属于______ (填“金属材料“或“合成材料”)。
(4)某工厂的废水中含有Mg2+、Fe2+、Cu2+、Ag+等阳离子,某化学兴趣小组的同学取该工厂废水样品进行下列实验。

①若a=b,则滤液中一定含有的阳离子是______ (填离子符号)。
②若向滤渣中加入稀盐酸,有气泡产生,则滤渣中一定含有______ (填化学式)。
(5)烧杯中盛有一定质量、温度为80℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。
若不考虑水蒸发对实验的影响,请回答下列问题。
①65℃时,该溶液是否为饱和溶液?______ (填“是”、“否”或“无法判断”)。
②将40℃时接近饱和的M溶液变成饱和溶液,下列方法中一定能达到目的有______ 。
a.升温;b.降温;c.加溶质M;d.加另一种固体N;e.恒温蒸发水;f.与40℃时M的饱和溶液混合。

(1)北斗导航卫星系统用铷原子钟提供精确时间。铷元素在元素周期表中的相关信息及原子结构示意图如图,则氯化铷的化学式为
(2)2021年3月,我国两会通过的“十四五”规划纲要,提出了力争2060年前实现“碳中和”的目标。目前科学家已将从空气中捕获的二氧化碳与氢气混合后,在高温条件下用金属钌催化将其转化为新能源甲醇(CH3OH),同时有水生成。则该反应的化学方程式为
(3)抗击新冠肺炎(2019-nCoV)疫情期间,我国政府颁布了公共场所必须戴口罩的通知,生产N95口罩的主要原料是聚丙烯,它属于
(4)某工厂的废水中含有Mg2+、Fe2+、Cu2+、Ag+等阳离子,某化学兴趣小组的同学取该工厂废水样品进行下列实验。

①若a=b,则滤液中一定含有的阳离子是
②若向滤渣中加入稀盐酸,有气泡产生,则滤渣中一定含有
(5)烧杯中盛有一定质量、温度为80℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。
| 溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
| 析出固体M的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
①65℃时,该溶液是否为饱和溶液?
②将40℃时接近饱和的M溶液变成饱和溶液,下列方法中一定能达到目的有
a.升温;b.降温;c.加溶质M;d.加另一种固体N;e.恒温蒸发水;f.与40℃时M的饱和溶液混合。
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
解题方法
【推荐1】现有以下四个化学反应(其反应条件已省略),其中A、B、C、D、、E、F、H、I为初中常见的九种物质。①A→B+C ②D→E+C ③F+C→G ④H+C→I;已知:B物质是生活中最常见的液态物质;E物质中有一种原子所形成的离子带一个单位的负电荷;反应③发生时会有明亮的蓝紫色的火焰;反应④的生成物I为黑色固体。请回答
(1)写出下列物质的化学符号:A_________ ,C_________
(2)写出反应②的文字表达式_____________
(1)写出下列物质的化学符号:A
(2)写出反应②的文字表达式
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】将氯酸钾与二氧化锰的混合物31g装入大试管中,加热到不再产生气体为止,冷却后得到21.4g固体物质。请你回答下列问题:
(1)写出生成气体的化学方程式_______ 。
(2)生成氧气的质量为_______ g。
(3)根据氧气的质量列出求解参加反应的氯酸钾的质量(x)的比例式_______ 。
(4)生成的氯化钾的质量为_______ 。
(5)若加热到产生4.8克氧气后就停止加热,“停止加热后氯酸钾就不再分解”试管中各固体质量的具体变化情况为_______ 。
(1)写出生成气体的化学方程式
(2)生成氧气的质量为
(3)根据氧气的质量列出求解参加反应的氯酸钾的质量(x)的比例式
(4)生成的氯化钾的质量为
(5)若加热到产生4.8克氧气后就停止加热,“停止加热后氯酸钾就不再分解”试管中各固体质量的具体变化情况为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】利用图1装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中H2O2的溶质质量分数为3%,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比。反应放热忽略不计。)

(1)写出装置中发生反应的文字表达式:______ ,MnO2在此反应前后______ 和______ 不发生改变。
(2)图2是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出______ 。
(3)当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图3所示的曲线。曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求。在此实验条件下,若MnO2的质量有4克(一药匙),就能使如图4______ (选填字母)烧杯中所装的3%H2O2溶液,其分解速度最接近实验要求。
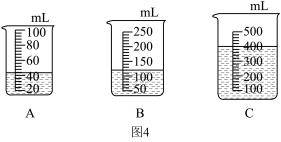
(4)某同学探究了影响双氧水分解速度的某种因素。实验数据记录如下:
本实验中,测量O2体积的装置是图5中的______ (填编号)。
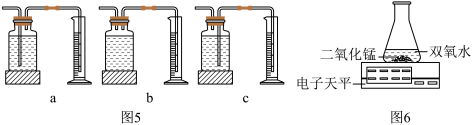
实验结论:在相同条件下,______ ,双氧水分解得越快。丙用图6装置进行实验,通过比较______ 也能达到实验目的。

(1)写出装置中发生反应的文字表达式:
(2)图2是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出
(3)当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图3所示的曲线。曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求。在此实验条件下,若MnO2的质量有4克(一药匙),就能使如图4

(4)某同学探究了影响双氧水分解速度的某种因素。实验数据记录如下:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |

实验结论:在相同条件下,
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】请根据下列实验装置图回答问题:

(1)仪器a的名称是_____ .
(2)若用B装置制氧气,反应的化学方程式是_____ .
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷.甲烷的制取和收集装置应选择_____ ,请写出甲烷完全燃烧的化学方程式_____ .

(1)仪器a的名称是
(2)若用B装置制氧气,反应的化学方程式是
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷.甲烷的制取和收集装置应选择
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,再用一氧化碳还原氧化铜粉末的实验装置如图所示。
甲酸和浓硫酸混合制备CO的方程式为 。
。
(1)装置A和装置B中浓硫酸的作用____ (填“相同”或“不同”),B中浓硫酸的作用是___ 。
(2)装置C中观察到的实验现象是______ 。
(3)装置E____ (填“能”或“不能”)用来检验装置D吸收二氧化碳是否完全,理由是____ 。
(4)装置F和G是对实验中尾气的处理,导管接口的顺序为a→______ →______ →e。
(5)用下图装置,制一氧化碳并还原氧化铜。为了保证实验安全,在进行实验操作时,应该先______ (填“滴加甲酸溶液”或“点燃酒精灯”)。为了防止污染空气,在c处应该进行尾气处理,可以在c处______ 。______ 。

甲酸和浓硫酸混合制备CO的方程式为
 。
。(1)装置A和装置B中浓硫酸的作用
(2)装置C中观察到的实验现象是
(3)装置E
(4)装置F和G是对实验中尾气的处理,导管接口的顺序为a→
(5)用下图装置,制一氧化碳并还原氧化铜。为了保证实验安全,在进行实验操作时,应该先

您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】氧气在生活、生产中应用广泛,制取氧气的方法也多种多样。
Ⅰ.氧气的应用
(1)人的呼吸离不开氧气,给病人输氧时往往会看到类似装置如图(甲),该装置连接病人端端口相当于实验室装置图(乙)中的_______ (填“a”或“b”)端,该装置盛半瓶水的作用是______ 。

(2)在钢铁工业上,“富氧空气”一般用作______ (填“燃料”或“炼钢”),“富氧空气”就是氧气与氮气的体积比高于普通空气的气体,下列属于“富氧空气”的是_______ 。
a.1:3 b.1:4 c.1:5
Ⅱ.氧气的制取
(3)工业上采用分离液态空气法制取氧气,主要原理利用液氮和液氧的_______ 不同。
(4)生活中某种便携制氧气机是利用“分子筛”技术。利用分子筛内部均匀微小孔径把空气中的氧分子吸入孔穴而与其他分子分离。制氧过程的微观示意图如图 17 所示(空气其他成分忽略不计)。根据图判断:由“ ”粒子所构成的物质占普通空气的体积分数为
”粒子所构成的物质占普通空气的体积分数为______

(5)潜水器中还可用“氧烛”来快速提供氧气。氧烛中含有氯酸钠(NaClO3)、Al、Fe、Mg等金属粉末(镁 粉、铝粉燃烧会产生白光,生成氧化镁和氧化铝)和催化剂(如图)。

①氧烛放出的氧气来自于上述物质中的______ ,判断的依据是______ ;
②下列说法正确的是______
a.氧烛在使用时可能具有照明的功能
b.氧烛中反应既有分解反应,也有化合反应。
c.使用完后,产氧药块中原物质的质量均减少
(6)实验室制取氧气的方法多种多样。高锰酸钾在加热分解的过程中,可能发生如下二个反应:
a.

 b.
b.


已知:①同温同压下,任何气体的体积之比等于分子个数比。
②在化学反应前后,原子的种类、原子的数目和原子的质量都不变。
在反应 a、b 中,理论上得到相同体积的氧气,需要高锰酸钾的质量多的是______ (填“a”或“b”)。
Ⅰ.氧气的应用
(1)人的呼吸离不开氧气,给病人输氧时往往会看到类似装置如图(甲),该装置连接病人端端口相当于实验室装置图(乙)中的

(2)在钢铁工业上,“富氧空气”一般用作
a.1:3 b.1:4 c.1:5
Ⅱ.氧气的制取
(3)工业上采用分离液态空气法制取氧气,主要原理利用液氮和液氧的
(4)生活中某种便携制氧气机是利用“分子筛”技术。利用分子筛内部均匀微小孔径把空气中的氧分子吸入孔穴而与其他分子分离。制氧过程的微观示意图如图 17 所示(空气其他成分忽略不计)。根据图判断:由“
 ”粒子所构成的物质占普通空气的体积分数为
”粒子所构成的物质占普通空气的体积分数为
(5)潜水器中还可用“氧烛”来快速提供氧气。氧烛中含有氯酸钠(NaClO3)、Al、Fe、Mg等金属粉末(镁 粉、铝粉燃烧会产生白光,生成氧化镁和氧化铝)和催化剂(如图)。

①氧烛放出的氧气来自于上述物质中的
②下列说法正确的是
a.氧烛在使用时可能具有照明的功能
b.氧烛中反应既有分解反应,也有化合反应。
c.使用完后,产氧药块中原物质的质量均减少
(6)实验室制取氧气的方法多种多样。高锰酸钾在加热分解的过程中,可能发生如下二个反应:
a.


 b.
b.


已知:①同温同压下,任何气体的体积之比等于分子个数比。
②在化学反应前后,原子的种类、原子的数目和原子的质量都不变。
在反应 a、b 中,理论上得到相同体积的氧气,需要高锰酸钾的质量多的是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】化学是一门以实验为基础的科学,实验室部分仪器或装置如图。请回答下列问题:

(1)写出仪器的名称:b______ 。
(2)实验室选用高锰酸钾来制取氧气,该反应的化学方程式为______ ;实验室用B装置制取氧气的化学方程式______ ,若用G装置收集氧气,验满的方法是______ 。
(3)实验室常选择装置C制取二氧化碳的反应方程式______ ,相对于B装置,C装置的优点是______ ,下列反应可用该装置制取的是______ (选填序号)。
A.过氧化氢溶液和二氧化锰混合制氧气
B.锌粒和稀硫酸
C.碳酸钠粉末和盐酸反应
(4)已知:氨气是重要的化工原料,可以与二氧化碳在一定条件下合成尿素,同时生成水。氨气是一种有刺激性气味的气体,密度小于空气,极易溶于水,难溶于 。实验室常用浓氨水和氢氧化钠固体在常温下制取氨气,发生装置可以选择图2中
。实验室常用浓氨水和氢氧化钠固体在常温下制取氨气,发生装置可以选择图2中______ ,某同学用如图中G装置收集氨气,应该从______ (填“a”或“b”)通入,实验时还需在装置G后接装置H,装置H的作用是______ 。

(1)写出仪器的名称:b
(2)实验室选用高锰酸钾来制取氧气,该反应的化学方程式为
(3)实验室常选择装置C制取二氧化碳的反应方程式
A.过氧化氢溶液和二氧化锰混合制氧气
B.锌粒和稀硫酸
C.碳酸钠粉末和盐酸反应
(4)已知:氨气是重要的化工原料,可以与二氧化碳在一定条件下合成尿素,同时生成水。氨气是一种有刺激性气味的气体,密度小于空气,极易溶于水,难溶于
 。实验室常用浓氨水和氢氧化钠固体在常温下制取氨气,发生装置可以选择图2中
。实验室常用浓氨水和氢氧化钠固体在常温下制取氨气,发生装置可以选择图2中
您最近一年使用:0次
【推荐3】实验室制取气体时所需的一些装置如图所示。据图回答下列问题:
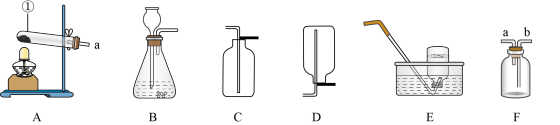
(1)写出指定仪器的名称:①_____ ;
(2)实验室用高锰酸钾为原料制取一瓶较纯净的氧气,应选用的装置组合是_____ (填字母),该反应的化学方程式为_____ ,若用F装置收集氧气,则气体从_____ (填“a”或“b”)进入,检验氧气已经集满的方法是_____ 。
(3)实验室加热氢氧化钙与氯化铵的固体混合物制取氨气,所需的发生装置为_____ (填字母),氨气极易溶于水、密度小于空气,收集装置可用_____ (填字母)或F装置。
(4)某兴趣小组在制取氧气的实验过程中,联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,过氧化钙和水反应能够放出氧气,所以小组决定用过氧化钙为原料制取氧气:
①过氧化钙与水反应_____ (填“适合”或“不适合”)用于实验室制取氧气。
②小林希望加快该反应速率,请你帮他提出合理化建议:_____ 。
③同学们对过氧化钙与水反应的生成物猜想如下:
(a)氢氧化钙和氧气(b)碳酸钙和氧气。
你认为猜想_____ 一定是错误的;请写出过氧化钙与水反应的化学方程式:_____ 。

(1)写出指定仪器的名称:①
(2)实验室用高锰酸钾为原料制取一瓶较纯净的氧气,应选用的装置组合是
(3)实验室加热氢氧化钙与氯化铵的固体混合物制取氨气,所需的发生装置为
(4)某兴趣小组在制取氧气的实验过程中,联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,过氧化钙和水反应能够放出氧气,所以小组决定用过氧化钙为原料制取氧气:
| 实验装置 | 实验步骤与现象 |
 | ①检查装置气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,振荡试管后仍有少量细小气泡缓慢放出。 |
②小林希望加快该反应速率,请你帮他提出合理化建议:
③同学们对过氧化钙与水反应的生成物猜想如下:
(a)氢氧化钙和氧气(b)碳酸钙和氧气。
你认为猜想
您最近一年使用:0次




