金属防锈是科学研究中的重大课题,某学习小组以铁的锈蚀为项目进行探究。
【实验1】探究铁生锈的条件
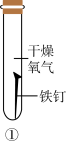
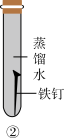
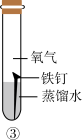
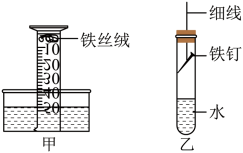
(1)如图所示,取三根洁净无锈的铁钉,分别放置在三个不同环境中,一周后铁钉生锈情况记录如下。
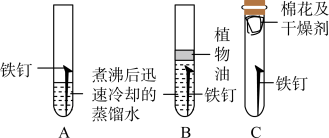
①对比实验______ (填序号),可以得出铁生锈与水有关。
②由上述实验可知,铁生锈的条件是______ 。
③下列环境中的铁制品最容易生锈的是______ (填字母序号)。
A未擦干的铁锅 B.涂油漆的栏杆 C.盛水的不锈钢水杯
【实验2】
(2)该小组用图甲装置再次进行探究铁的锈蚀的实验,起始时量筒内水面处于50mL刻度处,之后水面缓慢上升。几天后水面最终处于约______ (填“40”或“10”)mL刻度处,原因是______ 。
【拓展实验3】
(3)小强同学取铁钉用砂纸打磨,称其质量,按图乙安装装置,放置3天,再取出铁钉称量。
①在不同温度下重复上述实验,得到铁钉质量增加情况如下表。小强同学的实验是探究______ 因素对铁钉锈蚀快慢的影响,结论是______ 。
②有同学认为小强的实验未能真实反映50℃以后铁钉锈蚀的快慢,理由是50℃以后铁钉质量没有变化。请分析铁钉质量没有变化的可能原因______ ,改进实验方案证明你的分析______ 。
【实验1】探究铁生锈的条件
(1)如图所示,取三根洁净无锈的铁钉,分别放置在三个不同环境中,一周后铁钉生锈情况记录如下。

| 实验 | A | B | C |
| 现象 | 在液面附近,铁钉生锈严重 | 铁钉无明显变化 | 铁钉无明显变化 |
②由上述实验可知,铁生锈的条件是
③下列环境中的铁制品最容易生锈的是
A未擦干的铁锅 B.涂油漆的栏杆 C.盛水的不锈钢水杯
【实验2】
(2)该小组用图甲装置再次进行探究铁的锈蚀的实验,起始时量筒内水面处于50mL刻度处,之后水面缓慢上升。几天后水面最终处于约

【拓展实验3】
(3)小强同学取铁钉用砂纸打磨,称其质量,按图乙安装装置,放置3天,再取出铁钉称量。
①在不同温度下重复上述实验,得到铁钉质量增加情况如下表。小强同学的实验是探究
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 铁钉质量增加/g | 0.02 | 0.04 | 0.08 | 0.16 | 0.18 | 0.18 | 0.18 |
更新时间:2022-02-12 15:56:58
|
相似题推荐
实验题
|
适中
(0.65)
【推荐1】某化学实验小组对铁的燃烧和锈蚀进行如下探究:
(1)探究一:铁丝燃烧
如图所示,取3根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端系上粗铜丝,另一端系一根火柴,点燃火柴待快燃尽时,分别插入充满氧气的集气瓶中,观察到:Ⅰ、Ⅱ中铁丝都剧烈燃烧,且Ⅱ中铁丝燃烧比I中的更剧烈;Ⅲ中铁丝没有燃烧.
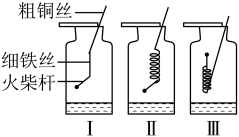
①集气瓶中加入少量水的作用:_________________________ 。
②Ⅲ中铁丝不能燃烧的原因是__________ 。
③分析Ⅱ中铁丝燃烧比Ⅰ中更剧烈的原因_________ (填字母序号)
A、II中铁丝绕成螺旋状,与氧气接触面积增大,反应更充分
B 、II中铁丝绕成螺旋状,能积聚热量,提高温度,对未然部分进行预热
C、II中铁丝绕成螺旋状,提高了铁丝的着火点
(2)探究二:铁粉腐蚀的条件
如图所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进广口瓶(容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数.记录起始和最终量筒的读数以及所需时间如下表
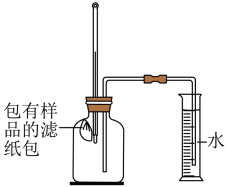
Ⅰ实验①和②对比说明NaCl可以 ___________ (填“加快”或“减慢”)铁粉锈蚀的速率;
Ⅱ实验开始后,广口瓶内温度有所上升,说明铁粉的锈蚀过程是_____ (填“放”或“吸”)热过程;
Ⅲ实验①和③是探究碳对铁粉锈蚀速率的影响,请在表格空白处填写实验③的样品组成___________ ;
Ⅳ该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_________ %(精确到0.1%),该实验结果出现误差的原因 ____________ (选填字母序号)
A、滤纸包占有一定体积;B、量筒中的水蒸发了一部分C、样品中药品少,没把瓶中的氧气耗完
(1)探究一:铁丝燃烧
如图所示,取3根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端系上粗铜丝,另一端系一根火柴,点燃火柴待快燃尽时,分别插入充满氧气的集气瓶中,观察到:Ⅰ、Ⅱ中铁丝都剧烈燃烧,且Ⅱ中铁丝燃烧比I中的更剧烈;Ⅲ中铁丝没有燃烧.

①集气瓶中加入少量水的作用:
②Ⅲ中铁丝不能燃烧的原因是
③分析Ⅱ中铁丝燃烧比Ⅰ中更剧烈的原因
A、II中铁丝绕成螺旋状,与氧气接触面积增大,反应更充分
B 、II中铁丝绕成螺旋状,能积聚热量,提高温度,对未然部分进行预热
C、II中铁丝绕成螺旋状,提高了铁丝的着火点
(2)探究二:铁粉腐蚀的条件
如图所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进广口瓶(容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数.记录起始和最终量筒的读数以及所需时间如下表

| 实验 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| ① | 1g铁粉、0.2g碳、10滴水 | 100 | 72 | 约120 |
| ② | 1g铁粉、0.2g碳、10滴水和少量NaCl | 100 | 72 | 约70 |
| ③ | _______ |
Ⅱ实验开始后,广口瓶内温度有所上升,说明铁粉的锈蚀过程是
Ⅲ实验①和③是探究碳对铁粉锈蚀速率的影响,请在表格空白处填写实验③的样品组成
Ⅳ该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是
A、滤纸包占有一定体积;B、量筒中的水蒸发了一部分C、样品中药品少,没把瓶中的氧气耗完
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】如图是“空气中氧气含量的测定”的实验。甲生设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷熄灭,集气瓶冷却到室温,打开弹簧夹,水进入集气瓶。回答下列问题:
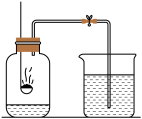
(1)实验过程中,观察到的主要现象是_____________ ;____________ 。
(2)乙生用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差(进入集气瓶的水的体积小于集气瓶内空气容积的1/5)。其操作上的原因可能是(答两种)______________ 、_____________ 。
(3)丙生也设计了一个实验方案,装置和操作同上,只不过用木炭代替了红磷。当木炭停止燃烧,集气瓶冷却至室温,打开弹簧夹后,水能否进入集气瓶?___________ ,其理由是________________ 。

(1)实验过程中,观察到的主要现象是
(2)乙生用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差(进入集气瓶的水的体积小于集气瓶内空气容积的1/5)。其操作上的原因可能是(答两种)
(3)丙生也设计了一个实验方案,装置和操作同上,只不过用木炭代替了红磷。当木炭停止燃烧,集气瓶冷却至室温,打开弹簧夹后,水能否进入集气瓶?
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐3】某兴趣小组的同学选用了40mL的试管作反应容器(如图)和量程体积足够大且润滑效果很好的针筒注射器,将足量的白磷(40℃时就可以燃烧,燃烧产物与红磷相同)放入试管后,用橡皮塞塞紧试管,并夹紧弹簧夹。用酒精灯加热白磷,燃烧结束后,等到试管冷却后松开弹簧夹,观察现象。
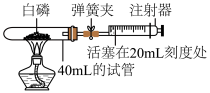
①正式开始实验前,该兴趣小组同学打开弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到活塞返回至20mL刻度处。该操作的主要目的是实验前要检查__________________ 。
②实验中,在松开弹簧夹前,大试管中可以观察到白磷燃烧时的现象____________ ,此时反应文字表达式_______________ 。
③实验后,理论上可以观察到针筒活塞会从原来的20mL刻度处慢慢向左移到约_________ 处。
④下列实验操作,对实验结果几乎没有影响的是_________ 。
A装置有点漏气 B白磷的量不足 C用干燥的红磷代替白磷做实验
⑤实验结束后发现针筒活塞停在14mL处,则测得空气中氧气体积分数为________ 。

①正式开始实验前,该兴趣小组同学打开弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到活塞返回至20mL刻度处。该操作的主要目的是实验前要检查
②实验中,在松开弹簧夹前,大试管中可以观察到白磷燃烧时的现象
③实验后,理论上可以观察到针筒活塞会从原来的20mL刻度处慢慢向左移到约
④下列实验操作,对实验结果几乎没有影响的是
A装置有点漏气 B白磷的量不足 C用干燥的红磷代替白磷做实验
⑤实验结束后发现针筒活塞停在14mL处,则测得空气中氧气体积分数为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】同学们学习了金属的有关知识后,为探究学习金属的物理性质和化学性质,在实验室设计并完成了如下实验。
实验方法:取适量的稀盐酸倒入装有生锈铁钉的试管中(稀盐酸浸没铁钉即可)。
(1)实验原理:_____ (用化学方程式表示)。
(2)实验现象:_____ 。
实验结论:盐酸可以去除铁锈。
【反思与交流】
(3)小原发现若将生锈的铁钉长时间浸泡在盐酸中,会观察到_____ ,其原因是_____ 。
(4)除锈后的铁钉,为防止其再次生锈,可采用的保存方法是_____ (写1点)。
实验方法:取适量的稀盐酸倒入装有生锈铁钉的试管中(稀盐酸浸没铁钉即可)。
(1)实验原理:
(2)实验现象:
实验结论:盐酸可以去除铁锈。
【反思与交流】
(3)小原发现若将生锈的铁钉长时间浸泡在盐酸中,会观察到
(4)除锈后的铁钉,为防止其再次生锈,可采用的保存方法是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】化学是一门实用的基础科学,在人类社会的发展历程中起看重要作用。
(1)正确认识物质 人们在实验研究中总结出常见金属的活动性顺序如图
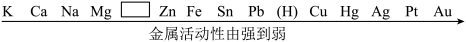
Mg、□、Zn、Fe、Sn、Pt、Au七种金属中,能与稀盐酸(或稀硫酸)发生转换反应的金属有___________ 种。
(2)合理利用资源 化学小组通过实验将生锈铁钉回收处理
【铁钉处理】
小组同学提出,烧杯中的废液也可以回收处理。
【废液处理】同学们查阅相关资料,获知:
a.Fe2O3是一种红棕色粉末,俗称铁红,常用作红色油漆和涂料。
b.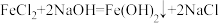
c.
d.不溶性碱受热易分解,生成对应的金属氧化物和水
实验流程:
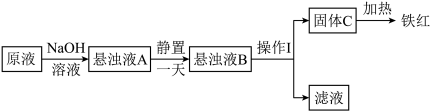
①悬浊液A静置一天的原因是___________ 。
②操作Ⅰ是___________ 。
③写出固体C转化为铁红的化学方程式___________ 。
(1)正确认识物质 人们在实验研究中总结出常见金属的活动性顺序如图
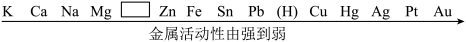
Mg、□、Zn、Fe、Sn、Pt、Au七种金属中,能与稀盐酸(或稀硫酸)发生转换反应的金属有
(2)合理利用资源 化学小组通过实验将生锈铁钉回收处理
【铁钉处理】
| 实验过程 | 实验现象 | 实验原理 | 保存方法 |
| a.向盛有生锈铁钉的烧杯中加入稀盐酸,浸没铁钉 | 溶液由无色变为黄色,铁钉表面有气泡产生,铁锈脱落 | 请写出稀盐酸除铁锈的化学方程式: | 写出一条防止铁制品生锈的方法: |
| b.取出铁钉,洗涤、干燥,妥善保管 | 铁钉呈现银白色 |
【废液处理】同学们查阅相关资料,获知:
a.Fe2O3是一种红棕色粉末,俗称铁红,常用作红色油漆和涂料。
b.
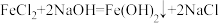
c.

d.不溶性碱受热易分解,生成对应的金属氧化物和水
实验流程:

①悬浊液A静置一天的原因是
②操作Ⅰ是
③写出固体C转化为铁红的化学方程式
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】钢铁的腐蚀是重要研究课题。某校兴趣小组以铁的腐蚀为课题进行如下探究。
[认识铁的腐蚀]
(1)下列环境中的铁制品最容易生锈的是______ (填序号)。
a.未擦干的铁锅 b.涂油漆的栏杆 c.盛水的不锈钢水杯
[探究铁的腐蚀]
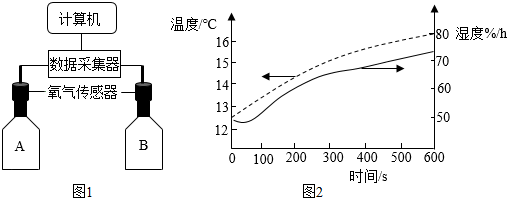
钱老师设计了如图1所示的数字化实验指导同学们对铜铁锈蚀进行探究。用铁粉和碳粉的均匀混合物模拟铁钉成分,用传感器测定试剂瓶内气体的相关数据。
可供选择的药品见表:
(2)铁在空气中锈蚀生成铁锈。铁锈的主要成分是______ (填化学式)。
(3)在A、B两只试剂瓶中依次加入第一组和第二组药品进行实验。
①600s内A瓶中O2含量几乎不变,B瓶中不断减少。实验表明,铁在空气中锈蚀是铁和O2、______ 发生了化学反应。
②将第二组药品中的水改为迅速冷却的沸水,且用量增多至足以完全浸没固体混合物。600s内B瓶中O2含量也略有减少,主要原因是______ 。
(4)为探究食盐对钢铁锈蚀速率的影响,应选择的药品组别是______ (填序号)。
(5)在两只试剂瓶中均加入第二组药品,分别改用温度和湿度传感器测得结果如图2所示。瓶内湿度随时间增大(即水蒸气含量增大),根本原因是______ 。
[处理铁的腐蚀]
(6)除砂纸打磨外,酸也能除锈。将生锈的铁钉放入一定量的稀盐酸中,充分反应,其中涉及的化学方程式有______ 、______ 、2FeCl3+Fe═3FeCl2。
[认识铁的腐蚀]
(1)下列环境中的铁制品最容易生锈的是
a.未擦干的铁锅 b.涂油漆的栏杆 c.盛水的不锈钢水杯
[探究铁的腐蚀]
钱老师设计了如图1所示的数字化实验指导同学们对铜铁锈蚀进行探究。用铁粉和碳粉的均匀混合物模拟铁钉成分,用传感器测定试剂瓶内气体的相关数据。

可供选择的药品见表:
组别 | 药品 | ||||
铁粉/g | 碳粉/g | 水/滴 | 食盐/g | 其他 | |
一 | 5.0 | 0.1 | 0 | 0 | 干燥剂 |
二 | 5.0 | 0.1 | 10 | 0 | 无 |
三 | 5.0 | 0.1 | 10 | 1.0 | 无 |
四 | 5.0 | 0.1 | 0 | 1.0 | 无 |
(3)在A、B两只试剂瓶中依次加入第一组和第二组药品进行实验。
①600s内A瓶中O2含量几乎不变,B瓶中不断减少。实验表明,铁在空气中锈蚀是铁和O2、
②将第二组药品中的水改为迅速冷却的沸水,且用量增多至足以完全浸没固体混合物。600s内B瓶中O2含量也略有减少,主要原因是
(4)为探究食盐对钢铁锈蚀速率的影响,应选择的药品组别是
(5)在两只试剂瓶中均加入第二组药品,分别改用温度和湿度传感器测得结果如图2所示。瓶内湿度随时间增大(即水蒸气含量增大),根本原因是
[处理铁的腐蚀]
(6)除砂纸打磨外,酸也能除锈。将生锈的铁钉放入一定量的稀盐酸中,充分反应,其中涉及的化学方程式有
您最近一年使用:0次
【推荐1】某校开展化学周活动,甲、乙、丙、丁四位同学分别设计并完成了如下实验:
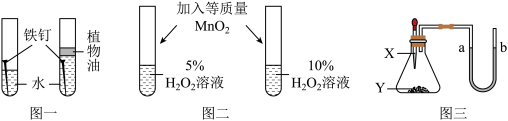
(1)图一为甲同学设计的探究铁生锈的条件实验,由实验可知铁生锈需要的条件是水和_____ ;
(2)图二为乙同学设计的探究二氧化锰对反应速率的影响实验,甲同学认为该实验不能成功,理由是______ ;
(3)图三为丙同学设计的“奇妙的U形管”实验,加入下列哪组物质会出现a处上升b处下降的现象 (填序号)。
(4)丁同学设计了如下实验探究稀盐酸的化学性质:
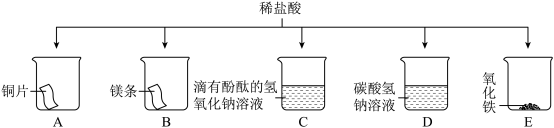
①不发生反应的是_________ (填字母序号);
②有气泡产生的是_________ (填字母序号);
③C中可观察到的现象为________ ;
④E中反应可用于生活中铁锈的去除,其反应现象为________ ,反应的方程式为_______ 。

(1)图一为甲同学设计的探究铁生锈的条件实验,由实验可知铁生锈需要的条件是水和
(2)图二为乙同学设计的探究二氧化锰对反应速率的影响实验,甲同学认为该实验不能成功,理由是
(3)图三为丙同学设计的“奇妙的U形管”实验,加入下列哪组物质会出现a处上升b处下降的现象 (填序号)。
| A.氢氧化钠、水 | B.锌、稀硫酸 | C.硝酸铵、水 |

①不发生反应的是
②有气泡产生的是
③C中可观察到的现象为
④E中反应可用于生活中铁锈的去除,其反应现象为
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
【推荐2】U型玻璃管是常见的化学仪器,在实验中有广泛的应用。
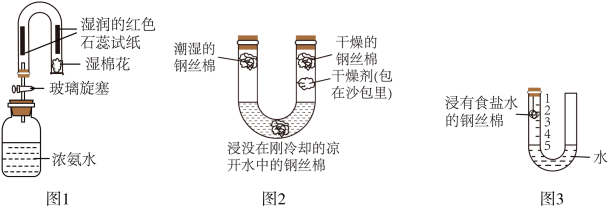
(1)借助U型玻璃管探究微粒的性质,如图1所示,打开玻璃旋塞,观察到湿润的红色石蕊试纸从左到右先后变蓝,该实验说明分子在不停地运动,湿棉花的作用是_________ 。
(2)借助U型玻璃管探究钢铁锈蚀的条件,如图2所示:
①一段时间后潮湿的钢丝棉有明显锈迹,干燥的钢丝棉没有锈迹,此现象说明_______ 。
②实验结束时,细心的同学发现浸没在凉开水中的钢丝棉也有少量锈迹,说明本实验有不完善之处,请利用原有装置提出具体改进方案__________________
(3)借助U型玻璃管粗略测定空气中氧气的体积分数,如图3所示,得出空气中氧气体积分数约为五分之一的实验现象是__________________________ 。

(1)借助U型玻璃管探究微粒的性质,如图1所示,打开玻璃旋塞,观察到湿润的红色石蕊试纸从左到右先后变蓝,该实验说明分子在不停地运动,湿棉花的作用是
(2)借助U型玻璃管探究钢铁锈蚀的条件,如图2所示:
①一段时间后潮湿的钢丝棉有明显锈迹,干燥的钢丝棉没有锈迹,此现象说明
②实验结束时,细心的同学发现浸没在凉开水中的钢丝棉也有少量锈迹,说明本实验有不完善之处,请利用原有装置提出具体改进方案
(3)借助U型玻璃管粗略测定空气中氧气的体积分数,如图3所示,得出空气中氧气体积分数约为五分之一的实验现象是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐3】钢铁的锈蚀及其防护。
(1)“知锈”:铁锈通常为_____ 色固体,其微观结构可用下图中的_____ 反映,区分铁和铁锈的简单物理方法是_____ 。

(2)“探锈”:设计以下实验探究铁发生锈蚀的主要因素。
实验时,试管②中的蒸水必经过煮沸,主要目的是_____ 。对比表格中的试管_____ (填编号),可知水是铁锈蚀的因素之一。
(3)“防锈”:很多学校在校门口摆放的铁质防冲撞栏防锈的方法是_____ 。
(4)“用锈”:某食品脱氧剂可迅速将包装袋内的氧气浓度降到0.01%以下。该脱氧剂中除含有铁粉、活性炭、水等物质外,还含有能促进铁锈蚀的_____ (填化学式)。
(1)“知锈”:铁锈通常为

(2)“探锈”:设计以下实验探究铁发生锈蚀的主要因素。
|
|
|
|
立即观察 | 不生锈 | 不生锈 | 不生锈 |
1天后 | 不生锈 | 不生锈 | 不生锈 |
3天后 | 不生锈 | 不生锈 | 表面有锈迹 |
1周后 | 不生锈 | 不生锈 | 锈蚀明显 |
实验时,试管②中的蒸水必经过煮沸,主要目的是
(3)“防锈”:很多学校在校门口摆放的铁质防冲撞栏防锈的方法是
(4)“用锈”:某食品脱氧剂可迅速将包装袋内的氧气浓度降到0.01%以下。该脱氧剂中除含有铁粉、活性炭、水等物质外,还含有能促进铁锈蚀的
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】在制取CO2的实验中,小雷发现质量相同而粗细不同的大理石与盐酸反应,产生CO2的快慢不同,细颗粒大理石与盐酸反应产生CO2更快。
(1)经思考后,小雷设计了如下实验,请你完成下表:(每次实验用大理石质量1g,盐酸20mL)
(2)写出大理石与稀盐酸反应的化学方程式:_____
(3)该实验收集二氧化碳的装置可选用下图_____ (填字母序号)。植物油的作用是_____ 。
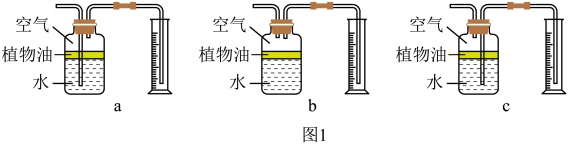
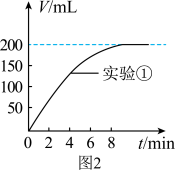
(4)实验①中CO2体积随时间的变化关系如图2所示,请在下图中画出实验②中CO2体积随时间变化关系的预期结果_____ 。
【拓展探究】
(5)影响大理石与盐酸反应快慢除上述因素外,还有_____ (写出1点即可),请设计实验方案:_____ 。
(1)经思考后,小雷设计了如下实验,请你完成下表:(每次实验用大理石质量1g,盐酸20mL)
| 实验序号 | 实验温度(℃) | 大理石颗粒 | 盐酸质量分数(%) | 实验目的 |
| ① | 20 | 粗 | 5 | 实验①②:探究大理石和盐酸的反应速率与大理石颗粒粗细的关系;实验①③:探究大理石和盐酸的反应速率与 |
| ② | 细 | 5 | ||
| ③ | 20 | 粗 | 10 |
(3)该实验收集二氧化碳的装置可选用下图

(4)实验①中CO2体积随时间的变化关系如图2所示,请在下图中画出实验②中CO2体积随时间变化关系的预期结果

【拓展探究】
(5)影响大理石与盐酸反应快慢除上述因素外,还有
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】某校化学兴趣小组在老师指导下,进行了“影响双氧水分解因素”的实验。以下是探究影响化学反应快慢因素的相关数据(常温指20℃;“浓度”指溶质的质量分数)
(1)通过实验①和②对比可知,化学反应快慢与___________ 有关;
(2)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是:温度为___________ ℃,过氧化氢的浓度为___________ ,二氧化锰___________ (填“有”或“无”);
(3)实验中除了量筒外,还需要用到的测量仪器是___________ ;
(4)为完成本实验,收集装置可以选图中的___________ (填序号)。

| 实验 序号 | 过氧化氢溶液溶度% 浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰 用量/g | 氧气体积/mL | 反应所需时间s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
(2)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是:温度为
(3)实验中除了量筒外,还需要用到的测量仪器是
(4)为完成本实验,收集装置可以选图中的

您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组同学发现,除二氧化锰外其他物质也能作氯酸钾分解的催化剂,那么氧化铜是否能作氯酸钾分解的催化剂?于是进行了如下的探究。
提出问题:氧化铜是否能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
设计实验:同学们设计了下面三组实验,实验中“待测数据”是生成相同体积的氧气所需时间 其它可能影响实验的因素均忽略
其它可能影响实验的因素均忽略 。
。
问题讨论:
(1)表中的待测数据是_______ ,实验②中反应的文字表达式是______ ,实验③中x的数值为______ 。
(2)由实验③与实验______ 的“待测数据”相对比,若实验③ “待测数据”更______  填“大”或“小”
填“大”或“小” ,则说明氧化铜能加快氯酸钾的分解速率。
,则说明氧化铜能加快氯酸钾的分解速率。
反思:
(3)若要证明氧化铜是该反应的催化剂,还要设计实验验证它在化学反应前后的______ 和______ 不变。
(4)你认为同学们设计实验②和实验③的对比的目的是_________ 。
提出问题:氧化铜是否能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
设计实验:同学们设计了下面三组实验,实验中“待测数据”是生成相同体积的氧气所需时间
 其它可能影响实验的因素均忽略
其它可能影响实验的因素均忽略 。
。| 实验编号 | 氯酸钾 | 其它物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | 二氧化锰0.5g | |
| ③ | xg | 氧化铜0.5g |
(1)表中的待测数据是
(2)由实验③与实验
 填“大”或“小”
填“大”或“小” ,则说明氧化铜能加快氯酸钾的分解速率。
,则说明氧化铜能加快氯酸钾的分解速率。反思:
(3)若要证明氧化铜是该反应的催化剂,还要设计实验验证它在化学反应前后的
(4)你认为同学们设计实验②和实验③的对比的目的是
您最近一年使用:0次