氯化钠和硝酸钾两种固体的溶解度曲线如图1所示。
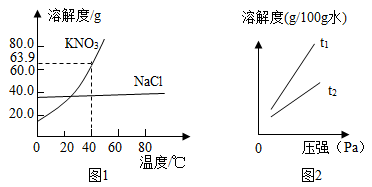
(1)40℃时,将35 g硝酸钾晶体放入50 g水中,充分搅拌后,所得溶液的溶质质量分数为_____ 。(精确到0.1%)。
(2)60℃时,分别将相同质量的NaCl与KNO3饱和溶液降温至20℃,析出晶体质量最大的是_____ 溶液。
(3)若用溶质质量分数为l6%的NaCl溶液和蒸馏水来配制100g溶质质量分数为10%的NaCl溶液。则所需16%的NaCl溶液与蒸馏水的质量比为_____ 。
(4)不同温度下,氧气的溶解度随压强的变化如图2所示,图中t1对应的温度为40℃,则t2对应的温度_____ (填字母)。
A 大于40℃ B 小于40% C 无法确定

(1)40℃时,将35 g硝酸钾晶体放入50 g水中,充分搅拌后,所得溶液的溶质质量分数为
(2)60℃时,分别将相同质量的NaCl与KNO3饱和溶液降温至20℃,析出晶体质量最大的是
(3)若用溶质质量分数为l6%的NaCl溶液和蒸馏水来配制100g溶质质量分数为10%的NaCl溶液。则所需16%的NaCl溶液与蒸馏水的质量比为
(4)不同温度下,氧气的溶解度随压强的变化如图2所示,图中t1对应的温度为40℃,则t2对应的温度
A 大于40℃ B 小于40% C 无法确定
更新时间:2021-01-01 22:36:28
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】下表是三种物质在不同温度时的溶解度,根据表中信息回答问题。
(1)60℃时,氯化钠的溶解度__________ 硝酸钾的溶解度(填“大于”、“小于”或“等于”);
(2)表中某物质的饱和溶液随温度升高析出固体,该物质是____________ ;
(3)向20℃的氢氧化钙和溶液中加入少量生石灰,再冷却至20℃,此时溶液中溶质的质量比加入生石灰前的溶液中溶质的质量___________ (填“增大”、“减小”或“不变”);
(4)混有少量氯化钠的硝酸钾固体,加水配成80℃的硝酸钾饱和溶液,再冷却至20℃,析出晶体并得到溶液。下列有关说法中正确的____________ (填字母序号)。
A析出的晶体中不一定含有硝酸钾
B所得溶液一定是硝酸钾饱和溶液
C上述方法可以将两种物质完全分离
温度/C | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
硝酸钾 | 13.3 | 31.6 | 64.0 | 110.0 | 169.0 | 246.0 | |
氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
(2)表中某物质的饱和溶液随温度升高析出固体,该物质是
(3)向20℃的氢氧化钙和溶液中加入少量生石灰,再冷却至20℃,此时溶液中溶质的质量比加入生石灰前的溶液中溶质的质量
(4)混有少量氯化钠的硝酸钾固体,加水配成80℃的硝酸钾饱和溶液,再冷却至20℃,析出晶体并得到溶液。下列有关说法中正确的
A析出的晶体中不一定含有硝酸钾
B所得溶液一定是硝酸钾饱和溶液
C上述方法可以将两种物质完全分离
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下表是氯化钠和硝酸钾在不同温度下的溶解度(假设硝酸钾与氯化钠同时溶解在水中各自的溶解度不变,实验过程中水分损失忽略不计)。
①硝酸钾和氯化钠的溶解度相同时的温度范围是_______ ;
A 0°C-20°C B 20°C-40°C C 40°C-60°C D 60°C-80°C
②20°C时,将20gKNO3放入50g水中,充分搅拌,所得溶液的质量是_______ ;要进一步提高该溶液的溶质质量分数,可进行的操作是_______ 。
③在80°C的100g水中溶解NaCl和KNO3,进行以下实验,已知溶液a中的硝酸钾恰好饱和:

Ⅰ. 操作1的名称是______ ;
Ⅱ. X=_______ 克,固体C的成分和该成分的质量分别是______ 和________ ;
Ⅲ. 对整个实验过程分析正确的是________ ;
A 40°C-60°C开始析出晶体
B 氯化钠在整个过程中一直保持不饱和状态
C 上述方法不能将氯化钠和硝酸钾完全分离
D 原溶液直接降温结晶,析出硝酸钾的质量不变
| 温度/°C | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 64.0 | 110.0 | 169.0 | 246.0 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
A 0°C-20°C B 20°C-40°C C 40°C-60°C D 60°C-80°C
②20°C时,将20gKNO3放入50g水中,充分搅拌,所得溶液的质量是
③在80°C的100g水中溶解NaCl和KNO3,进行以下实验,已知溶液a中的硝酸钾恰好饱和:

Ⅰ. 操作1的名称是
Ⅱ. X=
Ⅲ. 对整个实验过程分析正确的是
A 40°C-60°C开始析出晶体
B 氯化钠在整个过程中一直保持不饱和状态
C 上述方法不能将氯化钠和硝酸钾完全分离
D 原溶液直接降温结晶,析出硝酸钾的质量不变
您最近一年使用:0次
【推荐1】化学与生产、生活息息相关。
I.水是生命之道
自来水是我国目前主要的生活饮用水.下表是我国生活饮用水的部分标准:
①感官指标表现的是自来水的___________ 性质(填“物理”或“化学”)。
②化学指标中的pH=6.7时,表明自来水呈___________ 性。
③生活可用___________ 来区别硬水和软水,常用___________ 将硬水软化。
Ⅱ.硝酸钾的溶解度曲线如图所示。
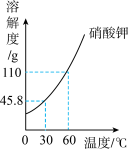
(1)30℃时,硝酸钾的溶解度是______________ 。
(2)60℃时,在200g水中加入120g硝酸钾固体,充分搅拌。
①所得溶液是__________ (填“饱和”或“不饱和”)溶液。
②将上述溶液降温至30℃,可析出硝酸钾晶体_______ g,此时溶液的溶质质量分数________ (填“>”、“=”或“<”)45.8%。
I.水是生命之道
自来水是我国目前主要的生活饮用水.下表是我国生活饮用水的部分标准:
| 项目 | 标准 |
| 感官指标 | 无异味、异臭 |
| 化学指标 | pH6.5﹣8.5,游离氯≥0.3mg/L﹣1,铁<0.3mg/L… |
②化学指标中的pH=6.7时,表明自来水呈
③生活可用
Ⅱ.硝酸钾的溶解度曲线如图所示。

(1)30℃时,硝酸钾的溶解度是
(2)60℃时,在200g水中加入120g硝酸钾固体,充分搅拌。
①所得溶液是
②将上述溶液降温至30℃,可析出硝酸钾晶体
您最近一年使用:0次
【推荐2】硝酸钾和氯化钠在不同温度下的溶解度如下表:
(1)10℃时,硝酸钾的溶解度________ (填“>”“<”或“=”)氯化钠的溶解度。
(2)20℃时,20克氯化钠固体放入50克水中,所得溶液______ (填“是”或“不是”)饱和溶液,溶液的质量为____ 克。
(3)现有硝酸钾和氯化钠的固体混合物146 g,为了得到其中的硝酸钾,设计如图实验:

原混合物中硝酸钾的纯度(质量分数)_____ (列算式即可)。
| 温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 | 100 | |
| 溶解度(g/100g水) | 硝酸钾 | 20. 9 | 31.6 | 45.8 | 64 | 110 | 169 | 246 |
| 氯化钠 | 35. 8 | 36 | 36.3 | 36.4 | 37 | 38.4 | 39.8 | |
(2)20℃时,20克氯化钠固体放入50克水中,所得溶液
(3)现有硝酸钾和氯化钠的固体混合物146 g,为了得到其中的硝酸钾,设计如图实验:

原混合物中硝酸钾的纯度(质量分数)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】甲、乙、丙三种物质的溶解度曲线如图所示(不含结晶水),请回答:
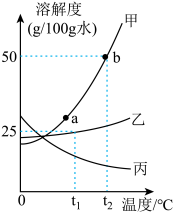
(1)0℃时,甲、乙、丙的溶解度最大的是_____ 。
(2)t2℃时,将30g甲固体加入到50g水中,充分搅拌后的所得溶液是_____ (填“饱和”“不饱和”)溶液。
(3)若甲中含有少量乙,应用_____ 法提纯甲。
(4)等质量的甲、乙、丙三种饱和溶液从t1℃降温至0℃后,溶液中溶质的质量分数由大到小的顺序是_____ 。
(5)若使甲溶液的状态从a点转化为b点,可采取的措施是_____ 。

(1)0℃时,甲、乙、丙的溶解度最大的是
(2)t2℃时,将30g甲固体加入到50g水中,充分搅拌后的所得溶液是
(3)若甲中含有少量乙,应用
(4)等质量的甲、乙、丙三种饱和溶液从t1℃降温至0℃后,溶液中溶质的质量分数由大到小的顺序是
(5)若使甲溶液的状态从a点转化为b点,可采取的措施是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】小明同学在家中自制“汽水”,他在饮料瓶中加入白糖、小苏打和适量果汁,再加入1.5克柠檬酸,立即旋紧瓶盖,摇匀,放入冰箱。半小时后,他就喝到了清凉可口的“汽水”。请回答:
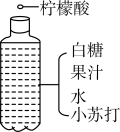
(1)制作“汽水”时加入柠檬酸的目的是什么?_____
(2)小明用的柠檬酸是食品级的添加剂,请你说出该添加剂应有的性质(答一点即可)_____
(3)打开瓶盖时“汽水”为什么会自动溢出?_____

(1)制作“汽水”时加入柠檬酸的目的是什么?
(2)小明用的柠檬酸是食品级的添加剂,请你说出该添加剂应有的性质(答一点即可)
(3)打开瓶盖时“汽水”为什么会自动溢出?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】俗话说:“世界面食在中国,中国面食在山西。”山西面食种类繁多,其中用荞麦面制作猫耳朵面食的制作手艺被国务院授予国家级非物质文化遗产。荞麦含有丰富的膳食纤维,铁、锰、锌的含量比一般谷物丰富,具有很好的营养保健作用。
(1)这里的“铁、锰、锌”是指___________ (选填“原子”“元素”或“单质”)。
(2)荞麦中含有的铁,可以预防的疾病是___________ 。
(3)用笊篱将锅中煮熟的荞麦猫耳朵捞出(如图),这实际上与化学实验操作中___________ (填操作名称)的原理相同。

(4)人喝了碳酸饮料之后会出现打嗝现象,原因是___________ 。
(1)这里的“铁、锰、锌”是指
(2)荞麦中含有的铁,可以预防的疾病是
(3)用笊篱将锅中煮熟的荞麦猫耳朵捞出(如图),这实际上与化学实验操作中

(4)人喝了碳酸饮料之后会出现打嗝现象,原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】化学源于生活又服务于生活:

(1)请用化学知识解释下列问题
①喝了汽水后常常会打嗝,原因是升温使气体溶解度_______
②食物保存在冰箱中不易变质,是因为化学反应速率与_______ 有关。
③塑料属于______ 物品,能把它投进带有 标志的垃圾桶
标志的垃圾桶
④铁元素是人体必需的一种微量元素。食用“加铁酱油”可预防_______ 。
(2)自行车作为常用的代步工具,既轻便灵活,又符合环保要求,右图是一款自行车的示意图。
①所标物质中,属于有机合成材料的是_______ (答出一个即可,下同),属于金属合金的是_______ ,含有的金属元素是_______ 。
②车架刷漆主要是为了防锈,其原理是_______ ;

(1)请用化学知识解释下列问题
①喝了汽水后常常会打嗝,原因是升温使气体溶解度
②食物保存在冰箱中不易变质,是因为化学反应速率与
③塑料属于
 标志的垃圾桶
标志的垃圾桶④铁元素是人体必需的一种微量元素。食用“加铁酱油”可预防
(2)自行车作为常用的代步工具,既轻便灵活,又符合环保要求,右图是一款自行车的示意图。
①所标物质中,属于有机合成材料的是
②车架刷漆主要是为了防锈,其原理是
您最近一年使用:0次
【推荐1】分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:
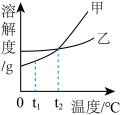
(1)氯化钠的溶解度曲线是_____ (填“甲”或“乙”)。
(2)20℃时,将40gNH4Cl 加入100g 的水中,充分搅拌后得到的是_____ 溶液(填“饱和”或“不饱和”),将上述溶液升温到30℃,该溶液的溶质质量分数为_____ (只列计算式,不需计算结果)。
(3)如图,t1℃时,将两种物质的饱和溶液各100g,分别恒温蒸发5g 水,析出晶体最多的是___ (填“甲”或“乙”)。
(4)计算配制50g 质量分数为3%的NaCl 溶液所需要质量分数为6%的NaCl 溶液的体积,需要用到的数据是_____。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |

(1)氯化钠的溶解度曲线是
(2)20℃时,将40gNH4Cl 加入100g 的水中,充分搅拌后得到的是
(3)如图,t1℃时,将两种物质的饱和溶液各100g,分别恒温蒸发5g 水,析出晶体最多的是
(4)计算配制50g 质量分数为3%的NaCl 溶液所需要质量分数为6%的NaCl 溶液的体积,需要用到的数据是_____。
| A.3%的NaCl 溶液的密度 | B.水的密度 | C.6%的NaCl 溶液的密度 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下表列出了硝酸钾在不同温度时的溶解度.
某兴趣小组做了以下实验:
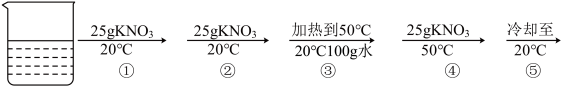
(1)上述溶液中的溶剂是________ ,上述实验过程中得到的溶液一定属于不饱和溶液的是________ (填数字序号),⑤所对应的实验现象是________ .
(2)实验过程中,溶质的质量分数一定相等的是________ (填数字序号).
(3)为了防止水体污染,小组同学提出了如下方案处理实验后的废液: 步骤I:将⑤继续冷却至0℃,过滤,共可回收得到KNO3固体________ g.
步骤II:向滤液中加入________ g水稀释,得到溶质的质量分数为1%的KNO3稀溶液,将此溶液做为化肥使用.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |

(1)上述溶液中的溶剂是
(2)实验过程中,溶质的质量分数一定相等的是
(3)为了防止水体污染,小组同学提出了如下方案处理实验后的废液: 步骤I:将⑤继续冷却至0℃,过滤,共可回收得到KNO3固体
步骤II:向滤液中加入
您最近一年使用:0次

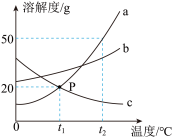
 ℃时物质a的饱和溶液中,溶质与溶剂质量比为
℃时物质a的饱和溶液中,溶质与溶剂质量比为 ℃时,分别在100g水中加入20g的a、b、c,充分搅拌后,所得溶液质量的大小关系是_____(填字母序号)。
℃时,分别在100g水中加入20g的a、b、c,充分搅拌后,所得溶液质量的大小关系是_____(填字母序号)。


