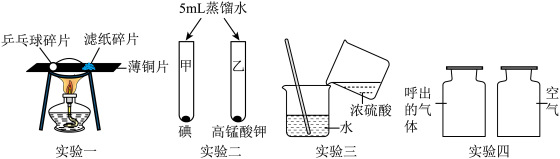
运用所学知识回答问题
(1)盐酸、硫酸是常见的两种酸。①打开装浓盐酸的试剂瓶时,瓶口出现白雾,说明浓盐酸具有_____ 性。②用水稀释浓硫酸时,将______ 并用玻璃棒不断搅拌即可。
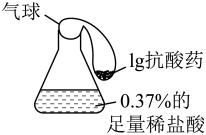
(2)如图是化肥硝酸铵包装袋上的部分说明:

①从说明上可以判断硝酸铵应具有的性质有__________ (填字母)。
A.易溶于水 B.撞击易爆炸 C.受热易分解
②若把硝酸铵溶于水配成溶液并用pH试纸检测溶液酸碱性,发现常温下溶液的pH=6,则该盐溶液呈_____ (填“酸性”、“碱性”或“中性”)。
③硝酸铵与碱反应生成硝酸盐、氨气和水,由于氨气挥发而导致肥效减弱,故施用硝酸铵时,要避免与碱性物质混合使用。写出硝酸铵与熟石灰在加热条件下反应的化学方程式_______ 。
(1)盐酸、硫酸是常见的两种酸。①打开装浓盐酸的试剂瓶时,瓶口出现白雾,说明浓盐酸具有
(2)如图是化肥硝酸铵包装袋上的部分说明:

①从说明上可以判断硝酸铵应具有的性质有
A.易溶于水 B.撞击易爆炸 C.受热易分解
②若把硝酸铵溶于水配成溶液并用pH试纸检测溶液酸碱性,发现常温下溶液的pH=6,则该盐溶液呈
③硝酸铵与碱反应生成硝酸盐、氨气和水,由于氨气挥发而导致肥效减弱,故施用硝酸铵时,要避免与碱性物质混合使用。写出硝酸铵与熟石灰在加热条件下反应的化学方程式
更新时间:2022-04-07 18:54:09
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图1是A、B、C三种物质的溶解度曲线,据图回答:

(1)M点表示的意义是______ 。
(2)t1℃时,30gA物质加入到50g水中不断搅拌形成的溶液质量是______ 。
(3)将t2℃时A、B、C三种物质饱和溶液的降温到t1℃时,所得三种溶液的质量大小关系是______。
(4)如图2所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的______(填字母序号)。

(1)M点表示的意义是
(2)t1℃时,30gA物质加入到50g水中不断搅拌形成的溶液质量是
(3)将t2℃时A、B、C三种物质饱和溶液的降温到t1℃时,所得三种溶液的质量大小关系是______。
| A. A>B>C | B.C>B>A | C.C>A>B | D.无法确定 |
(4)如图2所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的______(填字母序号)。
| A.氢氧化钠固体 | B.生石灰固体 |
| C.硝酸铵固体 | D.浓硫酸 |
| E.冰块 | |
您最近一年使用:0次
【推荐2】浓硫酸具有______ 性和强烈的______ 性,在稀释浓硫酸时,一定要把______ 沿器壁慢慢注入______ 中,并不断搅拌。将生锈的铁钉放入稀盐酸中,一段时间后,铁钉表面变光亮,其间发生的化学反应有______ (用化学方程式表示)。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】硫酸、盐酸都是重要的化工原料。
(1)硫酸在实验室常用作干燥剂,是因为浓硫酸具有________ 性。浓盐酸长期敞口放置在空气中溶质质量分数会逐渐________ (填变大,变小或不变),这是因为浓盐酸具有________ 性。
(2)写出稀硫酸与下列物质反应的化学方程式。
①与铁粉反应:________ 。
②与碳酸钠反应:________ 。
③与氯化钡反应:________ 。
④与氧化铁反应:________ 。
(1)硫酸在实验室常用作干燥剂,是因为浓硫酸具有
(2)写出稀硫酸与下列物质反应的化学方程式。
①与铁粉反应:
②与碳酸钠反应:
③与氯化钡反应:
④与氧化铁反应:
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】分类法是学习化学的重要思想方法。现有下列三组物质:
A.空气、熟石灰、冰水、蔗糖
B.KOH、C2H5OH、Ca(OH)2、NH3.H2O
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
(2)请仿照检验CO2的反应原理,写出SO2与NaOH溶液反应的化学反应方程式________________________ 。
(3)NH4Cl溶液与KOH溶液能够反应,实质是因为它们在水中解离出来的 和OH-结合生成了NH3和H2O。结合发生复分解反应的条件,请回答:Ba(OH)2溶液与Na2SO4溶液能够反应的实质是它们在水中能解离出的
和OH-结合生成了NH3和H2O。结合发生复分解反应的条件,请回答:Ba(OH)2溶液与Na2SO4溶液能够反应的实质是它们在水中能解离出的________________ 结合生成了________________ 。
(4)请依据(3)中获得的启示,判断下列在水溶液中能大量共同存在的一组离子是________ 。
A.H+、OH- B.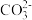 、H+
、H+
C.Cu2+、OH- D.Na+、Cl-
(5)在实验室有一些常识,如:氢氧化钠固体必须密封保存,原因是:__________________________ ,浓硫酸必须密封保存,原因是:__________________ ,如果溅到皮肤上应该先_____________ ,然后再____________________ 。打开浓盐酸瓶盖,瓶口有白雾,原因是:___________________________ 。
A.空气、熟石灰、冰水、蔗糖
B.KOH、C2H5OH、Ca(OH)2、NH3.H2O
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
| 组 别 | A组 | B组 | C组 |
| 分类标准 | 纯净物 | 碱 | |
| 不属于上述分类标准的物质 | 空气 | ② | SO2 |
(3)NH4Cl溶液与KOH溶液能够反应,实质是因为它们在水中解离出来的
 和OH-结合生成了NH3和H2O。结合发生复分解反应的条件,请回答:Ba(OH)2溶液与Na2SO4溶液能够反应的实质是它们在水中能解离出的
和OH-结合生成了NH3和H2O。结合发生复分解反应的条件,请回答:Ba(OH)2溶液与Na2SO4溶液能够反应的实质是它们在水中能解离出的(4)请依据(3)中获得的启示,判断下列在水溶液中能大量共同存在的一组离子是
A.H+、OH- B.
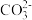 、H+
、H+C.Cu2+、OH- D.Na+、Cl-
(5)在实验室有一些常识,如:氢氧化钠固体必须密封保存,原因是:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】请结合所学知识回答下列问题:
(1)浓盐酸具有______ ,而浓硫酸具有______ 。将浓盐酸和浓硫酸敞口放置一段时间,溶质质量分数都会______ (填“增大”或“减小”或“不变”)。
(2)将一根生锈的铁钉放入稀盐酸中,先观察到_____________________ 现象,过一会儿还可观察到产生气泡的现象,涉及到的化学方程式为:
①____________________________________________ ,
②____________________________________________ 。
(1)浓盐酸具有
(2)将一根生锈的铁钉放入稀盐酸中,先观察到
①
②
您最近一年使用:0次
【推荐1】人体胃腺壁细胞能分泌出盐酸,使胃液呈酸性。胃酸在人体的消化吸收中发挥潜重要作用,比如为胃蛋白酶提供适宜的酸性环境,分解食物中的结缔组织和肌纤维,使其易于被消化吸收。而胃酸过多会对胃黏膜产生侵蚀作用,并使人感觉反酸或胃灼热。
胃酸过多会引起不适。治疗酸过多的药物主要有两大类:一是抑酸药,能抑制胃酸分泌,但本身不能和胃酸反应,二是抗酸药,能与胃酸反应,如常用的碳酸氢钠、氢氧化铝、氧化镁、氢氧化镁和碳酸钙等。不同病症需要服用不同的抗酸药。实验小组同学对抗酸药的选择进行探究。
【查阅资料】
1.抗酸药主要利用有效成分与胃液中的过量盐酸反应,药品用量一般为1~2片(约0.5g~1g)。
2.氧化镁和氧化铁均属于金属氧化物,与盐酸反应的原理相似。
3.胃蛋白酶是胃中唯一的消化性蛋白酶,当pH为3~5时活性较好,当pH超过6时会失去活性。
4.理想抗酸药应具备起效快速,避免产生气体刺激溃疡面等特点。
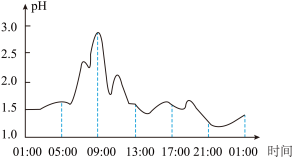
5.科学家发现人体胃液的pH影响人体对药物的吸收,胃液pH低时,胃对弱酸性类药物的吸收相对多;胃液pH高时,有利于弱碱性类药物的吸收。如图是一组胃病患者在空腹状态下24小时胃液pH的变化曲线。
I.是否引起胃内压强的变化
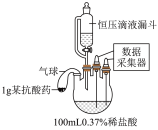
实验仪器及装置如表图中所示。锥形瓶中模拟胃酸过多的环境。将气球中的抗酸药加入锥形瓶中,观察实验现象并记录。
Ⅱ.是否引起胃内温度和pH的变化
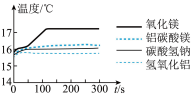
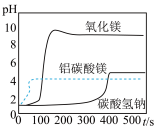
利用上述装置及药品进行实验。向4个烧瓶中分别加入抗酸药,打开恒压滴液漏斗,滴加0.37%的足量稀盐酸。传感器测得的相关结果见图。
【解释与结论】
(1)患者服用含实验1-1成分的胃药时,最适宜的用药时间约为_______ 。
(2)药品用量一般在1~2片内,对“严重胃溃疡患者”,你不建议选用的抗酸药及理由是:_______ (请用化学方程式表示)。
(3)综合资料信息,你优先选择的抗酸药是______ ,其优势有______ 等。
胃酸过多会引起不适。治疗酸过多的药物主要有两大类:一是抑酸药,能抑制胃酸分泌,但本身不能和胃酸反应,二是抗酸药,能与胃酸反应,如常用的碳酸氢钠、氢氧化铝、氧化镁、氢氧化镁和碳酸钙等。不同病症需要服用不同的抗酸药。实验小组同学对抗酸药的选择进行探究。
【查阅资料】
1.抗酸药主要利用有效成分与胃液中的过量盐酸反应,药品用量一般为1~2片(约0.5g~1g)。
2.氧化镁和氧化铁均属于金属氧化物,与盐酸反应的原理相似。
3.胃蛋白酶是胃中唯一的消化性蛋白酶,当pH为3~5时活性较好,当pH超过6时会失去活性。
4.理想抗酸药应具备起效快速,避免产生气体刺激溃疡面等特点。
5.科学家发现人体胃液的pH影响人体对药物的吸收,胃液pH低时,胃对弱酸性类药物的吸收相对多;胃液pH高时,有利于弱碱性类药物的吸收。如图是一组胃病患者在空腹状态下24小时胃液pH的变化曲线。
I.是否引起胃内压强的变化
实验仪器及装置如表图中所示。锥形瓶中模拟胃酸过多的环境。将气球中的抗酸药加入锥形瓶中,观察实验现象并记录。
| 1-1 | 氢氧化铝片 | 气球无明显变化 |
| 1-2 | 碳酸氢钠片 | 气球明显膨胀 | |
| 1-3 | 铝碳酸镁咀嚼片 | 气球无明显变化 | |
| 1-4 | 氧化镁粉末 | 气球无明显变化 |
利用上述装置及药品进行实验。向4个烧瓶中分别加入抗酸药,打开恒压滴液漏斗,滴加0.37%的足量稀盐酸。传感器测得的相关结果见图。
| . | |
|
| |
(1)患者服用含实验1-1成分的胃药时,最适宜的用药时间约为
(2)药品用量一般在1~2片内,对“严重胃溃疡患者”,你不建议选用的抗酸药及理由是:
(3)综合资料信息,你优先选择的抗酸药是
您最近一年使用:0次
【推荐2】酸、碱、盐是几类重要的化合物,它们与人类关系非常密切。
(1)某学习小组探究氢氧化钠、氢氧化钙的化学性质,并做了延伸探究。
①配制溶液:用氢氧化钠固体配制溶质质量分数为1%的氢氧化钠溶液200g,需NaOH_______ g。
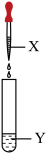
②按如图所示装置进行实验,将X溶液滴入Y溶液中,测定试管内溶液pH由1变到10,则___ (填“X”或“Y”)是NaOH溶液。由此得出氢氧化钠溶液与稀盐酸发生了反应,其化学方程式为___ 。
(2)如图是A、B两种物质的溶解度曲线,请回答:
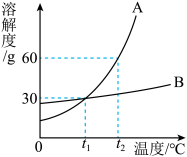
①在_______ 时,A、B两种物质的溶解度相等;
②在t2℃时,将35gA物质加入50g水中,充分溶解,所得溶液的质量为_______ g;
③当物质A中含有少量的B时,可以用_______ 法提纯A。
(1)某学习小组探究氢氧化钠、氢氧化钙的化学性质,并做了延伸探究。

①配制溶液:用氢氧化钠固体配制溶质质量分数为1%的氢氧化钠溶液200g,需NaOH
②按如图所示装置进行实验,将X溶液滴入Y溶液中,测定试管内溶液pH由1变到10,则
(2)如图是A、B两种物质的溶解度曲线,请回答:

①在
②在t2℃时,将35gA物质加入50g水中,充分溶解,所得溶液的质量为
③当物质A中含有少量的B时,可以用
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】胃的化学性消化功能:人类和其他动物的胃壁上有一种特殊的腺体,能分泌胃液。盐酸是胃液的一种成分,它能使胃液保持激活胃蛋白酶所需要的最适宜的pH,它还能使食物中的蛋白质变性而易于水解,以及具有杀死随食物进入胃里的细菌的作用。此外,酸性环境还有助于小肠吸收铁和钙。
胃有很强的消化功能,靠的是胃内的盐酸、胃蛋白酶和黏液、胃液的pH可以达到0.9~1.5,足以把金属锌溶解掉。胃蛋白酶能分解食物中的蛋白质,黏液能把食物包裹起来,既能起到润滑作用,又能保护胃黏膜,使它不受食物引起的机械损伤。但黏液中的糖蛋白有的含糖量很高,相对分子质量很大,它们能抑制胃蛋白酶的活性。胃里的盐酸、胃蛋白酶和黏液联合起来,几乎可以消化一切食物。
根据短文,回答下列问题。
(1)胃液的pH为______ ,酸性环境有助于小肠吸收的铁和钙是指______ (填“单质”或“元素”)。
(2)金属锌溶解在胃酸里的化学方程式为______ ,此反应属于______ (填基本反应类型)。
(3)文中提到的营养素有蛋白质、水、无机盐、______ ,人体所需的营养素还应有______ 。
胃有很强的消化功能,靠的是胃内的盐酸、胃蛋白酶和黏液、胃液的pH可以达到0.9~1.5,足以把金属锌溶解掉。胃蛋白酶能分解食物中的蛋白质,黏液能把食物包裹起来,既能起到润滑作用,又能保护胃黏膜,使它不受食物引起的机械损伤。但黏液中的糖蛋白有的含糖量很高,相对分子质量很大,它们能抑制胃蛋白酶的活性。胃里的盐酸、胃蛋白酶和黏液联合起来,几乎可以消化一切食物。
根据短文,回答下列问题。
(1)胃液的pH为
(2)金属锌溶解在胃酸里的化学方程式为
(3)文中提到的营养素有蛋白质、水、无机盐、
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】某碳酸氢钠中含有少量的氯化铵,为测得碳酸氢钠的含量设计以下两个方案(已知:碳酸氢钠与碱反应生成碳酸钠)
方案一:取样品mg,滴加足量稀盐酸,测量收集到的生成的气体质量。
方案二:取样品mg,滴加硝酸酸化的硝酸银溶液,测量生成沉淀的质量。
(1)方案一中发生反应的化学方程式为____ ;
(2)方案二中有关说法正确的是____________ ;
A、加入硝酸的目的是除去碳酸氢钠
B、可以用稀盐酸代替稀硝酸
C、反应生成的沉淀要经过洗涤,干燥
(3)同学们经过讨论认为通过其他两条途径也可以达到目的,方案是:取样品mg,①加入足量氢氧化钠溶液,测量收集到的______ (填化学式)质量;②加入过量的_____ 溶液后,测量生成沉淀的质量。
方案一:取样品mg,滴加足量稀盐酸,测量收集到的生成的气体质量。
方案二:取样品mg,滴加硝酸酸化的硝酸银溶液,测量生成沉淀的质量。
(1)方案一中发生反应的化学方程式为
(2)方案二中有关说法正确的是
A、加入硝酸的目的是除去碳酸氢钠
B、可以用稀盐酸代替稀硝酸
C、反应生成的沉淀要经过洗涤,干燥
(3)同学们经过讨论认为通过其他两条途径也可以达到目的,方案是:取样品mg,①加入足量氢氧化钠溶液,测量收集到的
您最近一年使用:0次
【推荐2】水和溶液在生产,生活中具有广泛的用途。
(1)下列物质属于溶液的是 (填字母)。
(2)甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。_____ 。
②t2℃时,分别将甲、乙固体溶于水,配成两种物质的饱和溶液各100g,所需水的质量相比,甲_____ 乙(填“大于”“小于”或“等于”)。
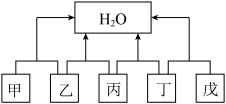
(3)如图中甲、乙、丙、丁、戊是五种不同类别的物质,且分别属于单质、氧化物、酸、碱盐中的一种。相连物质之间均能在一定条件下发生化学反应,且生成物之一为水。_______ (只写一组),其中丙和丁发生中和反应的化学方程式为_______ ;乙和丙反应的化学方程式为_____ 。
②若要鉴别氯化铵和氯化钾固体,请设计实验,并填写下表。
(1)下列物质属于溶液的是 (填字母)。
| A.医用酒精 | B.植物油和水的混合物 |
| C.蒸馏水 | D.糖水和食盐水的混合物 |
(2)甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。
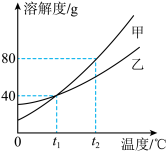
②t2℃时,分别将甲、乙固体溶于水,配成两种物质的饱和溶液各100g,所需水的质量相比,甲
(3)如图中甲、乙、丙、丁、戊是五种不同类别的物质,且分别属于单质、氧化物、酸、碱盐中的一种。相连物质之间均能在一定条件下发生化学反应,且生成物之一为水。
②若要鉴别氯化铵和氯化钾固体,请设计实验,并填写下表。
| 实验步骤 | 实验现象 | 实验结论 |
| 一只研钵中 | 该样品是氯化铵 | |
| 另一只研钵中 | 该样品是氯化钾 |
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】实验室有一固体物质A,其可能是NH4Cl、NaCl、Na2CO3中的两种或多种。按如图所示进行探究实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应)。
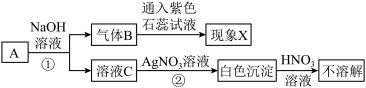
试根据实验过程中发生的现象作出判断,填写以下空白:
(1)气体B的化学式为_____ 。
(2)现象X为_____ 。
(3)固体物质A中不存在的物质是_____ (写化学式)。
(4)溶液C中含有的阴离子为_____ (写离子符号)。
(5)请写出步骤②中生成白色沉淀的化学方程式_____ 。

试根据实验过程中发生的现象作出判断,填写以下空白:
(1)气体B的化学式为
(2)现象X为
(3)固体物质A中不存在的物质是
(4)溶液C中含有的阴离子为
(5)请写出步骤②中生成白色沉淀的化学方程式
您最近一年使用:0次