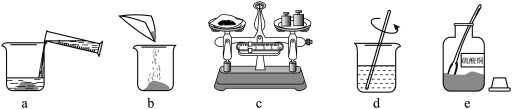
将一定质量的NaC1和Na2CO3固体混合物,加入一定质量分数的盐酸溶液100g,恰好完全反应,生成气体4.4g,经测定反应后溶液中含氯元素的质量为14.2g。计算:
(1)所加盐酸溶液的溶质质量分数:
(2)原固体混合物中氯化钠的质量:
(3)求反应后所得溶液中溶质的质量分数(计算结果保留0.1%)。
(1)所加盐酸溶液的溶质质量分数:
(2)原固体混合物中氯化钠的质量:
(3)求反应后所得溶液中溶质的质量分数(计算结果保留0.1%)。
2022·天津和平·三模 查看更多[2]
更新时间:2022-06-13 08:19:42
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】洁厕灵的有效成分是盐酸。洁厕灵中HCl的质量分数可用NaHCO3溶液来测定(假设洁厕灵中除HCl外的其他成分不与NaHCO3反应)。向锥形瓶加入50g洁厕灵,然后分五次加入NaHCO3溶液,每次加入NaHCO3溶液后均充分反应,且气体全部逸出。实验数据如下表:
请计算:
(1)第一次加入40 g NaHCO3溶液后,生成CO2的质量为多少g。
(2)该洁厕灵中HCl的质量分数(写出计算过程)。
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入NaHCO3溶液的质/g | 40 | 40 | 40 | 40 | 40 |
| 反应后锥形瓶中剩余物的总质量/g | 88.9 | 127.8 | 166.7 | 205.6 | 245.6 |
请计算:
(1)第一次加入40 g NaHCO3溶液后,生成CO2的质量为多少g。
(2)该洁厕灵中HCl的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某纯碱样品中含有氯化钠(假设其成分均匀)。化学兴趣小组按以下步骤测定该样品中氯化钠的质量分数。
(1)配制稀硫酸:
①计算:配制500 g质量分数为19.6%稀硫酸,需要质量分数为98%的浓硫酸(密度为1.84 g/cm3)___________ mL。(精确到0.1 mL)
②量取:用量程为___________ 的量筒量取所需的浓硫酸。
③稀释:______________________ 。
(2)实验测定:
称取10.0 g样品置于烧杯中,加入足量稀硫酸充分反应,烧杯总质量与反应时间的关系如下表所示:
①完全反应后,生成的二氧化碳气体的质量为___________ 。
②计算该样品中氯化钠的质量分数___________ 。(根据化学方程式的计算写出完整的计算步骤)
(1)配制稀硫酸:
①计算:配制500 g质量分数为19.6%稀硫酸,需要质量分数为98%的浓硫酸(密度为1.84 g/cm3)
②量取:用量程为
③稀释:
(2)实验测定:
称取10.0 g样品置于烧杯中,加入足量稀硫酸充分反应,烧杯总质量与反应时间的关系如下表所示:
| 反应时间/min | 0 | t1 | t2 | t3 |
| 烧杯总质量/g | 300.0 | 297.8 | 296.7 | 296.7 |
①完全反应后,生成的二氧化碳气体的质量为
②计算该样品中氯化钠的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取5.0g样品溶于一定量的水中得到25.0g溶液,再分别加入不同质量,溶质质量分数为10%的氢氧化钠溶液,反应得到沉淀的实验数据如下表:
(1)上述实验中,______ 同学进行的实验是氢氧化钠与氯化镁恰好完全反应的。
(2)计算上述实验中符合(1)要求的同学所得滤液中溶质的质量分数(计算结果精确至0.1%)。
| 甲 | 乙 | 丙 | |
| 加入氢氧化钠溶液质量(g) | 20.0 | 40.0 | 60.0 |
| 反应得到沉淀的质量(g) | 1.45 | 2.9 | 2.9 |
(1)上述实验中,
(2)计算上述实验中符合(1)要求的同学所得滤液中溶质的质量分数(计算结果精确至0.1%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】碱式碳酸镁【Mg2(OH)2CO3】是一种高效的新型阻燃剂,一种工业制备原理的化学方程式如下: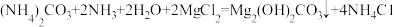 。现向475kg溶质质量分数为20%的MgCl2溶液中加入649kg(NH4)2CO3溶液并通入一定质量的NH3,恰好完全反应。试计算:
。现向475kg溶质质量分数为20%的MgCl2溶液中加入649kg(NH4)2CO3溶液并通入一定质量的NH3,恰好完全反应。试计算:
已知相对分子质量:MgCl2-95;Mg2(OH)2CO3-142;NH4Cl-53.5
(1)Mg2(OH)2CO3中质量分数最大的元素是______ (填元素符号)。
(2)最后所得溶液中溶质的质量分数。
(3)欲将475 kgMgCl2溶液的溶质质量分数由20%变为24%,求需要加入MgC12固体的质量。
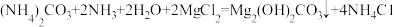 。现向475kg溶质质量分数为20%的MgCl2溶液中加入649kg(NH4)2CO3溶液并通入一定质量的NH3,恰好完全反应。试计算:
。现向475kg溶质质量分数为20%的MgCl2溶液中加入649kg(NH4)2CO3溶液并通入一定质量的NH3,恰好完全反应。试计算:已知相对分子质量:MgCl2-95;Mg2(OH)2CO3-142;NH4Cl-53.5
(1)Mg2(OH)2CO3中质量分数最大的元素是
(2)最后所得溶液中溶质的质量分数。
(3)欲将475 kgMgCl2溶液的溶质质量分数由20%变为24%,求需要加入MgC12固体的质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】碘元素对人体健康起着重要的作用,在食盐中加碘可有效预防甲状腺肿大的发生。
如图是某品牌加碘盐的标签,请回答下列问题。

(1)碘酸钾的相对分子质量为:_____________ ;
(2)碘酸钾中K、I、O三种元素的质量比为:_____ ;
(3)碘酸钾中I元素的质量分数为:__________ ;
(4)根据有关数据估算,每500g该加碘食盐中碘酸钾(KIO3)的质量范围是_____ 。(填字母序号)
A 25~51mg B 15~30mg C 50.6~101.2mg
如图是某品牌加碘盐的标签,请回答下列问题。

(1)碘酸钾的相对分子质量为:
(2)碘酸钾中K、I、O三种元素的质量比为:
(3)碘酸钾中I元素的质量分数为:
(4)根据有关数据估算,每500g该加碘食盐中碘酸钾(KIO3)的质量范围是
A 25~51mg B 15~30mg C 50.6~101.2mg
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】计算。
(1)制造口罩时,常用环氧乙烷(C2H4O)灭菌。常温下,环氧乙烷和乙烯(C2H4)按一定质量比混合的气体中碳元素的质量分数是72%。
①碳元素与氢元素的质量之比是______________ ;
②氧元素的质量分数是_________ ;
③环氧乙烷与乙烯的分子数之比是_________ 。
(2)某种由FeO和Fe2O3组成的混合物中,两种组分的个数之比为3:2,则670g混合物中铁元素的质量为______ g。
(3)测得Fe2O3和另一种氧化物的混合物中氧的含量为40%,则另一种氧化物可能是 ______(填序号)
(1)制造口罩时,常用环氧乙烷(C2H4O)灭菌。常温下,环氧乙烷和乙烯(C2H4)按一定质量比混合的气体中碳元素的质量分数是72%。
①碳元素与氢元素的质量之比是
②氧元素的质量分数是
③环氧乙烷与乙烯的分子数之比是
(2)某种由FeO和Fe2O3组成的混合物中,两种组分的个数之比为3:2,则670g混合物中铁元素的质量为
(3)测得Fe2O3和另一种氧化物的混合物中氧的含量为40%,则另一种氧化物可能是 ______(填序号)
| A.CaO | B.Na2O | C.Al2O3 | D.MgO |
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
解题方法
【推荐1】有一份铜锌合金粉末样品(设只含铜、锌),为认识其组成等,某学习小组进行了以下探究,请参与并完成有关计算:
(1)取样品20g,和足量稀硫酸充分混合,待反应完全后过滤,将滤渣洗涤,干燥后称得其质量为13.5g。该样品中铜的质量分数为______。
(2)再取三份不同质量的样品,分别加入到三份100g相同浓度的硫酸溶液中,充分反应后,测得的数据如下表:
试计算所用硫酸溶液的溶质质量分数(写出计算过程,结果精确到0.01%)。_______
(1)取样品20g,和足量稀硫酸充分混合,待反应完全后过滤,将滤渣洗涤,干燥后称得其质量为13.5g。该样品中铜的质量分数为______。
(2)再取三份不同质量的样品,分别加入到三份100g相同浓度的硫酸溶液中,充分反应后,测得的数据如下表:
| 实验序号 | ① | ② | ③ |
| 样品的质量/g | 10 | 20 | 30 |
| 生成气体的质量/g | 0.1 | 0.2 | 0.25 |
试计算所用硫酸溶液的溶质质量分数(写出计算过程,结果精确到0.01%)。_______
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】为了测定含有氯化钾和碳酸钾的化肥中氯化钾的含量,取5g混合物和11.1%的氯化钙溶液做如下实验:
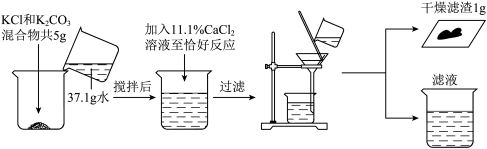
(1)写出上述反应的化学方程式_____;
(2)请列出能与氯化钙反应的物质的质量(x)的比例式_____;
(3)该化肥样品中氯化钾的纯度为_____;
(4)过滤后,最终滤液中溶质的质量分数为_____;
(5)若按上述过程用此化肥样品100t,可以生产出纯净的氯化钾_____t。

(1)写出上述反应的化学方程式_____;
(2)请列出能与氯化钙反应的物质的质量(x)的比例式_____;
(3)该化肥样品中氯化钾的纯度为_____;
(4)过滤后,最终滤液中溶质的质量分数为_____;
(5)若按上述过程用此化肥样品100t,可以生产出纯净的氯化钾_____t。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】现有碳酸钠和氯化钠的固体混合物14.9g,加入95.1水,固体完全溶解,向该溶液中加入氯化钙溶液,所得溶液质量与加入氯化钙溶液的质量的关系如图所示。请计算:

(1)恰好完全反应时,生成沉淀质量是______ 。
(2)恰好完全反应时,所得溶液中溶质的质量分数是多少?

(1)恰好完全反应时,生成沉淀质量是
(2)恰好完全反应时,所得溶液中溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】老师要求同学们将30gNaCl样品中的杂质CuCl2除去,同时测出其中所含CuCl2的质量分数。提供的试剂有:一定质量分数的NaOH溶液、KOH溶液、稀盐酸各100g。小林同学顺利完成了任务。她的方法是:将30gNaCl样品加入100g水中,固体全部溶解后再逐渐加入所选试剂,当加入的试剂质量为56g时,恰好完全反应,测得生成沉淀的质量为4.9g。请回答:
(1)小林同学所选用的试剂是______________ 。
(2)该NaCl样品中CuCl2的质量分数是多少?
(3)当恰好完全反应时,所得溶液的质量是多少?
(1)小林同学所选用的试剂是
(2)该NaCl样品中CuCl2的质量分数是多少?
(3)当恰好完全反应时,所得溶液的质量是多少?
您最近一年使用:0次