化学是一门以实验为基础的学科,下图是几个化学小实验。
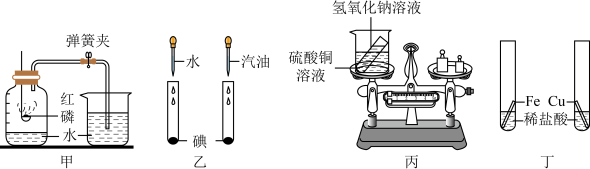
(1)甲图是测定空气中氧气含量的装置图:
①写出红磷燃烧的方程式_______ ,通过本实验可以推断出氧气的化学性质是_______ 。
②如果将烧杯中的水换成氢氧化钠溶液,就可以将红磷换成硫做此实验,原因是_______ 。
(2)乙图中看到的现象是_______ ,由此得出的结论是_______ 。
(3)丙图发生反应的方程式为_______ ,由此总结出盐的一条化性质是_______ 。
(4)通过丁图可以得到铁和铜的金属活动性顺序是Fe_______ Cu(填“>”或“<”),其中,稀盐酸还可以换成_______ 溶液(填一种不同类别的物质)也可以验证铁和铜的活动性顺序。

(1)甲图是测定空气中氧气含量的装置图:
①写出红磷燃烧的方程式
②如果将烧杯中的水换成氢氧化钠溶液,就可以将红磷换成硫做此实验,原因是
(2)乙图中看到的现象是
(3)丙图发生反应的方程式为
(4)通过丁图可以得到铁和铜的金属活动性顺序是Fe
更新时间:2022-07-07 14:22:58
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】空气是一种重要的自然资源。
(1)分子筛制氧机就是以空气为原料,将空气中的氧气与氮气进行分离,获得高浓度的氧气。
①空气经过分子筛时氮气被吸附,氧气通过,其微观示意图如下,请在方框中画出微粒图示_____ 。

②很多物质都可以在高浓度的氧气中燃烧,请写出一种物质在高浓度氧气中燃烧的实验现象及化学方程式_______ 、 _____ 。
(2)工业上需要大量的氧气,我们一般采用_______ 的方法获得。
(3)如图所示实验用于测定空气中氧气的含量。下列关于该实验的说法中正确的是 (填字母)。

(4)空气中除氧气、氮气外,还含有一类重要的混合物,这类物质是_______ 。
(1)分子筛制氧机就是以空气为原料,将空气中的氧气与氮气进行分离,获得高浓度的氧气。
①空气经过分子筛时氮气被吸附,氧气通过,其微观示意图如下,请在方框中画出微粒图示

②很多物质都可以在高浓度的氧气中燃烧,请写出一种物质在高浓度氧气中燃烧的实验现象及化学方程式
(2)工业上需要大量的氧气,我们一般采用
(3)如图所示实验用于测定空气中氧气的含量。下列关于该实验的说法中正确的是 (填字母)。

| A.该实验必须检查装置的气密性 |
| B.实验时红磷一定要足量 |
| C.点燃红磷前先用弹簧夹夹紧乳胶管 |
| D.红磷熄灭后立刻打开弹簧夹 |
| E.最终进入瓶中水的体积约为氧气的体积 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】火是文明的起源,取火的方法经过了漫长的演变过程。
(1)古代人使用的“火折子”吹气可燃,“火折子”的制作材料中有白磷。白磷燃烧的化学反应方程式为______ 。
(2)1830年,法国人发明了摩擦火柴,将白磷、硫、KClO3、MnO2混合做火柴头,摩擦生热使白磷燃烧,利用白磷燃烧的热量使KClO3分解,然后是硫燃烧。该过程中KClO3分解的化学反应方程式为______ 。推测摩擦过程中白磷比硫先燃烧的原因是______ 。
(3)19世纪中期,瑞典人创制出安全火柴,将红磷涂在火柴盒的摩擦面上,硫、KClO3、MnO2则藏于火柴头中、火柴划燃的瞬间,火苗异常旺,对产生此现象的原因推测不合理的是______(填序号)
(1)古代人使用的“火折子”吹气可燃,“火折子”的制作材料中有白磷。白磷燃烧的化学反应方程式为
(2)1830年,法国人发明了摩擦火柴,将白磷、硫、KClO3、MnO2混合做火柴头,摩擦生热使白磷燃烧,利用白磷燃烧的热量使KClO3分解,然后是硫燃烧。该过程中KClO3分解的化学反应方程式为
(3)19世纪中期,瑞典人创制出安全火柴,将红磷涂在火柴盒的摩擦面上,硫、KClO3、MnO2则藏于火柴头中、火柴划燃的瞬间,火苗异常旺,对产生此现象的原因推测不合理的是______(填序号)
| A.火柴头里的硫比火柴梗燃烧更剧烈 |
| B.MnO2分解产生氧气助燃 |
| C.KClO3分解产生氧气助燃 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】下列是初中化学的五个实验,按要求回答问题

(1)图 A 是测定空气中氧气含量的实验
①若实验 A 开始时未加紧弹簧夹,则测定出的空气中氧气含量____ 1/5,若装置漏气, 则测定出的空气中氧气含量____ 1/5。(填“大于”“小于”“等于”)
②该反应的符号表达式是_____ 。
(2)图 B 中的实验现象是_____ 。
(3)实验 C,对比两个实验能得出有关分子性质的结论是_____ 。
(4)图 D 是细铁丝在氧气中燃烧的实验,反应的符号表达式为_____ , 该实验需要预先在集气瓶中加入少量水,目的是_____ 。
(5)图 E 是硫在氧气中燃烧的实验,在空气中点燃硫粉时,观察到淡黄色固体熔化后, 燃烧发出_____ 色火焰;在氧气中,燃烧得更旺,发出_____ 色火焰。硫在氧气中比在空气中燃烧得更旺;铁丝在空气中不燃烧,在氧气中才能剧烈燃烧,是因为____ 。

(1)图 A 是测定空气中氧气含量的实验
①若实验 A 开始时未加紧弹簧夹,则测定出的空气中氧气含量
②该反应的符号表达式是
(2)图 B 中的实验现象是
(3)实验 C,对比两个实验能得出有关分子性质的结论是
(4)图 D 是细铁丝在氧气中燃烧的实验,反应的符号表达式为
(5)图 E 是硫在氧气中燃烧的实验,在空气中点燃硫粉时,观察到淡黄色固体熔化后, 燃烧发出
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】金属铍(Be)是原子能、火箭、导弹、航空、宇宙航行中不可缺少的宝贵材料,有着“超级金属”之称。制备金属铍的原料是绿柱石,其主要成分是BeO,还含有Al2O3、SiO2、Fe2O3和FeO,工艺流程如图12所示。

已知:①滤渣1的主要成分是SiO2,滤渣2的主要成分是Fe(OH)3和Al(OH)3。
②(NH4)2BeF4易溶于水,且在水中的溶解度随温度升高显著增大。
(1)“酸浸”后得到滤液中的金属离子有Be2+、Al3+和_______ (写离子符号);
(2)“氧化”时发生反应的化学方程式是_____ ;
(3)(NH4)2BeF4溶液经蒸发浓缩、______ 、过滤、洗涤、干燥等操作后可得到(NH4)2BeF4晶体;
(4)依据本流程,BeF2通过置换反应得到Be的化学方程式是____ ;
(5)铍的表面易形成致密氧化膜。请选择合适的试剂、设计合理的实验方案,比较铍与铜的金属活动性___ 。

已知:①滤渣1的主要成分是SiO2,滤渣2的主要成分是Fe(OH)3和Al(OH)3。
②(NH4)2BeF4易溶于水,且在水中的溶解度随温度升高显著增大。
(1)“酸浸”后得到滤液中的金属离子有Be2+、Al3+和
(2)“氧化”时发生反应的化学方程式是
(3)(NH4)2BeF4溶液经蒸发浓缩、
(4)依据本流程,BeF2通过置换反应得到Be的化学方程式是
(5)铍的表面易形成致密氧化膜。请选择合适的试剂、设计合理的实验方案,比较铍与铜的金属活动性
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】“奋斗者”号成功坐底世界最深处马里亚纳海沟,创造了我国载人深潜的新纪录。
(1)“奋斗者”号设备中有许多铁制品。工业上用赤铁矿(主要成分为氧化铁)炼铁的化学方程式是__________ 。
(2)为了承受深海110兆帕的巨大压力,载入球舱采用了新型钛合金Ti62A打造。工业上可利用钛白粉(TiO2)生产金属钛(Ti),生产过程如图:

①钛合金属于__________ (填“混合物”或“纯净物”)。
②步骤b中四氯化钛(TiC14)发生置换反应,该化学方程式为________ ;此反应需要在氩气氛围中进行,这是因为氩气的化学性质_________ 。
(3)潜水器动力电池系统使用国际领先的固态磷酸铁锂电池。工作原理是 ,放电时,能转化是
,放电时,能转化是_________ →_______ ,该过程中铁元素的化合价__________ (填“升高”、“降低”或“不变”)。
(4)某化学兴趣小组进行实验探究Ti、Mg、Cu的活动性顺序。在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度足量稀盐酸中,观察现象如下:
下列有关这三种金属的说法正确的是 。
(1)“奋斗者”号设备中有许多铁制品。工业上用赤铁矿(主要成分为氧化铁)炼铁的化学方程式是
(2)为了承受深海110兆帕的巨大压力,载入球舱采用了新型钛合金Ti62A打造。工业上可利用钛白粉(TiO2)生产金属钛(Ti),生产过程如图:

①钛合金属于
②步骤b中四氯化钛(TiC14)发生置换反应,该化学方程式为
(3)潜水器动力电池系统使用国际领先的固态磷酸铁锂电池。工作原理是
 ,放电时,能转化是
,放电时,能转化是(4)某化学兴趣小组进行实验探究Ti、Mg、Cu的活动性顺序。在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度足量稀盐酸中,观察现象如下:
| 金属 | Ti | Mg | Cu |
| 金属表面现象 | 缓慢放出气泡 | 较快放出气泡 | 无变化 |
| A.三种金属的活动性由强到弱的顺序是:Ti、Mg、Cu |
| B.若Ti粉中混有Mg,提纯Ti时可用稀盐酸除去Mg |
| C.也可以根据相同条件下相同时间里生成气体体积多少比较出它们的活动性 |
| D.温度、金属表面积、盐酸浓度等因素都会影响反应速率 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁路交通给人们出行方式和生活方式带来了巨大而深远的影响,回答下列问题:
(1)镁铝合金质轻、强度大的特点广泛运用于高铁的制造,镁铅合金属于___________(填序号)。
(2)铁路建设的钢材主要由铁矿炼制而成。用赤铁矿炼铁过程中,Fe2O3发生了___________ (填“氧化”或“还原”)反应。
(3)铝热剂是修筑铁路时常用的焊接材料,其反应原理是铝粉在一定的条件下与氧化铁发生置换反应,得到熔融的铁和另一种氧化物,该反应的化学方程式为___________ 。
(4)高铁车轮是用一种特制钢制成,该特制钢除铁外还含有铜、镍(Ni)等金属,资料显示金属活动性:Fe>Ni>Cu。直接使用下列药品可以验证三种金属的活动性顺序的是___________(填序号)。
(1)镁铝合金质轻、强度大的特点广泛运用于高铁的制造,镁铅合金属于___________(填序号)。
| A.复合材料 | B.合成材料 | C.金属材料 |
(3)铝热剂是修筑铁路时常用的焊接材料,其反应原理是铝粉在一定的条件下与氧化铁发生置换反应,得到熔融的铁和另一种氧化物,该反应的化学方程式为
(4)高铁车轮是用一种特制钢制成,该特制钢除铁外还含有铜、镍(Ni)等金属,资料显示金属活动性:Fe>Ni>Cu。直接使用下列药品可以验证三种金属的活动性顺序的是___________(填序号)。
| A.FeCl3溶液、Ni、CuCl2溶液 | B.Fe、NiCl2溶液、Cu | C.Fe、Ni、CuCl2溶液 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】根据所学化学知识回答下列问题:
(1)“加铁酱油”可预防贫血,其中的“铁”是指_____ (填 “元素”或“原子”)。
(2)冰箱中放活性炭除去异味,这是利用了活性炭的_____ 性 。
(3)加热冷水,当温度尚未达到沸点时,水中常有气泡冒出的原因是_____ 。
(4)食醋是常用的调味品,一般含有 3%~5%的醋酸(化学式CH3COOH)。醋酸由_____ 种元素组成,0.1mol 醋酸中约含有_____ 个分子(用科学记数法表示)。
(5)实验是进行科学探究的重要方式。请根据图示回答问题:

Ⅰ.图1中细铁丝在氧气中燃烧时,加少量水的作用是_____ 。
Ⅱ.图2电解水可制取氢气,电极X为电源的_____ (填“正”或“负”) 极,反应的化学方程式为_____ ;氢气作为新能源,其主要优点为_____ (写出一点)。
Ⅲ.图3中试管A、B是对比实验,试管A中固体几乎不溶,试管B中固体全部溶解,该实验说明了影响物质溶解性的因素是_____ 。
(6)汽车尾气中含有许多有害气体,使用催化转换器可减少有害气体的排放,其中某一反应过程的微观变化如图所示。

I.该反应的化学方程式为_____ 。
II.物质丁中元素的存在形态为_____ (填“游离态”或“化合态”)。
(1)“加铁酱油”可预防贫血,其中的“铁”是指
(2)冰箱中放活性炭除去异味,这是利用了活性炭的
(3)加热冷水,当温度尚未达到沸点时,水中常有气泡冒出的原因是
(4)食醋是常用的调味品,一般含有 3%~5%的醋酸(化学式CH3COOH)。醋酸由
(5)实验是进行科学探究的重要方式。请根据图示回答问题:

Ⅰ.图1中细铁丝在氧气中燃烧时,加少量水的作用是
Ⅱ.图2电解水可制取氢气,电极X为电源的
Ⅲ.图3中试管A、B是对比实验,试管A中固体几乎不溶,试管B中固体全部溶解,该实验说明了影响物质溶解性的因素是
(6)汽车尾气中含有许多有害气体,使用催化转换器可减少有害气体的排放,其中某一反应过程的微观变化如图所示。

I.该反应的化学方程式为
II.物质丁中元素的存在形态为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】对比是科学研究中常用的方法,下图所示的实验均用到对比的方法。

(1)甲用于探究分子的运动,观察到的现象是___ 。对比A和B烧杯的现象,你得出的结论是 ___ 。
(2)乙实验中应用对比得出的结论是______ 。
(3)丙实验用于探究物质的溶解,实验目的是______ 。

(1)甲用于探究分子的运动,观察到的现象是
(2)乙实验中应用对比得出的结论是
(3)丙实验用于探究物质的溶解,实验目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】日常生活中,物质溶解现象广泛存在。
(1)常温下,在密闭容器中的蔗糖溶液里,溶液下半部分的甜度与上半部分的甜度的关系是_____ (填“相同”或“下半部分高”)。
(2)用溶质质量分数为20%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要20%的氯化钠溶液_____ g。
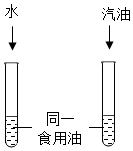
(3)常温下,某同学为探究同一物质在不同溶剂中的溶解性不同,设计了如图所示的实验装置,实验时除了要控制温度相同、试管大小规格相同、加入水与汽油的体积相同外,还要控制食用油的_____ 相同。
(4)事实证明,CaCl2溶于水,溶液导电能力显著增强,是因为其溶液中含有_____ ;若某CaCl2溶液中的C1一为a个,则应对的Ca2+为 _____ 个。
(1)常温下,在密闭容器中的蔗糖溶液里,溶液下半部分的甜度与上半部分的甜度的关系是
(2)用溶质质量分数为20%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要20%的氯化钠溶液
(3)常温下,某同学为探究同一物质在不同溶剂中的溶解性不同,设计了如图所示的实验装置,实验时除了要控制温度相同、试管大小规格相同、加入水与汽油的体积相同外,还要控制食用油的

(4)事实证明,CaCl2溶于水,溶液导电能力显著增强,是因为其溶液中含有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】以重晶石(主要成分是BaSO4,含Al、Fe等元素的杂质)为原料制备产品(BaCl2•2H2O)的一种流程如下:

已知:(1)滤液2主要含BaCl2,还含有AlCl3、FeCl3和HCl等杂质。
(2)25℃下,Fe(OH)3、Al(OH)3完全沉淀的pH依次为3.0和5.4。
(3)BaCl2•2H2O受热易失去结晶水。
回答下列问题:
(1)高温焙烧时将重晶石粉碎的目的是_____ 。焙烧后,除生成CO,还生成一种只含两种元素的化合物,请写出BaSO4与C反应的化学方程式:_____ 。
(2)“固体”(微溶于水)与盐酸发生复分解反应,生成的一种气体通入CuSO4溶液中也发生复分解反应,则滤渣3的成分是_____ (填化学式)。
(3)加入BaCO3的目的是调节溶液的pH,pH至少要达到_____ (填“3.0”或“5.4”),测定此pH应该选择_____ (填“广泛pH试纸”或“pH计”)。
(4)滤液4经蒸发浓缩、_____ 、过滤、洗涤和干燥,得到产品。经常选用95%的乙醇洗涤,优点是:①BaCl2•2H2O难溶于乙醇,能降低晶体损耗;②_____ 。

已知:(1)滤液2主要含BaCl2,还含有AlCl3、FeCl3和HCl等杂质。
(2)25℃下,Fe(OH)3、Al(OH)3完全沉淀的pH依次为3.0和5.4。
(3)BaCl2•2H2O受热易失去结晶水。
回答下列问题:
(1)高温焙烧时将重晶石粉碎的目的是
(2)“固体”(微溶于水)与盐酸发生复分解反应,生成的一种气体通入CuSO4溶液中也发生复分解反应,则滤渣3的成分是
(3)加入BaCO3的目的是调节溶液的pH,pH至少要达到
(4)滤液4经蒸发浓缩、
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】氯化钠是生活的必需品,也是重要的化工原料。某兴趣小组进行粗盐提纯的流程如图所示。

(1)操作②为_____________________ 。
(2)A操作中容易造成溶液飞溅,为避免此现象应进行的操作是___________________ 。
(3)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较高,其可能的原因是_________ (填字母)。
a.食盐没有全部溶解即过滤 b.蒸发时食盐水飞溅剧烈
c.蒸发后,所得精盐很潮湿 d.蒸发皿上沾有的精盐没有全部转移到称量纸上
(4)精盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质。化学工业上需要纯净的氯化钠,需对精盐进行提纯,其步骤是先将精盐溶于水,然后通过如下操作即可得到较纯的氯化钠:①过滤;②加过量的NaOH溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液。正确的操作顺序____ (填序号)。

(1)操作②为
(2)A操作中容易造成溶液飞溅,为避免此现象应进行的操作是
(3)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较高,其可能的原因是
a.食盐没有全部溶解即过滤 b.蒸发时食盐水飞溅剧烈
c.蒸发后,所得精盐很潮湿 d.蒸发皿上沾有的精盐没有全部转移到称量纸上
(4)精盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质。化学工业上需要纯净的氯化钠,需对精盐进行提纯,其步骤是先将精盐溶于水,然后通过如下操作即可得到较纯的氯化钠:①过滤;②加过量的NaOH溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液。正确的操作顺序
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐3】下图中的物质均为初中化学常见物质,其中A是常见的补钙剂,B是黑色粉末,H是蓝色沉淀。下图是它们之间的转化关系(部分生成物已经略去),请回答:

(1)写出B物质的化学式___________ ;
(2)写出F+G→H的化学方程式__________________ ;
(3)写出物质E的用途_________________ 。(一种即可)

(1)写出B物质的化学式
(2)写出F+G→H的化学方程式
(3)写出物质E的用途
您最近一年使用:0次



