t2℃时,将甲,乙各80g分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图。甲和乙的溶解度曲线如图。请结合图示回答下列问题:
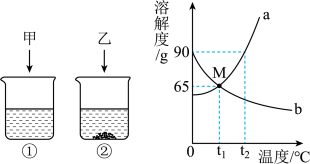
(1)固体甲对应的溶解度曲线是_____________ (填“a”或“b”)。
(2)a中含有少量b,可用______________ (填“降温结晶”或“蒸发结晶”)的方法提纯a。
(3)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液变成不饱和的是______________ (填“甲”或“乙”),所得溶液中溶剂的关系是甲______________ 乙(填“>”或“<”或“=”)。
(4)t1℃时,将165g甲的饱和溶液稀释成20%的溶液,需加水____________ g。

(1)固体甲对应的溶解度曲线是
(2)a中含有少量b,可用
(3)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液变成不饱和的是
(4)t1℃时,将165g甲的饱和溶液稀释成20%的溶液,需加水
2022·广西河池·二模 查看更多[2]
更新时间:2022-07-24 19:23:23
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】海水中蕴藏丰富的化学资源,辛勤劳动才能获得海洋的馈赠。
(一)从海水提取粗盐

(1)上图中N是_______ (“冷却”或“蒸发”)池
(2)根据海水晒盐的原理,下列说法错误的是_______ (填标号)。
A 海水进入贮水池中,海水的成分基本不变
B 在N中,海水中水的质量不变
C 在N中,海水中氯化钠的质量分数增加
D 析出晶体后的母液不能继续溶解氯化钠固体
(二)从海水获得淡水
海水淡化是国际上研究的热点问题。我国科学家在利用高分子膜进行海水淡化的研究上取得了一些成绩。如图为经过一段时间后左侧的海水经高分子膜渗透得到右侧的淡水。

(3)海水中含量最多的分子是_______ (填符号)。
(4)从微粒种类考虑,海水和淡水的本质区别是_______ 。
(5)从微观角度具体阐述高分子膜在海水淡化过程中所起的选择性作用_______ 。
(三)从海水提取镁

(6)实验室中进行操作a,需使用的玻璃仪器有烧杯、玻璃棒、_______ 。
(7)反应③中MgCl2与石灰乳发生复分解反应的化学方程式:_______ ,反应⑤中发生反应的化学方程式:_______ 。(两个反应任选一个,若两个都写,则按第一个进行评分)
(8)已知⑥为分解反应,则海水提取镁过程中可以循环利用的一种物质是_______ (填化学式)。
(一)从海水提取粗盐

(1)上图中N是
(2)根据海水晒盐的原理,下列说法错误的是
A 海水进入贮水池中,海水的成分基本不变
B 在N中,海水中水的质量不变
C 在N中,海水中氯化钠的质量分数增加
D 析出晶体后的母液不能继续溶解氯化钠固体
(二)从海水获得淡水
海水淡化是国际上研究的热点问题。我国科学家在利用高分子膜进行海水淡化的研究上取得了一些成绩。如图为经过一段时间后左侧的海水经高分子膜渗透得到右侧的淡水。

(3)海水中含量最多的分子是
(4)从微粒种类考虑,海水和淡水的本质区别是
(5)从微观角度具体阐述高分子膜在海水淡化过程中所起的选择性作用
(三)从海水提取镁

(6)实验室中进行操作a,需使用的玻璃仪器有烧杯、玻璃棒、
(7)反应③中MgCl2与石灰乳发生复分解反应的化学方程式:
(8)已知⑥为分解反应,则海水提取镁过程中可以循环利用的一种物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C三种物质的饱和溶液溶质质量分数随温度的变化如图1所示。
(2)t1℃时,将125g一定质量分数的A溶液恒温蒸发,溶液质量随蒸发掉水的质量的变化关系如图2所示,则125gA溶液_____ 饱和溶液(填“是”或“不是”),M点溶液中溶质质量为______ 。

| A.NaCl | B.Ca(OH)2 | C.KNO3 | D.NH4NO3 |
(2)t1℃时,将125g一定质量分数的A溶液恒温蒸发,溶液质量随蒸发掉水的质量的变化关系如图2所示,则125gA溶液

| A.t1℃时,将20gA物质加入到100g水中,充分溶解后,所得溶液的质量是120g |
| B.t2℃时,将A、B、C的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是B>A=C |
| C.若A物质中混有少量B物质,可通过冷却热饱和溶液提纯A物质 |
| D.t1℃时,A、C的饱和溶液中含有的溶剂质量相等 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】中华文明源远流长,优秀传统文化博大精深,灿烂辉煌,是民族的“根”与“魂”。《天工开物》记载了中国传统科技不同时期的辉煌成就。请分析图文信息,解答21~24题的相关问题。

1.“丹青”章中记载“每升水银一斤得朱(HgS)十四两,次朱三两五钱。出数藉硫质而生”(图1)。其描述的反应为Hg+S=HgS,其中汞由______ 构成,一斤汞(古代一斤是16两)能制取十七两五钱的硫化汞,比汞多出的一两五钱是______ 的质量。
【新角度·安全措施】
2.“燔石”章中记载南方竖井采煤时(图2),用竹管排出瓦斯(以甲烷为主的气体),目的是______ 。“珠玉”章中记载井下采宝时,下井人用长绳系腰并在腰间挂一巨铃,当下井人感到呼吸困难时赶快摇铃,让他人用长绳将其拉出井来。这是因为下井人吸入了大量“宝气”,“宝气”富含一氧化碳、甲烷、氮气以及其他毒气等,为保障下井人的人身安全和提高下井人的效率,你的建议是______ (写一条)。
3.“作咸”章记载的海盐制取中提到:在涨潮能淹没的浅滩地,直接采用风吹日晒蒸发结晶,原理是______ ;在不被海潮淹没的高地,则利用草木灰疏松的结构使土壤中含盐的水分以毛细作用大量进入灰里“种盐”,草木灰中含K2CO3,所制得的食盐更易保持Na-K平衡,Na、K是人体必需的______ (填“常量”或“微量”)元素。书中记载淋洗(图3):用竹或木将芦席架在浅坑上,将扫来的盐料铺在席上,中间用海水淋灌,盐卤水就渗到浅坑中、其操作为溶解与过滤,用海水反复淋洗盐意在______ 。
4.受时代局限和条件限制,书中记录难免有疏漏和不够确切之处。《天工开物》是第一本记述锌(即倭铅,如图4)的制法的著作。泥罐内将炉甘石(主要成分为ZnCO3)、煤粉混合,在高温下最终生成锌蒸气,如果不用铜来收伏,锌就会以蒸气形式逸出。靠泥固定的“封裹”状态会使锌蒸气逸出,须设法冷却后才能取锌的原因是______ ;泥罐顶部燃料煤饼的主要作用是提供热量,其主要成分完全燃烧的化学方程式是______ 。

1.“丹青”章中记载“每升水银一斤得朱(HgS)十四两,次朱三两五钱。出数藉硫质而生”(图1)。其描述的反应为Hg+S=HgS,其中汞由
【新角度·安全措施】
2.“燔石”章中记载南方竖井采煤时(图2),用竹管排出瓦斯(以甲烷为主的气体),目的是
3.“作咸”章记载的海盐制取中提到:在涨潮能淹没的浅滩地,直接采用风吹日晒蒸发结晶,原理是
4.受时代局限和条件限制,书中记录难免有疏漏和不够确切之处。《天工开物》是第一本记述锌(即倭铅,如图4)的制法的著作。泥罐内将炉甘石(主要成分为ZnCO3)、煤粉混合,在高温下最终生成锌蒸气,如果不用铜来收伏,锌就会以蒸气形式逸出。靠泥固定的“封裹”状态会使锌蒸气逸出,须设法冷却后才能取锌的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C三种固体物质的溶解度曲线如图所示,请完成下列问题:

(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是_______ 。
(2)t2℃时,70gA物质的饱和溶液升温至t3℃,溶液仍要达到饱和需要加入A物质的质量___ g。
(3)现有t1℃接近饱和的C溶液,在不改变溶液中溶质的质量分数的前提下,要使其变为饱和溶液,可采取的一种措施是______ 。
(4)若B中含有少量的A物质,可采用________ 方法提纯B。

(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是
(2)t2℃时,70gA物质的饱和溶液升温至t3℃,溶液仍要达到饱和需要加入A物质的质量
(3)现有t1℃接近饱和的C溶液,在不改变溶液中溶质的质量分数的前提下,要使其变为饱和溶液,可采取的一种措施是
(4)若B中含有少量的A物质,可采用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】如图是甲、乙、丙三种固体物质的溶解度曲线。根据图中的信息回答下列问题:
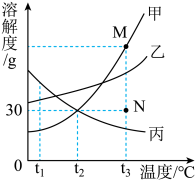
(1)tl℃时,甲的溶解度______ 乙的溶解度(填“>”、“<”或“二”);
(2)t2℃时,20g丙溶解于50g水中形成________ g溶液;
(3)若要将甲的饱和溶液转化为不饱和溶液可采用的一种方法 是________ ;
(4)t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的由大到小的是____________ 。

(1)tl℃时,甲的溶解度
(2)t2℃时,20g丙溶解于50g水中形成
(3)若要将甲的饱和溶液转化为不饱和溶液可采用的一种方法 是
(4)t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的由大到小的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】溶液在生产、生活中起着十分重要的作用。请回答下列问题。
(1)向生活中常见的四种物质中分别加入适量的水,充分搅拌后能形成溶液的是______(填序号)。
(2)在配制蔗糖溶液时,蔗糖溶于水并搅拌均匀后,上、下甜度______ (填“相同”或“不同”),这是因为溶液具有______ 性。发现溶解后液面低于原水平线,从微观角度来看,这是因为______ 。除了升高温度,还能通过______ 操作加快溶解速率。
(3)在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯中加水并进行搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是______(填序号)。
(4) 时,等质量的甲、乙两种固体分别加入等质量的水中,加入固体的质量与溶液溶质分数的关系如图所示,请回答下列问题。
时,等质量的甲、乙两种固体分别加入等质量的水中,加入固体的质量与溶液溶质分数的关系如图所示,请回答下列问题。______ ,将甲的不饱和溶液变为饱和溶液,可用的方法是______ 。
②该温度下,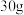 乙的饱和溶液稀释为
乙的饱和溶液稀释为 的溶液需加水
的溶液需加水______ g。
(1)向生活中常见的四种物质中分别加入适量的水,充分搅拌后能形成溶液的是______(填序号)。
| A.蔗糖 | B.小苏打 | C.食用油 | D.奶粉 |
(2)在配制蔗糖溶液时,蔗糖溶于水并搅拌均匀后,上、下甜度
(3)在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯中加水并进行搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是______(填序号)。
| A.氯化钠 | B.硝酸铵 | C.氢氧化钠 | D.蔗糖 |
(4)
 时,等质量的甲、乙两种固体分别加入等质量的水中,加入固体的质量与溶液溶质分数的关系如图所示,请回答下列问题。
时,等质量的甲、乙两种固体分别加入等质量的水中,加入固体的质量与溶液溶质分数的关系如图所示,请回答下列问题。
②该温度下,
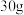 乙的饱和溶液稀释为
乙的饱和溶液稀释为 的溶液需加水
的溶液需加水
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是甲、乙两种固体物质在水中的溶解度曲线。

(1)t1℃时,甲的溶解度_____ 乙的溶解度(填“<”、“>”或“=”)。
(2)将t2℃时甲、乙的饱和溶液分别升温至t3℃,甲溶液中溶质的质量分数将_____ (填“增大”、“减小”或“不变”下同)。
(3)t2℃时,甲的饱和溶液中溶质的质量m甲与乙的饱和溶液中溶质的质量m乙相比较,两者的大小关系是 (选填序号)。

(1)t1℃时,甲的溶解度
(2)将t2℃时甲、乙的饱和溶液分别升温至t3℃,甲溶液中溶质的质量分数将
(3)t2℃时,甲的饱和溶液中溶质的质量m甲与乙的饱和溶液中溶质的质量m乙相比较,两者的大小关系是 (选填序号)。
| A.m甲>m乙 | B.m甲<m乙 | C.m甲=m乙 | D.不确定 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】甲、乙两种物质的溶解度曲线如图所示。下列说法中正确的是(______ )

A.t1℃时,甲饱和溶液的溶质质量分数大于乙饱和溶液
B. t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙
C. t2℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和
D. t2℃时,甲、乙饱和溶液的溶质质量分数都为_________

A.t1℃时,甲饱和溶液的溶质质量分数大于乙饱和溶液
B. t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙
C. t2℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和
D. t2℃时,甲、乙饱和溶液的溶质质量分数都为
您最近一年使用:0次
【推荐3】溶液与人类生产、生活密切相关。
(1)下列溶液中,溶剂不是水的是 (填序号)
(2)某固体物质溶于水能形成低温环境,可自制小“冰箱”,该固体是 (填序号)
(3)甲、乙、丙三种固体物质的溶解度曲线如图所示。回答:

①在__________ ℃时,甲、乙的溶解度相等。
②t2℃时,将甲溶液的状态由m点变为n点,可采用的方法是__________ (写一种)。
③将t2℃甲、乙、丙的饱和溶液,分别降温到t1℃,所得溶液的溶质质量分数最大的是__________ 。
(1)下列溶液中,溶剂不是水的是 (填序号)
| A.碘酒溶液 | B.生理盐水 | C.能量饮料 |
| A.食用盐 | B.氧化钙 | C.硝酸铵 |

①在
②t2℃时,将甲溶液的状态由m点变为n点,可采用的方法是
③将t2℃甲、乙、丙的饱和溶液,分别降温到t1℃,所得溶液的溶质质量分数最大的是
④t2℃时,将等质量的甲、乙、丙的饱和溶液,均恒温蒸发等质量的水,析出溶质质量由多到少的顺序为
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐1】阅读下面的短文,回答下列问题。
过氧乙酸是抗“新冠肺炎”的主要消毒杀菌剂。过氧乙酸的化学式为C2H4O3,是无色透明液体,易溶于水、酒精,易挥发,有很强的刺激性酸臭味,呈弱酸性,有腐蚀性。贮存过程中会逐渐分解,见光、遇热、有机物或金属等杂质分解更快,急剧分解时发生爆炸。过氧乙酸有很强的氧化性,质量分数在0.005%~1%的水溶液,是不同病毒、病菌的广谱、高效、速效的消毒杀菌剂。
(1)过氧乙酸由_________ 组成。
(2)过氧乙酸的物理性质是______ (写一条即可)。
(3)关于贮存及配制过氧乙酸消毒液的下列说法正确的是__________。
(4)要配制1000g溶质质量分数为0.2%的过氧乙酸的洗手液,需要溶质质量分数为40%的过氧乙酸溶液_____________ g。
过氧乙酸是抗“新冠肺炎”的主要消毒杀菌剂。过氧乙酸的化学式为C2H4O3,是无色透明液体,易溶于水、酒精,易挥发,有很强的刺激性酸臭味,呈弱酸性,有腐蚀性。贮存过程中会逐渐分解,见光、遇热、有机物或金属等杂质分解更快,急剧分解时发生爆炸。过氧乙酸有很强的氧化性,质量分数在0.005%~1%的水溶液,是不同病毒、病菌的广谱、高效、速效的消毒杀菌剂。
(1)过氧乙酸由
(2)过氧乙酸的物理性质是
(3)关于贮存及配制过氧乙酸消毒液的下列说法正确的是__________。
| A.贮存过氧乙酸应注意避光、密闭、低温保存 |
| B.可以在金属容器中配制过氧乙酸溶液 |
| C.配制过氧乙酸的稀溶液,可以用手搅拌 |
| D.消毒、杀菌用的过氧乙酸溶液,浓度越大越好 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)“生命吸管”是一种可以随身携带的小型净化器,里面装有网丝、注入了活性炭和碘的树脂。其中活性炭起到______ 和过滤的作用。
(2)衣服上沾有的油污,可用汽油洗去,是因为汽油能______ (选填“溶解”或“乳化”)油污。
(3)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体在温度越高时,在等量水中溶解得______ (选填“多”“少”或“不变”)。
(4)水常用来配制各种溶液,硝酸钾溶液中的溶质为______ 。
(5)农业生产上常用溶质质量分数为10%〜20%的氯化钠溶液来选种。现将300g25%的氯化钠溶液稀释为15%的氯化钠溶液,需要加水的质量为______ g。
(6)已知:60°C时,100g水中最多能溶解37.3g氯化钠;60°C时,100g水中最多能溶解55.2g氯化铵。60°C时,向两个分别盛有50g氯化钠和氯化铵的烧杯中,各加入100g水,充分溶解后,为饱和溶液的是____ 溶液;将不饱和的溶液转变为饱和溶液的方法有___ 。
(1)“生命吸管”是一种可以随身携带的小型净化器,里面装有网丝、注入了活性炭和碘的树脂。其中活性炭起到
(2)衣服上沾有的油污,可用汽油洗去,是因为汽油能
(3)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体在温度越高时,在等量水中溶解得
(4)水常用来配制各种溶液,硝酸钾溶液中的溶质为
(5)农业生产上常用溶质质量分数为10%〜20%的氯化钠溶液来选种。现将300g25%的氯化钠溶液稀释为15%的氯化钠溶液,需要加水的质量为
(6)已知:60°C时,100g水中最多能溶解37.3g氯化钠;60°C时,100g水中最多能溶解55.2g氯化铵。60°C时,向两个分别盛有50g氯化钠和氯化铵的烧杯中,各加入100g水,充分溶解后,为饱和溶液的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】溶液在生活、生产中具有广泛的用途。
(1)硝酸钾和氯化钠的溶解度曲线如图所示。

①在某一温度下,将 40g 硝酸钾固体加入100g 水中,充分搅拌后,仍 有 8.4g 硝酸钾固体未溶解。所得溶液是该温度下硝酸钾的________ (填 “饱和”或 “不饱和”)溶液;该温度约为________ °C 。
②工业上将硝酸钾和氯化钠的热混合溶液(两者均已达到饱和)冷却至室温,析出晶体中的主要物质是________________ 。
③10°C 时,将等质量的KNO3、NaCl分别加入到各盛有100g 水的两个烧杯中,充分搅拌后恢复到l 0°C ,现象如图所示。下列说法正确的是____________ (填字母)。

A 乙中加入的固体是NaCl
B 甲中溶液可能是该溶质的饱和溶液
C 将烧杯甲中的溶液全部倒入乙中,充分搅拌,一定有固体剩余
D 若将甲、乙的温度从10°C升高到30°C ,两溶液中的溶质质量分数相等
(2)若用溶质质量分数为24 % 的NaCl溶液和蒸馏水配制150g 溶质质量分数为16 %的NaCl溶液,则所需 24 % 的NaCl溶液与蒸馏水的质量比为________ ; 配制时所需仪器除了玻璃棒、烧杯、试剂瓶,还需_______________ 。
(1)硝酸钾和氯化钠的溶解度曲线如图所示。

①在某一温度下,将 40g 硝酸钾固体加入100g 水中,充分搅拌后,仍 有 8.4g 硝酸钾固体未溶解。所得溶液是该温度下硝酸钾的
②工业上将硝酸钾和氯化钠的热混合溶液(两者均已达到饱和)冷却至室温,析出晶体中的主要物质是
③10°C 时,将等质量的KNO3、NaCl分别加入到各盛有100g 水的两个烧杯中,充分搅拌后恢复到l 0°C ,现象如图所示。下列说法正确的是

A 乙中加入的固体是NaCl
B 甲中溶液可能是该溶质的饱和溶液
C 将烧杯甲中的溶液全部倒入乙中,充分搅拌,一定有固体剩余
D 若将甲、乙的温度从10°C升高到30°C ,两溶液中的溶质质量分数相等
(2)若用溶质质量分数为24 % 的NaCl溶液和蒸馏水配制150g 溶质质量分数为16 %的NaCl溶液,则所需 24 % 的NaCl溶液与蒸馏水的质量比为
您最近一年使用:0次



