某中学实验小组在实验室用加热氯酸钾和二氧化锰的混合物来制取氧气,此反应的符号表达式为________ 。反应一段时间收集到所需的氧气后停止加热,小组同学们讨论认为固体的组成存在两种情况,小组成员对其剩余固体的成分进行如下猜想:
小平的猜想:KClO3、KCl、MnO2。
小福的猜想:_______ 。
以上猜想中,小平猜想的理由,理由一:氯酸钾是剩余的固体反应物;理由二:________ ;
理由三:二氧化锰是固体催化剂一定存在。
小平同学为了验证自己的猜想,设计的实验方法是:取样于试管中(或继续)加热,伸入带火星的木条,________ ,则证明小平的猜想是正确的。
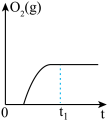
小组同学经过此次实验分析共同总结出对化学反应的固体成分探究时,需要考虑的因素是固体生成物、固体催化剂一定存在;_________ 可能存在。有关放出氧的质量(g)与反应时间(t)的关系图象如下图,t1时刻固体成分中________ 氯酸钾(填“存在或不存在")。
小平的猜想:KClO3、KCl、MnO2。
小福的猜想:
以上猜想中,小平猜想的理由,理由一:氯酸钾是剩余的固体反应物;理由二:
理由三:二氧化锰是固体催化剂一定存在。
小平同学为了验证自己的猜想,设计的实验方法是:取样于试管中(或继续)加热,伸入带火星的木条,
小组同学经过此次实验分析共同总结出对化学反应的固体成分探究时,需要考虑的因素是固体生成物、固体催化剂一定存在;

更新时间:2022-11-23 13:07:46
|
相似题推荐
科学探究题
|
较易
(0.85)
名校
【推荐1】某化学兴趣小组通过实验探究在分解氯酸钾制氧气的反应中二氧化锰的作用,该反应的化学方程式为 _____ 。

【设计实验】用图1 所示装置进行实验,步骤如下: 步骤Ⅰ:_____ ; 步骤Ⅱ:按照如图1 装入药品;
步骤Ⅲ:加热右侧支管,用带火星的木条在导管口检验生成的气体;
步骤Ⅳ:冷却后,将装置倾斜,使左侧支管中的药品进入右侧支管,再加 热右侧支管,用带火星的木条在导管口检验生成的气体。
【实验现象】步骤Ⅲ和步骤Ⅳ中,一段时间后都能观察到带火星的木条复燃,但木条复燃更快的是_____ (填“Ⅲ”或“IV”)。
【交流反思】要想确认分解氯酸钾制取氧气的反应中二氧化锰是催化剂,还需通过实验证 明二氧 化锰质量和_____ 在反应前后都没有发生变化。
【拓展探究】在老师的指导下,该小组同学利用图2 所示装置继续进行深入探究。以氧 气的体积分 数为纵坐标,温度为横坐标,得到图3 所示曲线(图中的“1:2”、“1:1”、“2:1”、“3:1”、“4:1”、“5:1”指氯酸钾和二氧化锰的质量比)。
【实验分析】根据图 3,氯酸钾的分解温度随氯酸钾和二氧化锰的质量比变化的大致规 律 是_____ ;在分解氯酸钾制氧气的反 应中 二氧化锰起催化作用,可能是因为二氧化锰能 _____ 。

【设计实验】用图1 所示装置进行实验,步骤如下: 步骤Ⅰ:
步骤Ⅲ:加热右侧支管,用带火星的木条在导管口检验生成的气体;
步骤Ⅳ:冷却后,将装置倾斜,使左侧支管中的药品进入右侧支管,再加 热右侧支管,用带火星的木条在导管口检验生成的气体。
【实验现象】步骤Ⅲ和步骤Ⅳ中,一段时间后都能观察到带火星的木条复燃,但木条复燃更快的是
【交流反思】要想确认分解氯酸钾制取氧气的反应中二氧化锰是催化剂,还需通过实验证 明二氧 化锰质量和
【拓展探究】在老师的指导下,该小组同学利用图2 所示装置继续进行深入探究。以氧 气的体积分 数为纵坐标,温度为横坐标,得到图3 所示曲线(图中的“1:2”、“1:1”、“2:1”、“3:1”、“4:1”、“5:1”指氯酸钾和二氧化锰的质量比)。
【实验分析】根据图 3,氯酸钾的分解温度随氯酸钾和二氧化锰的质量比变化的大致规 律 是
您最近一年使用:0次
【推荐2】某兴趣小组对氯酸钾分解反应制取氧气的催化剂进行研究,在相同的加热条件下,相同的装置完成表中实验:
(1)设置实验1的目的是_____ ;
(2)Fe2O3铁元素(Fe)的化合价为_____ ;
(3)由实验1和实验4可知,氯化钾_____ (填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50mL氧气,所需时间明显少于171s,解释原因:_____ 。
(4)要比较氯酸钾分解反应中不同催化剂的催化效果,除了测量收集50mL氧气所需时间外,还可以测量相同时间内_____ 。
(5)有同学在实验室中用高锰酸钾制取氧气时,发现收集到的氧气产量远远大于理论产量,提出如下猜想
猜想一:可能是锰酸钾在加热时会产生氧气;
猜想二:可能是_____ 在加热时会产生氧气;
请你设计实验证明猜想一正确(写出实验步骤和实验现象)。
实验步骤:_____ ;
实验现象:_____ 。
| 编号 | 氯酸钾质量/g | 催化剂 | 催化剂质量/g | 收集50mL氧气所需时间/s |
| 实验1 | 5 | - | - | 171 |
| 实验2 | 5 | MnO2 | 0.5 | 49 |
| 实验3 | 5 | Fe2O3 | 0.5 | 58 |
| 实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是
(2)Fe2O3铁元素(Fe)的化合价为
(3)由实验1和实验4可知,氯化钾
(4)要比较氯酸钾分解反应中不同催化剂的催化效果,除了测量收集50mL氧气所需时间外,还可以测量相同时间内
(5)有同学在实验室中用高锰酸钾制取氧气时,发现收集到的氧气产量远远大于理论产量,提出如下猜想
猜想一:可能是锰酸钾在加热时会产生氧气;
猜想二:可能是
请你设计实验证明猜想一正确(写出实验步骤和实验现象)。
实验步骤:
实验现象:
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐3】小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
【分析数据、得出结论】
(1)由实验_____ 对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是_____ 。
(3)若氧化铁是该反应的催化剂,请写出这个反应的文字表达式_____ 。
(4)如表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据。
①据如表可知二氧化锰与氯酸钾的质量比为_____ 时,反应速率最快;
②通过分析可知,在化学反应中催化剂的用量_____ 越多越好。(填“是”或“不是”)
③二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的_____ ,所以反应速率受到影响。
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验药品 | 分解温度 |
| ① | 氯酸钾 | 580℃ |
| ② | 氯酸钾、二氧化锰(质量比 1:1) | 350℃ |
| ③ | 氯酸钾、氧化铜(质量比 l:1) | 370℃ |
| ④ | 氯酸钾、氧化铁(质量比 1:1) | 390℃ |
【分析数据、得出结论】
(1)由实验
(2)实验所用的三种金属氧化物,催化效果最好的是
(3)若氧化铁是该反应的催化剂,请写出这个反应的文字表达式
(4)如表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据。
①据如表可知二氧化锰与氯酸钾的质量比为
②通过分析可知,在化学反应中催化剂的用量
③二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐1】在老师的指导下,某学习小组利用如图1所示装置对氯酸钾(KClO3)制氧气进行了深入的探究学习。

资料:
①KClO3的熔点约为356℃,MnO2的分解温度约为535℃。用酒精灯加热物质,受热物质的温度一般约为400℃左右;
②不同配比是指KClO3和MnO2混合物中,KClO3和MnO2的质量比;
③氯酸钾分解时,传感器测得氧气浓度随温度的变化示意图及不同配比时氧气浓度随温度的变化示意图分别如图2和图3所示。
(1)分析图2,KClO3分解温度_____ (填“高于”、“等于”或“低于”)其熔点。
(2)分析图3,KClO3分解温度随物质配比变化的规律是_____ 。
(3)为证实MnO2的催化作用,小组同学利用如图4装置进行如表所示的实验:
步骤Ⅳ的实验现象能否说明MnO2是KClO3分解的催化剂?_____ (填“能”或“不能”),原因是_____ 。
(4)除催化剂外,影响化学反应的速率的因素还有_____ 和_____ 等。
(5)步骤Ⅳ中,将MnO2混入右侧支管有余热的KClO3中的操作方法是将_____ 。

资料:
①KClO3的熔点约为356℃,MnO2的分解温度约为535℃。用酒精灯加热物质,受热物质的温度一般约为400℃左右;
②不同配比是指KClO3和MnO2混合物中,KClO3和MnO2的质量比;
③氯酸钾分解时,传感器测得氧气浓度随温度的变化示意图及不同配比时氧气浓度随温度的变化示意图分别如图2和图3所示。
(1)分析图2,KClO3分解温度
(2)分析图3,KClO3分解温度随物质配比变化的规律是
(3)为证实MnO2的催化作用,小组同学利用如图4装置进行如表所示的实验:
| 步骤 | 实验操作 | 实验现象 |
| Ⅰ | 检查气密性 | 气密性良好 |
| Ⅱ | 分别在“Y”形管两侧支管中加入少量MnO2和KClO3,塞紧橡皮塞 | 没有明显现象 |
| Ⅲ | 分别先后加热MnO2和KClO3,用带火星木条放在导管口。加热 | 木较条长时间后才能复燃 |
| Ⅳ | 冷却后,将“Y”形管左侧支管中部分MnO2混入右侧支管中,振荡“Y”形管,加热,用带火星木条放在导管口 |
(4)除催化剂外,影响化学反应的速率的因素还有
(5)步骤Ⅳ中,将MnO2混入右侧支管有余热的KClO3中的操作方法是将
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐2】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下实验:
Ⅰ、将 xg氯酸钾与 1.0gMnO2均匀混合加热
Ⅱ、将 3.0g氯酸钾与 1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生 O2的快慢.则:Ⅰ中 x的值应为______ ;此实验所用的实验方法为________ ;
(2)乙探究了影响过氧化氢分解速度的某种因素实验数据记录如下:
实验结论:在相同条件下,___________ ;请写出该反应的表达式(或文字表达式):___________ .
(3)丙分别等体积等浓度的双氧水与等量的二氧化锰和氧化铜作用,比较谁的催化效果好实验中应通过比较___________ 就能达到实验目的.

(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下实验:
Ⅰ、将 xg氯酸钾与 1.0gMnO2均匀混合加热
Ⅱ、将 3.0g氯酸钾与 1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生 O2的快慢.则:Ⅰ中 x的值应为
(2)乙探究了影响过氧化氢分解速度的某种因素实验数据记录如下:
| 双氧水的质量 | 过氧化氢的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
(3)丙分别等体积等浓度的双氧水与等量的二氧化锰和氧化铜作用,比较谁的催化效果好实验中应通过比较

您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐1】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。

探究:该气体的成分
【猜想与假设】小华说;该气体可能是CO2、O2、CO、H2、N2。
小明现:不可能含有N2,因为______ 。
小芳说:不可能含有CO和H2,因为从安全角度考虑。H2易燃易爆,CO有毒。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
【得出结论】(1)由实验①可知,该气体中肯定含有______ 。
(2)由实验②______ (填“能”或“不能”)确定该气体中不含氧气,理由是______ 。

探究:该气体的成分
【猜想与假设】小华说;该气体可能是CO2、O2、CO、H2、N2。
小明现:不可能含有N2,因为
小芳说:不可能含有CO和H2,因为从安全角度考虑。H2易燃易爆,CO有毒。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(2)由实验②
您最近一年使用:0次
科学探究题
|
较易
(0.85)
【推荐2】根据金属活动顺序,只有排在前面的金属才能把排在后面的金属从它的盐溶液中置换出来。小芬同学从实验室中找来了一小块钠放在硫酸铜溶液中,结果发现:有大量的气泡产生,同时生成蓝色沉淀。根据所学的知识,蓝色沉淀可能是__________ 。
对所生成的气体,同学们有以下猜想:
猜想一:生成的气体可能是氢气 猜想二:生成的气体可能是氧气
猜想三:生成的气体可能是二氧化碳。
其中猜想__________ 是不正确的,因为__________ 。
请你对猜想二进行探究:
反思:活泼金属(如钾、钙、钠)与盐溶液反应时,反应比较复杂,不属于置换反应。
对所生成的气体,同学们有以下猜想:
猜想一:生成的气体可能是氢气 猜想二:生成的气体可能是氧气
猜想三:生成的气体可能是二氧化碳。
其中猜想
请你对猜想二进行探究:
| 操作方法 | 实验现象 | 结论 |
反思:活泼金属(如钾、钙、钠)与盐溶液反应时,反应比较复杂,不属于置换反应。
您最近一年使用:0次
科学探究题
|
较易
(0.85)
真题
【推荐3】小李将实验剩余的FeCl3溶液倒入含有H2O2的废液缸,立即产生大量的无色气泡。
(1)小李根据组成的元素猜测,无色气体可能是H2、O2、HCl、Cl2中的一种或多种。
【查阅资料】1.Cl2是黄绿色、有刺激性气味的气体 2.FeCl3在水中解离出Fe3+、Cl-
根据资料,小李可排除的气体为______
【实验一】为进一步验证该气体成分,他用燃着的木条伸入收集满该气体的小试管中,只观察到木条燃得更旺,则该气体一定含_______ 。
(2)小李认为上诉过程中FeCl3溶液作了H2O2分解的催化剂。
【实验二】为了进一步探究哪种离子起催化作用,他做了下图所示的对比实验。若要证明FeCl3溶液中的Fe3+对HO2分解起催化作用,除观察到试管c中无明显现象外,还需观察到的现象为______ 。
【实验三】_____
【得出结论】要证明FeCl3溶液作H2O2分解的催化剂,须满足一下两个方面的条件:
①从定性角度需观察到______ (填序号)的现象。A.实验一 B.实验二 C.实验三
②从定量角度需得到的关系式为m1=______ (用m2和m3表示)。
(1)小李根据组成的元素猜测,无色气体可能是H2、O2、HCl、Cl2中的一种或多种。
【查阅资料】1.Cl2是黄绿色、有刺激性气味的气体 2.FeCl3在水中解离出Fe3+、Cl-
根据资料,小李可排除的气体为
【实验一】为进一步验证该气体成分,他用燃着的木条伸入收集满该气体的小试管中,只观察到木条燃得更旺,则该气体一定含
(2)小李认为上诉过程中FeCl3溶液作了H2O2分解的催化剂。
【实验二】为了进一步探究哪种离子起催化作用,他做了下图所示的对比实验。若要证明FeCl3溶液中的Fe3+对HO2分解起催化作用,除观察到试管c中无明显现象外,还需观察到的现象为
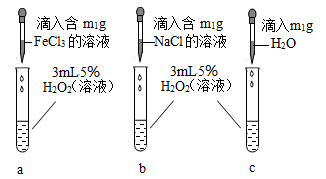
【实验三】
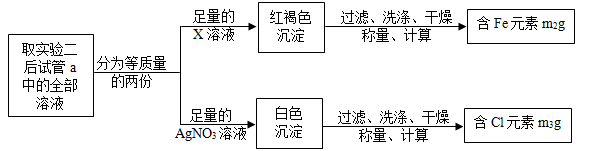
【得出结论】要证明FeCl3溶液作H2O2分解的催化剂,须满足一下两个方面的条件:
①从定性角度需观察到
②从定量角度需得到的关系式为m1=
您最近一年使用:0次
科学探究题
|
较易
(0.85)
名校
解题方法
【推荐1】天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】甲:CO2、 H2O 乙:CO 、H2O 丙:NH3、 CO2 、H2O 丁:CO2、 CO 、H2O
你认为_______ 同学的猜想是错误的,理由是_______ 。
【实验探究】:为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:

(1)A、B装置的顺序能否颠倒?(填“能”或“否”)_______ 。
(2)实验中用纯净O2而不用空气的原因是_______ 。
(3)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断_______ 同学猜想成立。
(4)请写出C中红色粉末变成黑色的化学方程式:_______ 。
【反思与交流】为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是____ 。
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】甲:CO2、 H2O 乙:CO 、H2O 丙:NH3、 CO2 、H2O 丁:CO2、 CO 、H2O
你认为
【实验探究】:为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:

(1)A、B装置的顺序能否颠倒?(填“能”或“否”)
(2)实验中用纯净O2而不用空气的原因是
(3)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断
(4)请写出C中红色粉末变成黑色的化学方程式:
【反思与交流】为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是
您最近一年使用:0次
科学探究题
|
较易
(0.85)
解题方法
【推荐2】纯碱在生产和生活中有广泛的用途。某化学兴趣小组对纯碱的制备、性质及用途等开展项目式学习。
任务一:了解纯碱的制备——“侯氏制碱法”
“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠和氯化铵,再加热碳酸氢钠即可制得纯碱。
(1)饱和氯化钠溶液吸收的两种气体是(填字母)。
任务二:探究纯碱的性质
【查阅资料】氯化钙溶液呈中性。
同学们分别取一定量的碳酸钠溶液于4支试管中,进行如图所示的实验。

(2)四支试管中均发生了化学反应,写出试管②中发生反应的化学方程式_______ 。
实验结束后,同学们将四支试管中的物质全部倒入洁净的废液缸中,充分反应后,静置,得到白色沉淀和无色上层清液。
【提出问题】上层清液中除酚酞外所含的溶质是什么?
【猜想假设】
(3)小明作出了如下猜想:上层清液中一定含有NaCl;一定没有碳酸钠,氢氧化钠、氢氧化钙、稀盐酸;可能含有_______ 。
【进行实验】
(4)为确定“可能含有的物质”是否存在,小组同学分别进行了如表实验,均得出了“可能含有的物质”存在的结论。
【评价与反思】
(5)通过分析,小组同学一致认为小红的实验不可靠,原因是_______ 。
任务三:了解纯碱的用途
(6)纯碱具有广泛应用。下列属于纯碱用途的是(填字母)。
任务一:了解纯碱的制备——“侯氏制碱法”
“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠和氯化铵,再加热碳酸氢钠即可制得纯碱。
(1)饱和氯化钠溶液吸收的两种气体是(填字母)。
| A.Cl2 | B.NH3 | C.SO2 | D.CO2 |
任务二:探究纯碱的性质
【查阅资料】氯化钙溶液呈中性。
同学们分别取一定量的碳酸钠溶液于4支试管中,进行如图所示的实验。

(2)四支试管中均发生了化学反应,写出试管②中发生反应的化学方程式
实验结束后,同学们将四支试管中的物质全部倒入洁净的废液缸中,充分反应后,静置,得到白色沉淀和无色上层清液。
【提出问题】上层清液中除酚酞外所含的溶质是什么?
【猜想假设】
(3)小明作出了如下猜想:上层清液中一定含有NaCl;一定没有碳酸钠,氢氧化钠、氢氧化钙、稀盐酸;可能含有
【进行实验】
(4)为确定“可能含有的物质”是否存在,小组同学分别进行了如表实验,均得出了“可能含有的物质”存在的结论。
| 实验操作 | 实验现象 | |
| 小亮的实验 | 取少量上层清液于试管中,向其中加入适量碳酸钠溶液 | |
| 小红的实验 | 取少量上层清液于试管中,向其中加入适量硝酸银溶液 | 产生白色沉淀 |
【评价与反思】
(5)通过分析,小组同学一致认为小红的实验不可靠,原因是
任务三:了解纯碱的用途
(6)纯碱具有广泛应用。下列属于纯碱用途的是(填字母)。
| A.用于生产玻璃 | B.用作食品干燥剂 |
| C.用于配制农药波尔多液 | D.用于改良酸性土壤 |
您最近一年使用:0次

 氢氧化钾溶液的烧杯中滴加几滴酚酞溶液,可观察到的现象是
氢氧化钾溶液的烧杯中滴加几滴酚酞溶液,可观察到的现象是


