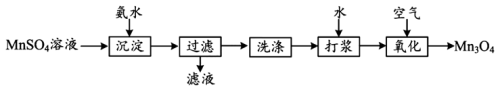
锰元素能形成MnO、MnO2、Mn2O3和Mn3O4等多种氧化物,其中Mn3O4是重要的结构材料。工业用硫酸锰(MnSO4)制备Mn3O4的流程如下:
(1)“沉淀”反应是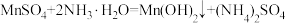 。该反应的基本类型为
。该反应的基本类型为________ 。
(2)写出“过滤”所得滤液的一种用途:____________ 。
(3)将Mn(OH)2加水“打浆”制成悬浊液,可加快“氧化”反应速率的原因是__________________ 。
(4)“氧化”时,Mn(OH)2与空气中的氧气在60℃条件下反应生成Mn3O4,该反应的化学方程式为_______________ 。
(5)通过测定固体产物中锰元素质量分数来推断产物成分。“氧化”所得固体产物中锰元素质量分数随通空气时间的变化如图所示。
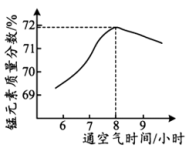
通空气8小时左右,所得固体几乎全部为Mn3O4.推出该结论的依据是______________ 。

(1)“沉淀”反应是
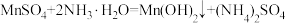 。该反应的基本类型为
。该反应的基本类型为(2)写出“过滤”所得滤液的一种用途:
(3)将Mn(OH)2加水“打浆”制成悬浊液,可加快“氧化”反应速率的原因是
(4)“氧化”时,Mn(OH)2与空气中的氧气在60℃条件下反应生成Mn3O4,该反应的化学方程式为
(5)通过测定固体产物中锰元素质量分数来推断产物成分。“氧化”所得固体产物中锰元素质量分数随通空气时间的变化如图所示。

通空气8小时左右,所得固体几乎全部为Mn3O4.推出该结论的依据是
2023·湖北武汉·模拟预测 查看更多[2]
更新时间:2023-03-30 10:27:47
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】已知A~G是初中化学常见的七种物质,其中B、C、D含有一种相同的元素,E、F、G含有同一种金属元素,A 常用于制玻璃、洗涤剂,B 是胃酸的主要成分,C 是密度最小的单质,F 是常见建筑材料的主要成分,相互间存在如图所示的反应与转化关系“—”表示反应关系,“→”表示转化系。请问:

(1)写出物质F 的化学式__________ 。
(2)物质G的一种用途是__________ 。
(3)B和E发生的反应、属于__________ 反应。(填基本反应类型)
(4)A与G发生的反应的化学方程式为__________ 。

(1)写出物质F 的化学式
(2)物质G的一种用途是
(3)B和E发生的反应、属于
(4)A与G发生的反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
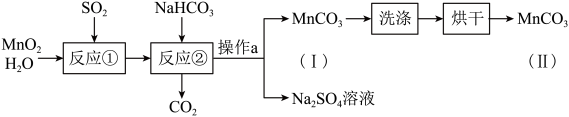
【推荐2】某化学活动小组在实验室以 MnO2固体为原料制取少量 MnCO3,基本流程如下:
(1)操作 a 要用到的实验用品中,除玻璃仪器以外,还有______________ (填一种具体的实验用品)。
(2)反应①为化合反应,产物为 MnSO4该反应的化学方程式为____________ ,下列物质中能与 MnSO4反应的有_____________ 。
A.稀硫酸 B.BaCl2 C.盐酸 D.Na2CO3
(3)反应②的基本反应类型为_____________ 反应。
(4)产品 MnCO3(II)比 MnCO3(I)更纯净,原因是产品 MnCO3(I)经过洗涤、烘干以后,表面附着的______ (填化学式)及______ (填化学式)等杂质已被除去。
(5)为了获得纯净的 MnCO3烘干时需要控制的条件是___________ 。
(1)操作 a 要用到的实验用品中,除玻璃仪器以外,还有
(2)反应①为化合反应,产物为 MnSO4该反应的化学方程式为
A.稀硫酸 B.BaCl2 C.盐酸 D.Na2CO3
(3)反应②的基本反应类型为
(4)产品 MnCO3(II)比 MnCO3(I)更纯净,原因是产品 MnCO3(I)经过洗涤、烘干以后,表面附着的
(5)为了获得纯净的 MnCO3烘干时需要控制的条件是
您最近一年使用:0次
【推荐3】I、价类二维图反映的是元素的化合价与物质类别之间的关系,构建价类二维图是化学学习的重要方法,如图是某同学绘制的关于氯元素的价类二维图(第I题图)。请完成下列问题。
第Ⅰ题图:
第Ⅱ题图:
(1)X处的物质类别为______ ,B的化学式为______ ,C的化学式为______ 。
(2)A与氢氧化钠反应生成D和水,该反应属于基本反应类型中的______ 。
(3)实验室可用A的浓溶液和浓碳酸钠溶液制作简易泡沫灭火器,是利用______ 能灭火的原理,它之所以可以灭火,原因之一是利用其______ 的化学性质。
(4)E物质常用于实验室制氧气, 同时生成KCl, 该反应的化学方程式是______ 。
Ⅱ、
(5)已知Fe、Mn、Ag三种金属存在如图所示的转化关系(第Ⅱ题图),则三种金属的活动性由强到弱的顺序是______ ,欲验证三种金属的活动性顺序,可选用的一组药品为Mn、Ag和______ 溶液。
第Ⅰ题图:

第Ⅱ题图:

(1)X处的物质类别为
(2)A与氢氧化钠反应生成D和水,该反应属于基本反应类型中的
(3)实验室可用A的浓溶液和浓碳酸钠溶液制作简易泡沫灭火器,是利用
(4)E物质常用于实验室制氧气, 同时生成KCl, 该反应的化学方程式是
Ⅱ、
(5)已知Fe、Mn、Ag三种金属存在如图所示的转化关系(第Ⅱ题图),则三种金属的活动性由强到弱的顺序是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D、E为初中化学常见的五种物质,它们之间存在如图所示的关系(“→”表示物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)。请回答下列问题:

(1)若A、B为组成元素相同的气体,E为大理石的主要成分,A物质的用途______ 。则B的化学式为______ ,物质D的类别为______ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)若A是能供给人类呼吸的气体,B是一种最常用的溶剂,D的水溶液显蓝色。则C-D反应的基本类型是______ ,D-E反应的化学方程式是______ 。

(1)若A、B为组成元素相同的气体,E为大理石的主要成分,A物质的用途
(2)若A是能供给人类呼吸的气体,B是一种最常用的溶剂,D的水溶液显蓝色。则C-D反应的基本类型是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源。煤气化和液化流程示意图如图所示
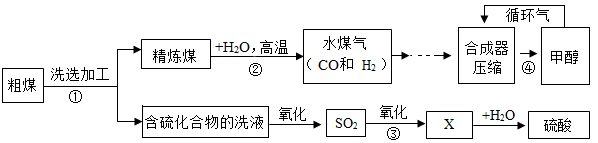
(1) 第①步操作发生的是_____ (填“物理”或“化学”)变化。
(2)步骤③中,SO2 进一步氧化得到 X,X为硫的另一种氧化物,其中硫元素的化合价为+6 价,X的化学式为_____ 。
(3)经过进一步净化,含较多杂质的水煤气转化为合成气(CO和 H2 的混合气体),步骤④中生成的甲醇(CH3OH)是一种重要的化工原料,该反应的化学方程式为_____ ,该反应的基本类型是_____ 。
(4)循环气的主要成分是_____ 和少量未完全分离出去的甲醇。
(5)从“绿色化学”的角度分析,“煤的气化和液化”流程的优点:_____ 。

(1) 第①步操作发生的是
(2)步骤③中,SO2 进一步氧化得到 X,X为硫的另一种氧化物,其中硫元素的化合价为+6 价,X的化学式为
(3)经过进一步净化,含较多杂质的水煤气转化为合成气(CO和 H2 的混合气体),步骤④中生成的甲醇(CH3OH)是一种重要的化工原料,该反应的化学方程式为
(4)循环气的主要成分是
(5)从“绿色化学”的角度分析,“煤的气化和液化”流程的优点:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】我国是全球规模最大的禽蛋生产国和消费国。对蛋壳(主要成分为碳酸钙)中的钙源进行回收利用,可以变废为宝。蛋壳高温煅烧法制备乳酸钙的工艺流程如图。

已知反应②: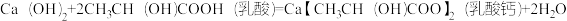
(1)蛋壳是生物活性钙源,含人体所需的硒,其属于___________ (选填“常量”或“微量”)元素。
(2)写出反应①的化学反应方程式:___________ 。
(3)②中“搅拌”的作用是___________ 。
(4)某兴趣小组取4g“灰分”与乳酸反应,研究结果如图,其最佳反应条件是___________(填标号)。

(5)已知一个鸡蛋壳约5g,蛋壳中碳酸钙含量约90%。某品牌乳酸钙产品,每瓶180粒,每粒含钙元素400mg,采用鸡蛋壳作为唯一钙源,制备这样一瓶钙片至少需要___________ 个鸡蛋壳。

已知反应②:
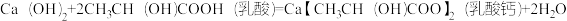
(1)蛋壳是生物活性钙源,含人体所需的硒,其属于
(2)写出反应①的化学反应方程式:
(3)②中“搅拌”的作用是
(4)某兴趣小组取4g“灰分”与乳酸反应,研究结果如图,其最佳反应条件是___________(填标号)。

| A.34℃时,加12mL乳酸,反应75分钟 |
| B.35℃时,加11.5mL乳酸,反应70分钟 |
| C.35℃时,加12mL乳酸,反应75分钟 |
(5)已知一个鸡蛋壳约5g,蛋壳中碳酸钙含量约90%。某品牌乳酸钙产品,每瓶180粒,每粒含钙元素400mg,采用鸡蛋壳作为唯一钙源,制备这样一瓶钙片至少需要
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】尿素是重要的氮肥,利用空气、水和煤等原料合成尿素【CO(NH2)2】的流程如图所示。
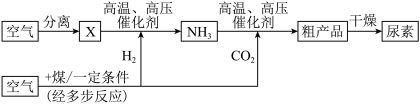
(1)X的化学式为_______ ,约占空气体积的_______ 。
(2)“多步反应”过程中,煤的主要成分碳体现了_______ (填“氧化性”或“还原性”)。
(3)NH3和CO2反应的化学方程式为

 ,生产900t尿素【CO(NH2)2】,需要NH3的质量是多少?
,生产900t尿素【CO(NH2)2】,需要NH3的质量是多少?
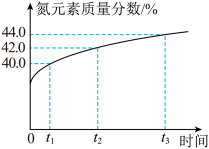
(4)产物中含有尿素和水,对产品进行干燥后得到900t不含水的尿素,在干燥的过程中用氮元素含量测定仪跟踪测试得到图。则t1时刻产品中水的质量为_______ t。

(1)X的化学式为
(2)“多步反应”过程中,煤的主要成分碳体现了
(3)NH3和CO2反应的化学方程式为


 ,生产900t尿素【CO(NH2)2】,需要NH3的质量是多少?
,生产900t尿素【CO(NH2)2】,需要NH3的质量是多少?(4)产物中含有尿素和水,对产品进行干燥后得到900t不含水的尿素,在干燥的过程中用氮元素含量测定仪跟踪测试得到图。则t1时刻产品中水的质量为

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】高纯氧化铁可作为现代电子工业的材料,以下是硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:[(NH4)2CO3溶液呈碱性,40℃以上时(NH4)2CO3分解]。
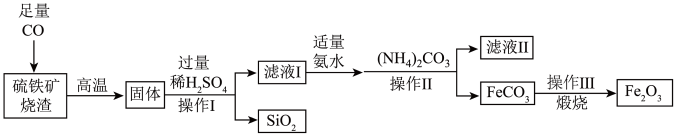
(1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器玻璃棒、_______ 、烧杯等。
(2)写出通入CO后所发生反应的化学方程式_______ (任意写一个)。
(3)在该生产流程中当加入(NH4)2CO3后,应该控制的条件是______ 。
(4)滤液Ⅱ中可回收的物质在农业上可做_____
(5)写出在空气中煅烧FeCO3的化学方程式_____ 。

(1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器玻璃棒、
(2)写出通入CO后所发生反应的化学方程式
(3)在该生产流程中当加入(NH4)2CO3后,应该控制的条件是
(4)滤液Ⅱ中可回收的物质在农业上可做
(5)写出在空气中煅烧FeCO3的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
【推荐2】完成下列变化的化学方程式,并按要求填空。
(1)镁条在空气中燃烧_______________ ,点燃镁条时使用的夹持仪器是________ 。
(2)实验室用6%的过氧化氢溶液与二氧化锰混合制氧气_____________ ,6%的过氧化氢溶液中氢元素的质量分数为____________ 。(计算结果精确到0.1%)
(3)氨水与硫酸反应_______________________ ,生成的盐可用作________ 肥(填写化肥种类)。
(4)一氧化碳在高温下与氧化铁反应_______________ ,反应前后气体的化学计量数之比为_______________ 。
(5)受到猛烈撞击时,硝酸铵会迅速分解生成一氧化二氮气体和另一种氧化物___________ ,一氧化二氮中氮元素的化合价为____________________ 。
(1)镁条在空气中燃烧
(2)实验室用6%的过氧化氢溶液与二氧化锰混合制氧气
(3)氨水与硫酸反应
(4)一氧化碳在高温下与氧化铁反应
(5)受到猛烈撞击时,硝酸铵会迅速分解生成一氧化二氮气体和另一种氧化物
您最近一年使用:0次



