铁红(Fe2O3)常用于油漆、油墨及橡胶工业。《唐本草》等古籍记载着中国很早就能煅烧硫酸亚铁晶体制备铁红,现代可以用废铁屑制取铁红,工艺流程如下:
(1)把废铁屑粉碎后再加入硫酸溶液,其目的是_______ 。(写一条)
(2)“沉淀”过程,要控制反应温度不宜过高,其原因是_______ 。
(3)证明滤液中含有 :取适量滤液于试管中,
:取适量滤液于试管中,_______ (写出操作和现象)。
(4)在空气中“煅烧”FeCO3,生成Fe2O3和CO2,该反应化学方程式为_______ 。
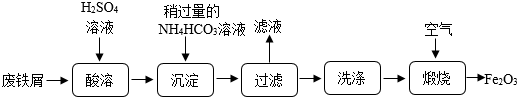
(1)把废铁屑粉碎后再加入硫酸溶液,其目的是
(2)“沉淀”过程,要控制反应温度不宜过高,其原因是
(3)证明滤液中含有
 :取适量滤液于试管中,
:取适量滤液于试管中,(4)在空气中“煅烧”FeCO3,生成Fe2O3和CO2,该反应化学方程式为
2023·江苏徐州·一模 查看更多[4]
2023年江苏省徐州市中考一模化学试题(已下线)2023年中考押题预测卷02(徐州卷)-化学2024年江苏省徐州市沛县第五中学中考模拟化学试题 2024年江苏省徐州市铜山区柳新镇中心中学中考模拟化学试题
更新时间:2023-04-15 12:24:56
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
【推荐1】在“宏观一微观一符号”之间建立联系,是化学特有的思维方式。
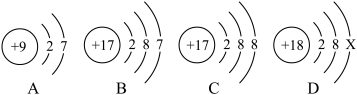
(1)上图是四种粒子结构示意图。
① 中的
中的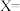
______ ,C粒子的符号为______ 。
② 、B、C、D中属于同种元素的粒子是
、B、C、D中属于同种元素的粒子是______ 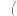 填序号
填序号 。
。
(2)汽车尾气催化转换器可减少有害气体排放,其反应过程的微观变化如图所示。

①已知丁是一种单质,则丁是______ (写化学式)。
②根据图示得出的结论中,正确的有______ 。
A 化学反应是原子的重组过程 B 该反应是置换反应
C 参加反应的甲和乙的质量比为14:15 D 生成丙和丁的分子个数为1:1
③写出该反应的化学方程式:______ 。

(1)上图是四种粒子结构示意图。
①
 中的
中的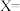
②
 、B、C、D中属于同种元素的粒子是
、B、C、D中属于同种元素的粒子是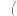 填序号
填序号 。
。(2)汽车尾气催化转换器可减少有害气体排放,其反应过程的微观变化如图所示。

①已知丁是一种单质,则丁是
②根据图示得出的结论中,正确的有
A 化学反应是原子的重组过程 B 该反应是置换反应
C 参加反应的甲和乙的质量比为14:15 D 生成丙和丁的分子个数为1:1
③写出该反应的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】某科学兴趣小组查阅资料得知镁可在以下三种气体中燃烧,其化学方程式为:



(1)上述三个化学反应中镁元素都是由O价变为_____ 价。
(2)已知氮化镁是黄绿色固体,而镁在空气中燃烧生成的主要是白色固体,由此可以推测,氧气和氮气相比较,较活泼的是_____ 。
(3)氮化镁与水反应,生成一种难溶于水的碱和一种气体, 把该气体通入无色的酚酞试溶中,可观察到无色酚酞试液变红色,试写出氮化镁与水反应的化学方程式为_____ 。
(4)根据化学方程式猜想:镁在二氧化碳气体中燃烧的现象为_____ 。(至少写出两种现象)。
(5)依据上述信息和所学知识判定,下列说法中正确的是_____ (填字母)。
a、可燃物燃烧不一定与氧气接触
b、不能用镁条代替红磷测量空气中氧气的含量
c、生产金属镁的工厂应该准备充足的液态二氧化碳灭火器
d、镁原子最外层有两个电子,易失去电子变成镁离子,所以镁是一种活泼金属



(1)上述三个化学反应中镁元素都是由O价变为
(2)已知氮化镁是黄绿色固体,而镁在空气中燃烧生成的主要是白色固体,由此可以推测,氧气和氮气相比较,较活泼的是
(3)氮化镁与水反应,生成一种难溶于水的碱和一种气体, 把该气体通入无色的酚酞试溶中,可观察到无色酚酞试液变红色,试写出氮化镁与水反应的化学方程式为
(4)根据化学方程式猜想:镁在二氧化碳气体中燃烧的现象为
(5)依据上述信息和所学知识判定,下列说法中正确的是
a、可燃物燃烧不一定与氧气接触
b、不能用镁条代替红磷测量空气中氧气的含量
c、生产金属镁的工厂应该准备充足的液态二氧化碳灭火器
d、镁原子最外层有两个电子,易失去电子变成镁离子,所以镁是一种活泼金属
您最近一年使用:0次
【推荐3】根据如图所示的实验回答下列问题。

(1)甲图实验中仪器①的名称是______ ,若利用该装置在实验室制取氧气,反应的化学方程式为______ 。
(2)乙是硫燃烧的实验,集气瓶中水的作用是______ 。
(3)丙是配制质量分数为6%的氯化钠溶液过程中的称量操作。称量过程中,若观察到托盘天平的指针向右偏时,应进行的操作是______ ;若选用食用碘盐配制该溶液,则所得溶液中氯化钠的质量分数______ (填“大于”“小于”或“等于”)6%。

(1)甲图实验中仪器①的名称是
(2)乙是硫燃烧的实验,集气瓶中水的作用是
(3)丙是配制质量分数为6%的氯化钠溶液过程中的称量操作。称量过程中,若观察到托盘天平的指针向右偏时,应进行的操作是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】为了保护环境,某村办企业需对含硫酸的废水处理呈中性后排放。
(1)若要达到排放标准,可以向废水里加入 (填字母)。
(2)某同学欲利用该村的赤铁矿(杂质不溶于水,也不与酸反应)来处理废水,并制取红色颜料(Fe2O3)从而变废为宝。他设计了如下方案,试回答相关问题。(已知:不溶于水的碱受热易分解为两种氧化物,且化合价不变)。

反应①的化学方程式是______ 。反应③是分解反应,除Fe2O3外,另一种产物的名称是____ 。
(1)若要达到排放标准,可以向废水里加入 (填字母)。
| A.氯化钠 | B.氯化钡 | C.生石灰 |
(2)某同学欲利用该村的赤铁矿(杂质不溶于水,也不与酸反应)来处理废水,并制取红色颜料(Fe2O3)从而变废为宝。他设计了如下方案,试回答相关问题。(已知:不溶于水的碱受热易分解为两种氧化物,且化合价不变)。

反应①的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】硫酸铜晶体常于配制农药波尔多液。以下是用废黄铜料(含锌)生产硫酸铜晶体的流程。______ 。
(2)操作 需要用到玻璃棒,其作用为
需要用到玻璃棒,其作用为______ 。③的化学反应方程式为______ ,该反应的基本类型是______ 。
(3)已知: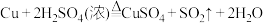 。从经济和环保的角度分析,对比途径Ⅱ,途径Ⅰ的优点有:
。从经济和环保的角度分析,对比途径Ⅱ,途径Ⅰ的优点有:______ 。
(4)随着科学技术的发展及环境保护意识的提升,“生物炼铜”技术逐渐兴起。以辉铜矿(主要成分为 )为原料也可制得
)为原料也可制得 ,其反应原理为
,其反应原理为 ,则
,则 的化学式为
的化学式为______ 。
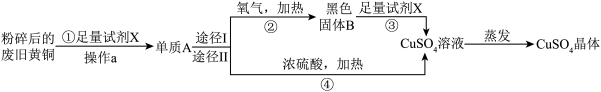
(2)操作
 需要用到玻璃棒,其作用为
需要用到玻璃棒,其作用为(3)已知:
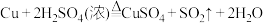 。从经济和环保的角度分析,对比途径Ⅱ,途径Ⅰ的优点有:
。从经济和环保的角度分析,对比途径Ⅱ,途径Ⅰ的优点有:(4)随着科学技术的发展及环境保护意识的提升,“生物炼铜”技术逐渐兴起。以辉铜矿(主要成分为
 )为原料也可制得
)为原料也可制得 ,其反应原理为
,其反应原理为 ,则
,则 的化学式为
的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】(1)构建知识网络是化学学习中重要的学习方法,小玲同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:

①图中①的现象是______ ;
②若用湿润的PH试纸测定盐酸的PH,则结果会______ (填“偏大”“偏小”“无影响”)
③写出一个符合图中②的化学方程式______ ;
④图中③的性质在工业上可用于除锈,试写出铁锈和适量盐酸反应化学方程式____________ 。
(2)符合下列要求的物质,将化学式填在空格中:
①最常用的溶剂____________ ;
②可用作食品干燥剂的氧化物___________ ;
③家庭厨房中的一种酸_________ ;
④碱溶液中都含有的阴离子____________ ;

①图中①的现象是
②若用湿润的PH试纸测定盐酸的PH,则结果会
③写出一个符合图中②的化学方程式
④图中③的性质在工业上可用于除锈,试写出铁锈和适量盐酸反应化学方程式
(2)符合下列要求的物质,将化学式填在空格中:
①最常用的溶剂
②可用作食品干燥剂的氧化物
③家庭厨房中的一种酸
④碱溶液中都含有的阴离子
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】从大理石(主要杂质是氧化铁)中提纯碳酸钙的一种实验流程如下:

(1)用硝酸不用稀硫酸的主要原因是______ 。
(2)硝酸与氧化铁反应的化学方程式是______ 。
(3)生成碳酸钙的化学方程式是______ 。
(4)第二次过滤所得滤液在农业生产中的一种用途是______ 。

(1)用硝酸不用稀硫酸的主要原因是
(2)硝酸与氧化铁反应的化学方程式是
(3)生成碳酸钙的化学方程式是
(4)第二次过滤所得滤液在农业生产中的一种用途是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】某固体物质可能含有氯化铁、氢氧化钾、硝酸镁、硫酸钾、氯化钠中的一种或几种,为确定样品的成分,做如下实验:
①取少量该固体样品,加入足量水,完全溶解,得到无色溶液a。
②取少量a溶液于试管中,向其中滴加少量硝酸铁溶液,产生红褐色沉淀。
③另取少量a溶液于试管中,向其中滴加少量的氯化钡溶液,产生白色沉淀。
据此推断,该固体物质中一定含有(写化学式,下同)_______ ,可能含有的物质是_______ ;请写出步骤(3)中发生反应的化学方程式_______ ;为确定可能含有的成分是否存在,以无色溶液a为原料,依次需要用到的试剂为:_______ 。
①取少量该固体样品,加入足量水,完全溶解,得到无色溶液a。
②取少量a溶液于试管中,向其中滴加少量硝酸铁溶液,产生红褐色沉淀。
③另取少量a溶液于试管中,向其中滴加少量的氯化钡溶液,产生白色沉淀。
据此推断,该固体物质中一定含有(写化学式,下同)
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】海水中含有大量盐类,海水淡化是综合利用海洋资源的重要产业。某种海水淡化装置允许水分子透过,阻止盐类透过。采用该装置淡化海水,可分别获得浓盐水和淡水。
(1)①进入淡化装置前的海水必须进行预处理,可用纯碱除去大部分钙盐和镁盐,写出纯碱与CaCl2生成沉淀的化学方程式_____ 。
②该方法除了用于海水淡化,还可用于_____ 。
A.硬水软化 B.污水处理 C.物质鉴别
(2)某工厂淡化海水后得到的浓盐水和淡水中盐类物质含量如下表(微量盐类忽略不计)。国家规定居民生活用水中盐类物质总含量≤500mg·L-1,计算并推断所得淡水中盐类总含量_____ 生活用水的标准(填“达到”或“未达到”);该工厂一套淡化装置每小时产生浓盐水300L,其中含有NaCl_____ kg。
(3)淡化海水所得的浓盐水中含大量MgCl2可制备金属镁,主要物质转化关系如图所示:

①写出生成Mg(OH)2的反应方程式_____ 。
②浓盐水经过步骤1和2两步反应后又获得了MgCl2,设计这两步的目的是_____ 。
③图中未涉及的反应类型为_____ 。
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
④镁在空气中燃烧发出耀眼白光,依据此现象可用镁制作_____ (写出一种即可)。
(1)①进入淡化装置前的海水必须进行预处理,可用纯碱除去大部分钙盐和镁盐,写出纯碱与CaCl2生成沉淀的化学方程式
②该方法除了用于海水淡化,还可用于
A.硬水软化 B.污水处理 C.物质鉴别
(2)某工厂淡化海水后得到的浓盐水和淡水中盐类物质含量如下表(微量盐类忽略不计)。国家规定居民生活用水中盐类物质总含量≤500mg·L-1,计算并推断所得淡水中盐类总含量
 | 氯化钠 | 氯化镁 | 硫酸镁 | 硫酸钙 |
| 淡水 | 0.17 | 0.012 | 4.8×10-9 | 8.5×10-9 |
| 浓盐水 | 45.0 | 3.6 | 3.3 | 0.14 |

①写出生成Mg(OH)2的反应方程式
②浓盐水经过步骤1和2两步反应后又获得了MgCl2,设计这两步的目的是
③图中未涉及的反应类型为
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
④镁在空气中燃烧发出耀眼白光,依据此现象可用镁制作
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】有A、B两种固体物质,A是一种化肥,B广泛用作食品干燥剂.把A、B分别放入水中,前者所得溶液温度显著降低,后者与水反应生成C并放出大量热;将A与C的粉末混合、研磨,会嗅到刺鼻的氨味.
(1)则A物质是_____ ,B物质是_____ ;
(2)A物质属于化肥中的_____ 肥(选填“氮”、“磷”或“钾”);
(3)指出C物质在农业生产中的一种用途:_____ ;
(4)把A放入水中所得溶液温度显著降低的原因是_____ ;
(5)B与水反应的化学方程式是_____ ,反应类型是_____ 反应.
(1)则A物质是
(2)A物质属于化肥中的
(3)指出C物质在农业生产中的一种用途:
(4)把A放入水中所得溶液温度显著降低的原因是
(5)B与水反应的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】根据如图所示实验回答下列问题:

(1)甲实验中两支试管里分别盛有相同温度的水。该实验的目的是_______ 。
(2)乙实验配制50g10%的氯化钠溶液,量取水的操作如图所示,其他操作都正确,所配溶液中氯化钠的质量分数_______ (选填“>”、“=”或“<”)10%。
(3)丙实验验证了硫酸铵的物理性质:_______ (答一条即可);化学性质:_______ 。

(1)甲实验中两支试管里分别盛有相同温度的水。该实验的目的是
(2)乙实验配制50g10%的氯化钠溶液,量取水的操作如图所示,其他操作都正确,所配溶液中氯化钠的质量分数
(3)丙实验验证了硫酸铵的物理性质:
您最近一年使用:0次



