根据NaCl和KNO3的部分溶解度数据,回答下列问题:
(1)0℃时,NaCl的溶解度为______ g 可得影响溶解度的因素有______ (任写一点即可)。
(2)KNO3中混有少量NaCl时,提纯硝酸钾的方法是______ 。
(3)按照下图进行实验,各步操作均已充分溶解,实验过程中溶剂的挥发不计

①a和b中溶质的质量分数:a______ b(用“<”“>”“=”填空,下同);a和d中溶剂质量:a______ d;如c和f上层清液溶质质量分数相等,则t℃的最小范围是______ 。
②e中溶质质量分数为______ ,b中是否是该温度下硝酸钾的饱和溶液?______ (填“是”“否”“不一定”)。
温度/℃ | 0 | 20 | 40 | |
溶解度g /100g水 | NaCl | 35.7 | 36.0 | 36.6 |
KNO3 | 13.3 | 31.6 | 63.9 | |
(1)0℃时,NaCl的溶解度为
(2)KNO3中混有少量NaCl时,提纯硝酸钾的方法是
(3)按照下图进行实验,各步操作均已充分溶解,实验过程中溶剂的挥发不计

①a和b中溶质的质量分数:a
②e中溶质质量分数为
更新时间:2023-04-22 12:33:05
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。该技术以从海水中提取出来的食盐(NaCl)为主要原料制取纯碱,同时得到可用作化学肥料的物质氯化铵(NH4Cl)。NaCl和NH4Cl的溶解度曲线如图所示,请回答下列问题。

①t2℃时,NH4Cl的溶解度_____ (填“小于”、“等于”、“大于”之一)NaCl的溶解度。
②交点P表示的一条意义_____ 。
③当NH4Cl固体中含有少量NaCl时,提纯NH4Cl可采用_____ (填“降温结晶”、“蒸发结晶”、“过滤”之一)。

①t2℃时,NH4Cl的溶解度
②交点P表示的一条意义
③当NH4Cl固体中含有少量NaCl时,提纯NH4Cl可采用
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】如图所示为甲、乙两种物质的溶解度曲线。t1℃时,将20g甲物质加入到50g水中,充分溶解后形成的溶液是_____ 。(填“饱和”或“不饱和”)溶液:t2℃时,将70g乙的饱和溶液与30g水混合,所得溶液的溶质质量分数是______ ;若甲的饱和溶液中混有少量乙物质,可通过______ 的方法提纯甲物质。


您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如图为我国古代“布灰种盐”生产海盐的部分场景,其过程为“烧草为灰,布在滩场,然后以海水渍之,俟晒结浮白,扫而复淋”。

(1)“晒结浮白”是指海水浸渍的草灰经日晒后出现白色海盐颗粒的过程,化学上称之为___________ 。
(2)经过多次“扫而复淋”,提高卤水浓度获得“上等卤水”。上等卤水中含有MgC12、KCl和MgSO4等物质,如图是它们的溶解度曲线。

①下列有关说法中正确的是___________ 。
A.MgCl2属于可溶性物质
B.20℃时,MgSO4的溶质质量分数小于MgCl2
C.将t℃时KCl和MgSO4的饱和溶液都降温到20℃,MgSO4溶液析出的晶体多
D.90℃时,将40gMgC12加入50g水中,可得到85g溶液
②现有一瓶t℃时的硫酸镁不饱和溶液,若要使其变成饱和溶液,可采取的方法是___________ (答一条即可)。

(1)“晒结浮白”是指海水浸渍的草灰经日晒后出现白色海盐颗粒的过程,化学上称之为
(2)经过多次“扫而复淋”,提高卤水浓度获得“上等卤水”。上等卤水中含有MgC12、KCl和MgSO4等物质,如图是它们的溶解度曲线。

①下列有关说法中正确的是
A.MgCl2属于可溶性物质
B.20℃时,MgSO4的溶质质量分数小于MgCl2
C.将t℃时KCl和MgSO4的饱和溶液都降温到20℃,MgSO4溶液析出的晶体多
D.90℃时,将40gMgC12加入50g水中,可得到85g溶液
②现有一瓶t℃时的硫酸镁不饱和溶液,若要使其变成饱和溶液,可采取的方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】20℃时,向盛有100g水的甲、乙、丙三个烧杯中,分别加入a、b、c三种物质各30g,充分溶解后,现象如图一所示。继续升高温度,三个烧杯中溶液的溶质质量分数随温度的变化如图二所示。

(1)丙烧杯对应的物质为_____ (填“a”、“b”或“c”)。
(2)20℃时,甲烧杯中剩余固体质量为_____ 。
(3)P点的纵坐标为_____ (保留一位小数)。

(1)丙烧杯对应的物质为
(2)20℃时,甲烧杯中剩余固体质量为
(3)P点的纵坐标为
您最近一年使用:0次
【推荐2】如图是A、B两固体物质的溶解度曲线,在t1℃时,将25gA物质和25gB物质分别加到各盛有50g水的甲、乙两烧杯中。

(1)t1℃时,B形成的溶液为________ 溶液(填饱和或不饱和)。
(2)在t1℃时A物质溶液中,溶质的质量和溶剂的质量比为_________ 。
(3)由t1℃升温到t2℃,要达到饱和,需要增加A、B的质量________ 。(A多、B多、一样多)。

(1)t1℃时,B形成的溶液为
(2)在t1℃时A物质溶液中,溶质的质量和溶剂的质量比为
(3)由t1℃升温到t2℃,要达到饱和,需要增加A、B的质量
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐1】下表是氢氧化钠和氢氧化钙的溶解度数据
(1)为测定X的值,取四份60℃的水各50g,分别进行实验,并记录数据如下:
实验结果分析,可知X的值为_____
(2)去除NaOH溶液中的Ca(OH)2,通过蒸发浓缩、_____ ,然后过滤、洗涤、干燥得到NaOH固体
(3)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复到20℃得到的溶液(乙溶液),此时溶液的溶质质量分数乙_____ 甲(填>、<、=).
(4)在20℃时,向盛有100g水的烧杯中加入111gNaOH,欲使其完全溶解变成不饱和溶液,下列说法中正确的是_____
A 溶液中溶质的质量分数可能不变 B 溶液中溶质的质量分数一定减小
C 溶液中溶质的质量一定增大 D 溶液中溶质的质量分数一定增大
E NaOH的溶解度一定变大 F 可以升温到40℃以上
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaOH | 31 | 91 | 111 | X | 313 | 336 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
(1)为测定X的值,取四份60℃的水各50g,分别进行实验,并记录数据如下:
| 实验编号 | 实验1 | 实验2 | 实验3 | 实验4 | |
| NaOH/g | 50 | 60 | 70 | 80 | |
| H2O/g | 50 | 50 | 50 | 50 | |
| 溶液质量g/ | 100 | 110 | 114.5 | 114.5 | |
实验结果分析,可知X的值为
(2)去除NaOH溶液中的Ca(OH)2,通过蒸发浓缩、
(3)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复到20℃得到的溶液(乙溶液),此时溶液的溶质质量分数乙
(4)在20℃时,向盛有100g水的烧杯中加入111gNaOH,欲使其完全溶解变成不饱和溶液,下列说法中正确的是
A 溶液中溶质的质量分数可能不变 B 溶液中溶质的质量分数一定减小
C 溶液中溶质的质量一定增大 D 溶液中溶质的质量分数一定增大
E NaOH的溶解度一定变大 F 可以升温到40℃以上
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图是甲、乙、丙的溶解度曲线,回答下列问题。
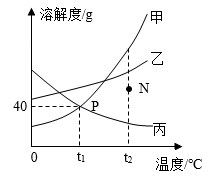
(1)P点的含义是_________ 。
(2)在t1℃时,将30g甲物质加入到50g水中,充分搅拌后溶液的质量为_________ g。
(3)N点表示t2℃时乙的_________ 溶液(填“饱和”或“不饱和”)。
(4)将甲、乙、丙三种物质的饱和溶液分别由t1℃升温到t2℃,所得溶液中溶质的质量分数最大的物质是_________ 。
(5)t2℃时,将甲物质的不饱和溶液转变成饱和溶液可采取的方法有_________ (填一种即可)。

(1)P点的含义是
(2)在t1℃时,将30g甲物质加入到50g水中,充分搅拌后溶液的质量为
(3)N点表示t2℃时乙的
(4)将甲、乙、丙三种物质的饱和溶液分别由t1℃升温到t2℃,所得溶液中溶质的质量分数最大的物质是
(5)t2℃时,将甲物质的不饱和溶液转变成饱和溶液可采取的方法有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】溶液与人们的生产生活密切相关。
(1)下列常见物质不属于溶液的是______ 。(填序号)
A.生理盐水 B.糖水 C.医用酒精 D.牛奶
(2)如图是A物质的溶解度曲线,下表是B物质在不同温度时的溶解度。

①60℃时,A物质的溶解度是______ g。
②50℃时,向100g水中加入40gB物质,充分溶解后得到的是______ (填“饱和”或“不饱和”)溶液,此时溶液的溶质质量分数是______ (计算结果精确到0.1%)。
③请根据表格数据,在A物质溶解度曲线图上绘出B物质的溶解度曲线______ 。
④A、B两种物质溶解度相同时的温度是______ ℃。
(3)将50℃时A、B两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数大小关系为A______ B(填“>”、“=”或者“<”)。
(4)下列说法正确的是______ (填序号)。
①所有物质的溶解度都随温度的升高而增大
②30℃时,物质的溶解度A小于B
③物质A中含有少量B时,可以采用降温结晶的方法提纯A
④40℃时分别将物质A、B的饱和溶液降温至10℃,析出物质的质量A大于B
(1)下列常见物质不属于溶液的是
A.生理盐水 B.糖水 C.医用酒精 D.牛奶
(2)如图是A物质的溶解度曲线,下表是B物质在不同温度时的溶解度。

| 温度/℃ | B物质的溶解度/g |
| 0 | 32 |
| 20 | 35 |
| 40 | 40 |
| 60 | 45 |
| 80 | 55 |
②50℃时,向100g水中加入40gB物质,充分溶解后得到的是
③请根据表格数据,在A物质溶解度曲线图上绘出B物质的溶解度曲线
④A、B两种物质溶解度相同时的温度是
(3)将50℃时A、B两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数大小关系为A
(4)下列说法正确的是
①所有物质的溶解度都随温度的升高而增大
②30℃时,物质的溶解度A小于B
③物质A中含有少量B时,可以采用降温结晶的方法提纯A
④40℃时分别将物质A、B的饱和溶液降温至10℃,析出物质的质量A大于B
您最近一年使用:0次
【推荐1】请根据如图甲、乙、丙三种固体物质的溶解度曲线,回答下列问题。
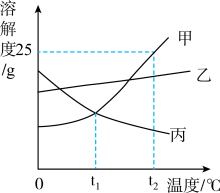
(1)在______ ℃时,甲、丙两种物质的溶解度相等;
(2)在t2℃时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的溶质质量分数为______ 。
(3)若乙物质中混有少量甲物质,最好采用______ (填“降温结晶”或“蒸发结晶”)的方法提纯

(1)在
(2)在t2℃时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的溶质质量分数为
(3)若乙物质中混有少量甲物质,最好采用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】化学就在我们身边,生活中蕴藏着丰富的化学知识。
(1) 日常生活中可用___________ 区分硬水和软水。
(2) 炒菜时锅中油起火燃烧,正确的方法是用锅盖盖灭,其原理是____________ 。
(3)酒精(C2H5OH)是清洁燃料之一,酒精完全燃烧的化学方程式是__________ 。
(4)有一种抗生素为粉末状固体,每瓶含0.5 g,注射时应配成质量分数为20%的溶液,则使用时每瓶至少需加入蒸馏水________ mL。
(1) 日常生活中可用
(2) 炒菜时锅中油起火燃烧,正确的方法是用锅盖盖灭,其原理是
(3)酒精(C2H5OH)是清洁燃料之一,酒精完全燃烧的化学方程式是
(4)有一种抗生素为粉末状固体,每瓶含0.5 g,注射时应配成质量分数为20%的溶液,则使用时每瓶至少需加入蒸馏水
您最近一年使用:0次





