某硫酸厂排放的污水中通常含有硫酸杂质。为测定污水中硫酸的溶质质量分数。做如下实验:取10g该污水,向污水中逐滴加入溶质质量分数为4%的氢氧化钠溶液,所滴加氢氧化钠溶液的质量与溶液pH变化关系如图所示。
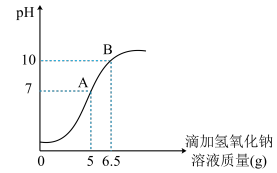
(1)逐滴加入氢氧化钠溶液需用到的仪器是______ ;
(2)B点处溶液中的溶质有______ (写化学式);
(3)某同学滴加氢氧化钠溶液时不慎滴到试管外,此同学测得的污水中硫酸的溶质质量分数会______ (填“增大、减小、不变”)。
(4)请根据实验计算,该污水中硫酸的溶质质量分数是多少?

(1)逐滴加入氢氧化钠溶液需用到的仪器是
(2)B点处溶液中的溶质有
(3)某同学滴加氢氧化钠溶液时不慎滴到试管外,此同学测得的污水中硫酸的溶质质量分数会
(4)请根据实验计算,该污水中硫酸的溶质质量分数是多少?
更新时间:2023-04-23 17:33:50
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把200g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应)。请计算:
(1)上表中n的数值为___________ 。
(2)样品中碳酸钙的质量分数是___________ 。(结果精确值至0.1%)
(3)求该实验所用稀盐酸中溶质质量分数(写出计算过程,结果精确值至0.1%)。
| 序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 第1次 | 50 | 11 |
| 第2次 | 50 | 6 |
| 第3次 | 50 | 2.8 |
| 第4次 | 50 | n |
(2)样品中碳酸钙的质量分数是
(3)求该实验所用稀盐酸中溶质质量分数(写出计算过程,结果精确值至0.1%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】为测定某镁矿石中镁元素的质量分数,兴趣小组的同学取了10g该镁矿石粉末,加入过量的稀盐酸,充分反应后过滤、除杂,得到只含有 和
和 两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
请计算:
(1)该镁矿石中镁元素的质量分数为________ 。(假设10g镁矿石中的镁元素全部转化到100g混合溶液中)
(2)加入的氢氧化钠溶液的溶质质量分数为_____________ 。
(3)将恰好完全反应时的溶液过滤,再将滤液蒸发掉89.18g水,所得溶液中溶质质量分数为多少?(假设整个过程无损耗)
 和
和 两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取60g氢氧化钠溶液,分6次加入盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:实验编号 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 |
加入氢氧化钠溶液质量/g | 10 | 10 | 10 | 10 | 10 | 10 |
烧杯中生成沉淀的总质量/g | 0 | 0.58 | 1.16 | 1.74 | 2.32 | 2.32 |
(1)该镁矿石中镁元素的质量分数为
(2)加入的氢氧化钠溶液的溶质质量分数为
(3)将恰好完全反应时的溶液过滤,再将滤液蒸发掉89.18g水,所得溶液中溶质质量分数为多少?(假设整个过程无损耗)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】硫酸钡是一种不溶于水,也不溶于酸的固体,医疗上常用硫酸钡作透视肠胃的内服造影剂,俗称“钡餐”。若“钡餐”中含有碳酸钡,就会致人中毒。为测定某硫酸钡样品中碳酸钡的含量,取10g样品,向其中逐渐加入一定质量分数的稀硝酸至恰好完全反应,发生反应的化学方程式为: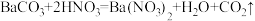 ,测得共用去稀硝酸63g,反应后称得烧杯中物质的总质量为72.78g。请计算:
,测得共用去稀硝酸63g,反应后称得烧杯中物质的总质量为72.78g。请计算:
(1)反应生成的二氧化碳为 g。
(2)原样品中碳酸钡的质量分数是多少?
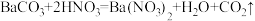 ,测得共用去稀硝酸63g,反应后称得烧杯中物质的总质量为72.78g。请计算:
,测得共用去稀硝酸63g,反应后称得烧杯中物质的总质量为72.78g。请计算:(1)反应生成的二氧化碳为 g。
(2)原样品中碳酸钡的质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某纯碱样品中含有少量氯化钠。现称量该样品22.8g放入烧杯中,再向其中加入一定溶质质量分数的稀盐酸至186g时恰好完全反应,此时烧杯内的物质质量为200g。试计算:
(1)反应后生成的气体质量为_____g;
(2)恰好完全反应时所得溶液中溶质的质量分数。_____(要求写出计算过程,结果精确到0.1%)
(1)反应后生成的气体质量为_____g;
(2)恰好完全反应时所得溶液中溶质的质量分数。_____(要求写出计算过程,结果精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】取含有杂质KCl的KOH样品2.5 g,溶于12.9 g水量。待全部溶解后加入10%的盐酸14.6 g恰好中和。求样品中KOH的质量分数和反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】中和反应是一类重要的化学反应。某同学利用如甲图所示装置研究盐酸与氢氧化钠溶液的反应过程。分别取稀盐酸和氢氧化钠溶液各100g进行实验,并用pH计和温度传感器测量反应过程中相关物理量的变化情况,得到图乙、丙。已知选用的盐酸的浓度为14.6%。
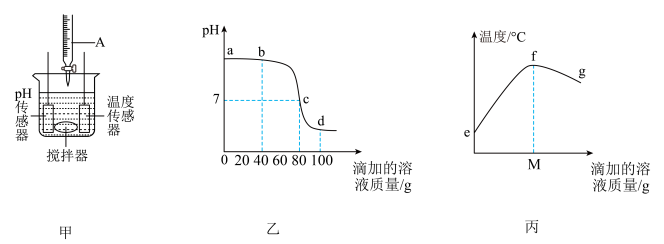
(1)依图可知中和反应是______反应(选填“吸热”或“放热”)。
(2)图丙中M的数值最接近______(填“40”“80”或“100”)。
(3)计算所用氢氧化钠溶液的溶质质量分数______。(计算结果精确到0.1%)
(4)请在图中画出在滴加溶液的过程中,所滴加溶液的质量与生成的氯化钠的质量对应的变化图,并标注必要的数值______。

(1)依图可知中和反应是______反应(选填“吸热”或“放热”)。
(2)图丙中M的数值最接近______(填“40”“80”或“100”)。
(3)计算所用氢氧化钠溶液的溶质质量分数______。(计算结果精确到0.1%)
(4)请在图中画出在滴加溶液的过程中,所滴加溶液的质量与生成的氯化钠的质量对应的变化图,并标注必要的数值______。

您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】根据初中化学酸、碱、盐的反应,回答下列问题:
(1)实验室常用浓度为1:5的稀盐酸(密度为1.03g·mL-1)进行化学实验,该盐酸由浓盐酸和水以体积比1:5比例混合而成。目前实验室中购置了市售溶质质量分数为38%,密度为1.18g·mL-1的浓盐酸,以此来配制此稀溶液,此时稀盐酸的溶质质量分数为 (计算结果保留到0.1%)。
(2)向试管中加入2mL溶质质量分数为5%的氢氧化钠溶液(密度为1.05g·m L-1.)滴入2滴酚酞试液,振荡,再逐滴滴入上述稀盐酸,直至溶液刚好变为 色,即可认为恰好完全反应,试列式计算理论上需要加入上述稀盐酸多少滴?(已知:每滴溶液的体积近似为0.05mL)
(3)某校学生在完成该实验时,记录滴入的稀盐酸为32滴。请思考实际滴数和理论滴数不一致的原因可能是 (填字母序号)。
a.使用的浓盐酸具有强烈挥发性,使配制得到的稀盐酸浓度偏低
b.使用的氢氧化钠溶液吸收二氧化碳而发生变质
c.滴入稀盐酸过程中,试管没有充分振荡
(1)实验室常用浓度为1:5的稀盐酸(密度为1.03g·mL-1)进行化学实验,该盐酸由浓盐酸和水以体积比1:5比例混合而成。目前实验室中购置了市售溶质质量分数为38%,密度为1.18g·mL-1的浓盐酸,以此来配制此稀溶液,此时稀盐酸的溶质质量分数为 (计算结果保留到0.1%)。
(2)向试管中加入2mL溶质质量分数为5%的氢氧化钠溶液(密度为1.05g·m L-1.)滴入2滴酚酞试液,振荡,再逐滴滴入上述稀盐酸,直至溶液刚好变为 色,即可认为恰好完全反应,试列式计算理论上需要加入上述稀盐酸多少滴?(已知:每滴溶液的体积近似为0.05mL)
(3)某校学生在完成该实验时,记录滴入的稀盐酸为32滴。请思考实际滴数和理论滴数不一致的原因可能是 (填字母序号)。
a.使用的浓盐酸具有强烈挥发性,使配制得到的稀盐酸浓度偏低
b.使用的氢氧化钠溶液吸收二氧化碳而发生变质
c.滴入稀盐酸过程中,试管没有充分振荡
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】实验室测定一瓶稀硫酸中溶质的质量分数.取10g该待测液,向其中逐滴加入5%的NaOH溶液,加入NaOH溶液的质量与溶液pH的变化关系如图所示。
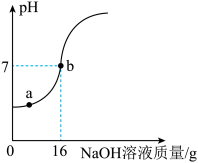
(1)16g5%的NaOH溶液中所含溶质的质量是________ g;
(2)a点对应溶液中的溶质是________ ;
(3)计算待测稀硫酸中溶质的质量分数_________ (写出计算过程及结果)。

(1)16g5%的NaOH溶液中所含溶质的质量是
(2)a点对应溶液中的溶质是
(3)计算待测稀硫酸中溶质的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。分析并计算:
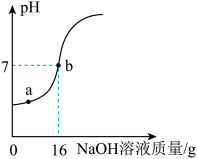
(1)写出反应的化学方程式_______ 。
(2)a点溶液中含有的离子是_______ 。
(3)当pH=7时,列出求解参加反应的硫酸质量(X)的比例式________ 。
(4)计算稀硫酸中溶质的质量分数________ 。
(5)若用质量分数98%的浓硫酸配制上述实验所需稀硫酸,需要浓硫酸质量为________ 。
(6)向恰好完全反应时的溶液中加入24克水,所得溶液的溶质质量分数_______ 。

(1)写出反应的化学方程式
(2)a点溶液中含有的离子是
(3)当pH=7时,列出求解参加反应的硫酸质量(X)的比例式
(4)计算稀硫酸中溶质的质量分数
(5)若用质量分数98%的浓硫酸配制上述实验所需稀硫酸,需要浓硫酸质量为
(6)向恰好完全反应时的溶液中加入24克水,所得溶液的溶质质量分数
您最近一年使用:0次
【推荐3】二氧化硫(SO2)是一种食品添加剂。葡萄酒酿造过程中添加SO2可防止其变质,但需严格控制用量,我国《葡萄酒国家标准》中规定SO2的含量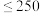 mg/L。
mg/L。
为检测某净含量750mL的国产葡萄酒SO2中的含量是否符合国家标准,进行如下实验:
步骤1:取100mL该葡萄酒于锥形瓶中,加入质量分数为10%的H2O2溶液,将SO2完全转化成硫酸。
步骤2:向锥形瓶中滴加指示剂(该指示剂在pH<7的溶液中显紫色,pH>7的溶液显绿色),用氢氧化钠溶液中和,测得锥形瓶中硫酸的质量为14.7mg。
(1)步骤2中,滴入指示剂后溶液呈________ 色。
(2)向10g 30%的H2O2溶液中加入________ g水,可稀释为10%的H2O2溶液。
(3)通过计算判断该葡萄酒中SO2的含量是否符合国家标准。
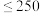 mg/L。
mg/L。为检测某净含量750mL的国产葡萄酒SO2中的含量是否符合国家标准,进行如下实验:
步骤1:取100mL该葡萄酒于锥形瓶中,加入质量分数为10%的H2O2溶液,将SO2完全转化成硫酸。
步骤2:向锥形瓶中滴加指示剂(该指示剂在pH<7的溶液中显紫色,pH>7的溶液显绿色),用氢氧化钠溶液中和,测得锥形瓶中硫酸的质量为14.7mg。
(1)步骤2中,滴入指示剂后溶液呈
(2)向10g 30%的H2O2溶液中加入
(3)通过计算判断该葡萄酒中SO2的含量是否符合国家标准。
您最近一年使用:0次