大量的研究工作者正在寻求各种方便有效的方法来降低大气中 CO2的浓度。
(1)矿物固碳的基本原理是用固碳试剂将二氧化碳转化为碳酸盐保存。氢氧化钙是一种传统的固碳试剂。国内外学者对其固碳过程与机理进行了大量研究。
①制备氢氧化钙可用生石灰(CaO)与水混合形成饱和溶液,该过程____________ (填“吸收”或“放出”热量,然后结晶。请写出用氢氧化钙固碳的反应原理____________ 。(用化学方程式表示)
②常压时,干燥的氢氧化钙需要在 300~600℃的温度下才能与 CO2发生反应,则制作氢氧化钙样品块时需要加入少量水的目的是____________ 。
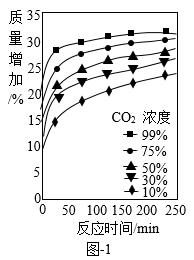
③根据图-1,你能得到关于氢氧化钙固碳速率的结论是_____________ 。
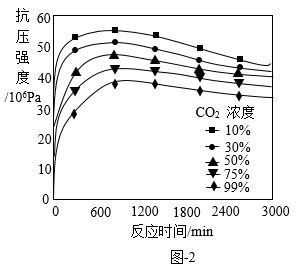
④根据图-2 可知,固碳后样品的抗压强度随碳化过程中 CO2浓度的增加而减小。试解释产生该现象的可能原因是____________ 。
⑤请设计简单方案检验碳化后的产物中含有碳酸盐____________ 。
(2)中国科学家己实现由 CO2到淀粉的全人工合成,主要过程的微观示意图如下:
(1)矿物固碳的基本原理是用固碳试剂将二氧化碳转化为碳酸盐保存。氢氧化钙是一种传统的固碳试剂。国内外学者对其固碳过程与机理进行了大量研究。
①制备氢氧化钙可用生石灰(CaO)与水混合形成饱和溶液,该过程
②常压时,干燥的氢氧化钙需要在 300~600℃的温度下才能与 CO2发生反应,则制作氢氧化钙样品块时需要加入少量水的目的是
③根据图-1,你能得到关于氢氧化钙固碳速率的结论是
④根据图-2 可知,固碳后样品的抗压强度随碳化过程中 CO2浓度的增加而减小。试解释产生该现象的可能原因是
⑤请设计简单方案检验碳化后的产物中含有碳酸盐
(2)中国科学家己实现由 CO2到淀粉的全人工合成,主要过程的微观示意图如下:
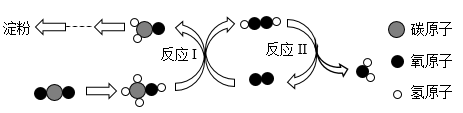
①反应Ⅰ是甲醇分子(CH4O)到甲醛分子 CH2O)的转化,过程中产生的 分子的化学式为
分子的化学式为
②为使得反应工持续进行,反应Ⅱ中需要不断补充  分子,理论每完成一个甲醇分子到甲醛分子的转化,需要补充
分子,理论每完成一个甲醇分子到甲醛分子的转化,需要补充 分子。
分子。
2023·江苏·二模 查看更多[6]
更新时间:2023-04-29 14:28:02
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】为解决能源与环境问题,有学者提出如下图所示的含碳物质转化的技术路线。

(1)“可燃冰”主要成分的名称为_______ ;
(2)反应①的化学方程式为_______ 。
(3)反应②属于_______ (填基本反应类型)。
(4)反应③的化学方程式为________ 。
(5)反应④中,参加反应的CO2和H2的分子个数比为________ 。

(1)“可燃冰”主要成分的名称为
(2)反应①的化学方程式为
(3)反应②属于
(4)反应③的化学方程式为
(5)反应④中,参加反应的CO2和H2的分子个数比为
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐2】化学方程式是重要的化学用语,质量守恒定律是化学反应中的重要定律。
(1)根据化学方程式能获得的信息是_________ (填字母序号)。
A.化学反应的条件 B.化学反应的快慢
C.反应物和生成物的质量比 D.化学反应的反应物和生成物
(2)在一密闭容器里放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
①表中m的数值为_________ 。
②反应中Y和Z变化的质量比_________ 。
③若X,Z的相对分子质量之比为7∶8,则它们的化学计量数之比为_________ 。
(3)无标签试剂瓶中有一种黑色不溶于水的固体,可能是硫化铜或硫化亚铜。查阅资料可知:
硫化铜(CuS)和硫化亚铜(Cu2S)在空气中灼烧分别发生下列化学反应:





某同学用天平准确称量一定质量的待测黑色固体于坩埚中,在空气中充分灼烧,冷却后再称量剩余固体质量。若灼烧前后固体质量不变,则该固体的化学式是___________ 。
(1)根据化学方程式能获得的信息是
A.化学反应的条件 B.化学反应的快慢
C.反应物和生成物的质量比 D.化学反应的反应物和生成物
(2)在一密闭容器里放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
| 物质 | X | Y | Z | W |
| 反应前的质量/g | 10 | 5 | 20 | 8 |
| 反应后的质量/g | 7.2 | 13.8 | 10.4 | m |
①表中m的数值为
②反应中Y和Z变化的质量比
③若X,Z的相对分子质量之比为7∶8,则它们的化学计量数之比为
(3)无标签试剂瓶中有一种黑色不溶于水的固体,可能是硫化铜或硫化亚铜。查阅资料可知:
硫化铜(CuS)和硫化亚铜(Cu2S)在空气中灼烧分别发生下列化学反应:





某同学用天平准确称量一定质量的待测黑色固体于坩埚中,在空气中充分灼烧,冷却后再称量剩余固体质量。若灼烧前后固体质量不变,则该固体的化学式是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】 化学兴趣小组对CO2和NaOH溶液能否反应进行分组实验探究。
(2)乙组同学向实验后左瓶内的溶液中滴加足量稀盐酸,也能达到实验目的,原因是什么?(用化学方程式解释)

(2)乙组同学向实验后左瓶内的溶液中滴加足量稀盐酸,也能达到实验目的,原因是什么?(用化学方程式解释)
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】A-F均为初中化学常见的物质,它们之间的关系如下图所示(部分物质已略去),其中D是石灰石的主要成分,C为最常见的液体,且C与E元素组成相同,请回答下列问题。
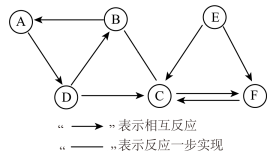
(1)写出E的化学式_______ 。
(2)写出A物质的一种用途_______ 。
(3)写出B和C反应的化学方程式:_______ 。

(1)写出E的化学式
(2)写出A物质的一种用途
(3)写出B和C反应的化学方程式:
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
真题
解题方法
【推荐1】如图中A、B、C、D为初中常见的四种化合物,其中“﹣”表示两端的物质在一定条件下能反应,“→”表示一种物质在一定条件下能反应生成另一种物质.已知A、B、C中都有两种相同的元素,其中一种为金属元素,另一种为非金属元素,D是植物进行光合作用必不可少的气体.

(1)推断A的化学式为
_________ ,D的化学式为
_________ ;
(2)反应“B﹣D”的化学方程式为
_________ .

(1)推断A的化学式为
(2)反应“B﹣D”的化学方程式为
您最近一年使用:0次
【推荐2】水和溶液在自然界、生产和生活中都有广泛用途。
(1)水是重要的氧化物,电解水实验说明水是由______ 组成的。
(2)水是重要的溶剂,配制2%的氯化钠溶液500g,不需要使用的仪器是______。
(3)除去NaOH溶液中混有的少量Na2CO3杂质,需加入适量的______ 溶液至不再产生沉淀为止,然后过滤,再将滤液______ ,便可得到NaOH固体。
(4)现有20℃时Ca(OH)2的饱和溶液甲,向其中加入一定量CaO,一段时间后得到同温度的溶液乙,则甲、乙溶液中溶质质量甲______ 乙(填“>”“<”或“=”)。
(1)水是重要的氧化物,电解水实验说明水是由
(2)水是重要的溶剂,配制2%的氯化钠溶液500g,不需要使用的仪器是______。
| A.酒精灯 | B.玻璃棒 | C.烧杯 | D.量筒 | E.托盘天平 |
(4)现有20℃时Ca(OH)2的饱和溶液甲,向其中加入一定量CaO,一段时间后得到同温度的溶液乙,则甲、乙溶液中溶质质量甲
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】某兴趣小组用碳酸钠溶液鉴别稀盐酸、氯化钠溶液和澄清石灰水。进行实验如下表:
写出a试管中发生反应的化学方程式___________ 。把c试管反应后的物质进行过滤,得到滤液。
[提出问题]滤液中溶质的成分是什么?
猜想一: Na2CO3和NaOH; 猜想二: NaOH; 猜想三:NaOH和Ca(OH)2。
[实验过程]为了证明哪种猜想正确,进行了如下实验:
写出上述有白色沉淀生成的化学方程式____________ 。
| 实验步骤 | 实验现象 | 实验结论 |
| 分别用a、b、c三支试管取样,各加入一定量碳酸钠溶液 | a中有气泡产生 | a中物质是稀盐酸 |
| b中无明显现象 | b中物质是氯化钠溶液 | |
| c中 | c中物质是澄清石灰水 |
[提出问题]滤液中溶质的成分是什么?
猜想一: Na2CO3和NaOH; 猜想二: NaOH; 猜想三:NaOH和Ca(OH)2。
[实验过程]为了证明哪种猜想正确,进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取一定量滤液于试管中,加入一种盐溶液(写溶质化学式) | 有白色沉淀 | 猜想一正确 |
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】有一包白色固体样品,可能含有NaOH、Na2CO3、K2SO4、BaCl2、CuSO4中的一种或几种,为确定其组成,进行如下实验:
(1)步骤Ⅰ:取少量样品于烧杯中,加足量水,充分搅拌,静置,有白色固体产生,上层清液呈无色。则该样品中一定不含_______ 。
(2)步骤Ⅱ:取步骤Ⅰ所得上层清液于试管中,滴入几滴酚酞溶液,溶液变红色;再滴入过量稀盐酸,无气泡产生,红色逐渐褪去,得到无色溶液。则溶液的红色褪去,发生反应的化学方程式是_____ 。
(3)步骤Ⅲ:取步骤Ⅰ所得白色固体于试管中,滴入过量稀盐酸,有大量气泡产生,白色固体全部溶解。综合步骤Ⅰ、步骤Ⅱ、步骤Ⅲ分析,该样品中一定含有_______ 。
(1)步骤Ⅰ:取少量样品于烧杯中,加足量水,充分搅拌,静置,有白色固体产生,上层清液呈无色。则该样品中一定不含
(2)步骤Ⅱ:取步骤Ⅰ所得上层清液于试管中,滴入几滴酚酞溶液,溶液变红色;再滴入过量稀盐酸,无气泡产生,红色逐渐褪去,得到无色溶液。则溶液的红色褪去,发生反应的化学方程式是
(3)步骤Ⅲ:取步骤Ⅰ所得白色固体于试管中,滴入过量稀盐酸,有大量气泡产生,白色固体全部溶解。综合步骤Ⅰ、步骤Ⅱ、步骤Ⅲ分析,该样品中一定含有
您最近一年使用:0次
【推荐3】酸、碱、盐是用途广泛的化合物。
(1)请从以下选项中选择适当物质的标号填空:
A.盐酸 B.氯化钠 C.氢氧化钠 D.硝酸银
①可用于金属表面除锈的是________ ;
②可与硫酸发生中和反应的是________ ;
③可用于腌渍蔬菜、鱼、肉、蛋等的是_________ 。
(2)实验室用Na2CO3固体配制100g5%的Na2CO3溶液,需要水的质量为______ g。
(3)室温下,向Na2CO3溶液中加入一定量的Ba(OH)2溶液,充分反应后过滤。反应前后溶液中存在的主要离子如下图:_____ 7(填“>”“=”或“<”)。
②取反应后的溶液,滴加过量稀盐酸,产生气泡,则图中R表示的离子是_______ (填离子符号)。
③下列能代替稀盐酸,检验反应后溶液中R离子的是_______ (填标号)。
A.稀硝酸 B.Ba(OH)2溶液 C.CaCO3粉末 D.MgCl2溶液
(1)请从以下选项中选择适当物质的标号填空:
A.盐酸 B.氯化钠 C.氢氧化钠 D.硝酸银
①可用于金属表面除锈的是
②可与硫酸发生中和反应的是
③可用于腌渍蔬菜、鱼、肉、蛋等的是
(2)实验室用Na2CO3固体配制100g5%的Na2CO3溶液,需要水的质量为
(3)室温下,向Na2CO3溶液中加入一定量的Ba(OH)2溶液,充分反应后过滤。反应前后溶液中存在的主要离子如下图:

②取反应后的溶液,滴加过量稀盐酸,产生气泡,则图中R表示的离子是
③下列能代替稀盐酸,检验反应后溶液中R离子的是
A.稀硝酸 B.Ba(OH)2溶液 C.CaCO3粉末 D.MgCl2溶液
您最近一年使用:0次


 CaCO3+CO2↑+H2O,物质之间转化关系如图所示戊、己组成元素相同。用化学方程式表示下列转化过程
CaCO3+CO2↑+H2O,物质之间转化关系如图所示戊、己组成元素相同。用化学方程式表示下列转化过程


