2023年江苏省苏州市中考二模化学试题
江苏
九年级
二模
2023-06-25
297次
整体难度:
容易
考查范围:
化学与社会发展、身边的化学物质、物质构成的奥秘、化学实验、物质的化学变化
一、选择题 添加题型下试题
| A.彩绘天王木盒 | B.秘色瓷莲花碗 |
| C.鎏金铁芯铜龙 | D.行书兰亭序卷 |
【知识点】 金属材料和非金属材料解读 塑料、合成橡胶、合成纤维解读
| A.金刚石 |
| B.铜 |
| C.氯化钠 |
| D.干冰 |
| A.氧气 | B.氢气 | C.氮气 | D.一氧化碳 |
【知识点】 证明空气及各成分的存在及性质解读 空气中各成分的用途解读
A.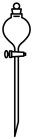 长颈漏斗 长颈漏斗 | B.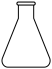 烧杯 烧杯 |
C. 镊子 镊子 | D.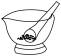 研钵 研钵 |
【知识点】 常见仪器及制材的辨认解读
| A.铁离子—Fe2+ | B.纯碱—NaHCO3 |
| C.2 个氮分子—2N2 | D.氯元素—CL |
| A.蔗糖水 | B.肥皂水 | C.蒸馏水 | D.食盐水 |
【知识点】 溶液的酸碱性的判断与pH的测定解读
9. 镓是一种奇妙的金属,放在手心会很快变为液态流动,其信息和原子结构示意图如图所示。下列说法不正确的是

| A.x=3 | B.镓属于金属元素 |
| C.镓熔点较低 | D.镓的相对原子质量为 69.72 g |
| A.许多植物能通过光合作用把太阳能贮存在纤维素中 |
| B.能用碘水或碘酒判断食物中是否含有纤维素 |
| C.棉、麻等植物纤维灼烧后有烧焦羽毛味 |
| D.纤维素能转化为葡萄糖,葡萄糖和油脂组成相同,都是有机高分子化合物 |
| A.石灰石受热易分解,能用作建筑材料 |
| B.醋酸有挥发性,可用于除水垢 |
| C.一氧化碳有可燃性,可以用于炼铁 |
| D.固体氢氧化钠有吸水性,可作干燥剂 |
A. 检查装置气密性 检查装置气密性 | B. 加入石灰石 加入石灰石 |
C.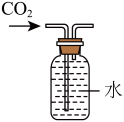 收集CO2 收集CO2 | D. 存放CO2 存放CO2 |
| A.稀释浓硫酸时,将水倒入盛有浓硫酸的烧杯中,并用玻璃杯不断搅拌 |
| B.用浓盐酸制备的 CO2气体中会混入较多氯化氢杂质 |
| C.大气中的 CO2 溶于水显酸性,是造成酸雨的主要原因 |
| D.多种物质能在氧气中燃烧,说明氧气具有可燃性 |
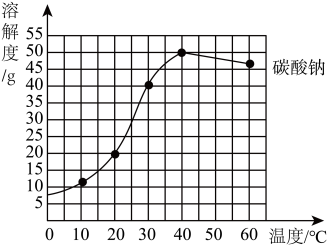
| A.碳酸钠的溶解度随温度升高而增大 |
| B.将20℃的碳酸钠饱和溶液升温至30℃,溶质质量分数不变 |
| C.30℃时,将25g碳酸钠加入50g水中,所得溶液质量为75g |
| D.40℃时,碳酸钠饱和溶液的溶质质量分数为50% |
| A.空气和氧气:伸入带火星的木条,观察现象 |
| B.二氧化锰和炭粉:取样加入双氧水,观察现象 |
| C.食盐水和蒸馏水:玻璃棒蘸取溶液灼烧,观察现象 |
| D.稀盐酸和稀硫酸:打开瓶口,观察是否有白雾 |
| A.碳原子和硫原子属于不同种元素——质子数不同 |
| B.瘪乒乓球放入热水中能鼓起——分子的体积增大 |
| C.酸有相似的化学性质——酸溶液中都含有大量H+ |
| D.端午时节,粽叶飘香——分子总是在不断运动着 |

| A.a点对应的物质可能是CH4 |
| B.《抱朴子》中描述一种物质:“可以刻玉,虽铁椎击之亦不能伤”,该物质化学式对应b点 |
| C.c点对应的物质能使澄清石灰水变浑浊 |
| D.e点对应的一种物质能使紫色石蕊试液变红 |
| A.该有机物中不含有氧元素 |
| B.该有机物中碳元素质量分数最大 |
| C.该有机物中C、H、O、N的原子个数比为1:4:1:2 |
| D.若有机物未完全干燥,则氧元素质量分数结果偏大 |
| 实验序号 | 盐酸pH | 压强P/kPa | 溶解氧(DO)/mg·L-1 | |||
| P反应前 | P反应后 | DO反应前 | DO反应后 | 开始降低所需时间/s | ||
| ① | 2.0 | 90.8 | 91.8 | 5.2 | 4.3 | 131 |
| ② | 3.0 | 90.8 | 91.5 | 5.0 | 3.7 | 68 |
| ③ | 4.0 | 90.8 | 90.3 | 4.9 | 3.4 | 24 |
| ④ | 5.0 | 90.8 | 90.5 | 4.9 | 3.7 | 98 |
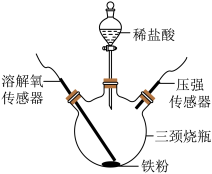
| A.实验中溶解氧浓度均下降是因为铁生锈需要消耗氧气 |
| B.实验①和实验②都生成了氢气 |
| C.实验③能观察到气泡,可能产生了氢气并消耗了更多体积的氧气 |
| D.由表中数据可知,pH 越小,铁生锈速率越快 |
二、填空与简答 添加题型下试题
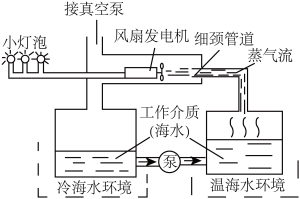
(1)真空泵能通过降低压强,
(2)使用海水为工作介质的一大优点是能在冷环境中得到淡水, 这一过程类似实验室的
(3)实际生产过程中,需在钢制设备外喷涂保护层,其目的是
(4)提高海洋温差能源利用率的方式除了寻找更佳的导热材料、工作介质外,还可以
【知识点】 资源综合利用和新能源开发的重要意义解读 蒸馏解读
三、实验题 添加题型下试题

(2)写出高锰酸钾分解制氧气的化学方程式:
(3)氯酸钾(KClO3)是实验室常用的另一种制氧药品,为了较准确测定氯酸钾完全分解产生氧气的体积,并对完全分解后的残留固体进行分离。进行以下实验:称取一定量氯酸钾与1.5g 二氧化锰混合,然后加热直至无气体放出。
①读取气体体积时,应将反应发生装置和收集装 置中的气体冷却至室温再进行。则收集气体应选如图中的
②实验操作与实验目的息息相关。要测量气体体 积应选择
a.待导管口有气泡均匀连续逸出时开始收集
b.加热后,立即开始收集气体
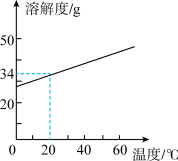
③KCl 的溶解度曲线如右图所示。将残留固体冷却至室温(20℃),称得其质量为 4.8 g。欲将 KCl 全部溶解, 至少应加入该温度下蒸馏水的体积约
四、填空与简答 添加题型下试题
(1)矿物固碳的基本原理是用固碳试剂将二氧化碳转化为碳酸盐保存。氢氧化钙是一种传统的固碳试剂。国内外学者对其固碳过程与机理进行了大量研究。
①制备氢氧化钙可用生石灰(CaO)与水混合形成饱和溶液,该过程
②常压时,干燥的氢氧化钙需要在 300~600℃的温度下才能与 CO2发生反应,则制作氢氧化钙样品块时需要加入少量水的目的是
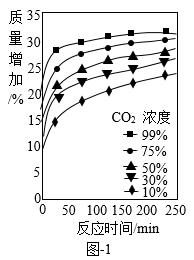
③根据图-1,你能得到关于氢氧化钙固碳速率的结论是
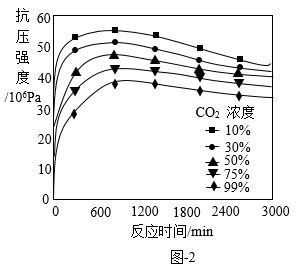
④根据图-2 可知,固碳后样品的抗压强度随碳化过程中 CO2浓度的增加而减小。试解释产生该现象的可能原因是
⑤请设计简单方案检验碳化后的产物中含有碳酸盐
(2)中国科学家己实现由 CO2到淀粉的全人工合成,主要过程的微观示意图如下:
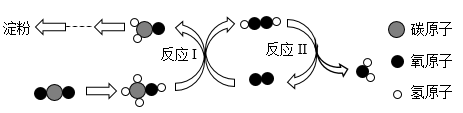
①反应Ⅰ是甲醇分子(CH4O)到甲醛分子 CH2O)的转化,过程中产生的 分子的化学式为
分子的化学式为
②为使得反应工持续进行,反应Ⅱ中需要不断补充  分子,理论每完成一个甲醇分子到甲醛分子的转化,需要补充
分子,理论每完成一个甲醇分子到甲醛分子的转化,需要补充 分子。
分子。

(1)18 世纪中叶,英国化学家普利斯特里用锌加入稀硫酸中制得“可燃空气”,将少量“可燃空气”与空气通入铁质容器混合点燃,能产生剧烈的爆鸣,并产生水雾。该“可燃空气” 应该是
(2)1781 年,英国化学家卡文迪许加热汞锻灰(HgO)后得到了一种液态金属单质和一种气体——“脱燃素空气”,蜡烛在这种气体中燃烧更明亮。请写出卡文迪许制得“脱燃素空气” 的反应方程式
(3)卡文迪许认为普利斯特斯的实验并不能证明水的组成,于是用“脱燃素空气”代替空气重做了实验,目的是
(4)1783 年,法国化学家拉瓦锡将水加热成蒸气通过高温的铁管,一段时间后,在出口处收集到一种可燃性气体。实验后称量发现水的质量减少,铁管的质量增加,经研究证明铁转化为四氧化三铁,装置如题 24 图-1 所示。其反应原理为
(5)180 年,英国化学家尼科尔森通过伏打电池在常温下对水进行通电分解,得到氢气和氧气,再次确认了水的组成。某同学在实验室模拟了尼科尔森用电分解水的实验(题 24 图—2), 得到不同电极的电解结果如下表所示。
表:不同电极在相同条件下的的电解结果(以气柱高度表示电解产生的气体体积)
| 电极 | 时间 | H2体积 | O2体积 | V(H2):V(O2) |
| 多孔碳棒 | 4’28” | 66 | 25 | 2.6:1 |
| 镀镍回形针 | 2’22” | 66 | 31 | 2.1:1 |
| 铜丝 | 2’15” | 66 | 33 | 2:1 |
结合图表信息回答,用多孔碳棒作电极时,氢气和氧气的体积比总是大于 2:1 的原因可能有哪些:
(6)在整个发现过程中,科学家利用了“分合”思想证明了水的组成。下面实验中属于“分” 思想的是
a.氢气燃烧实验 b.铁管实验 c.水通电实验

(1)“酸溶”时,金属镍是否发生反应
(2)“氧化”阶段发生的反应为 H2O2 + 2FeSO4+ H2SO4 = Fe2(SO4)3 + 2H2O,则反应中化合价改变的元素有
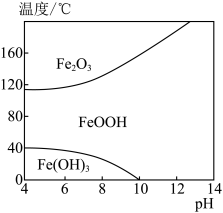
(3)“除铁”的目的是除去溶液中的 Fe3+。改变温度、pH,Fe 转化所得产物可能不同(如图)。80 ℃、pH=6 时,Fe3+转化为
A.将 NiSO4溶液与 Na2CO3溶液同时加入烧杯
B.将 Na2CO3溶液缓慢加入到盛有 NiSO4溶液的烧杯中
C.将 NiSO4溶液缓慢加入到盛有 Na2CO3溶液的烧杯中
五、科学探究题 添加题型下试题
【查阅资料】
①木炭能在较高温度环境中将氧化铜中的氧元素夺去,生成单质铜
②酒精灯防风罩能将酒精灯火焰温度提升至 600~800℃
③铜的熔点为 1083℃
【装置分析】
①该实验并未采用略向下倾斜试管的加热方法,原因可能是
A.使火焰更好包裹住药品部位,提高反应温度
B.防止生成的气体冲散药品,降低实验成功率
C.过程中会生成液态的铜,且防止石灰水倒吸
【实验过程】
实验:取 0.1 g 木炭粉与一定量的氧化铜粉末按下表所示比例充分混合,在粉末堆中插入一块灼烧过的铜片,进行实验。
| 序号 | 木炭粉与氧化铜粉末混合质量比 | 充分反应后试管底部固体的颜色 | |
| 1) | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
| 2) | 1:10 | 混有很少量黑色物质 | |
| 3) | 1:11 | 混有极少量黑色物质 | |
| 4) | 1:12 | 无黑色物质 | |
| 5) | 1:13 | 混有少量黑色物资 | |
③无需再进行木炭粉与氧化铜粉末质量比为 1: 14 的实验,原因是
④取出铜片观察,发现埋入粉末的部分变红,有金属光泽,上方铜片也变为亮红色,右侧澄清石灰水变浑浊,由此推测反应中产生的气体一定有
⑤某同学取 8.0 g CuO 固体粉末与一定量木炭以最佳质量比混合,若 CuO 完全转化为 Cu, 理论上预计能得到 Cu 的质量为
⑥试管底部的亮红色固体呈“海绵状”,如图-2 所示,实验得到“海绵铜”而非块状铜的原因是
(2)分别在 H2与 CO 气氛下,还原氧化铜样品。对反应后的样品进行 X 射线衍射,得到的XRD 图谱结果如图-3 所示。XRD 图谱中的峰值可以表征某物种的存在。结合图像说明,能否采用热还原的方法直接制得纯净的 Cu2O 产品,
【知识点】 不含杂质的化学方程式计算解读 木炭还原氧化铜的实验解读 控制变量
试卷分析
试卷题型(共 26题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 蛋白质 维生素的来源 油脂的来源 糖类的来源 | 单选题 |
| 2 | 0.65 | 金属材料和非金属材料 塑料、合成橡胶、合成纤维 | 单选题 |
| 3 | 0.94 | 分子、原子的区别与联系 分子是保持物质化学性质的最小微粒 | 单选题 |
| 4 | 0.85 | 证明空气及各成分的存在及性质 空气中各成分的用途 | 单选题 |
| 5 | 0.94 | 常见仪器及制材的辨认 | 单选题 |
| 6 | 0.65 | 离子符号的含义及书写 元素符号书写及含义 化学式书写及读法 常见盐的俗名、用途 | 单选题 |
| 7 | 0.85 | 人体内的常量元素 某些元素的缺乏症 | 单选题 |
| 8 | 0.94 | 溶液的酸碱性的判断与pH的测定 | 单选题 |
| 9 | 0.65 | 原子中各类微粒的数值关系 相对原子质量的概念及有关计算 元素周期表及元素分类 周期表信息示意图及结构示意图的综合考查 | 单选题 |
| 10 | 0.85 | 高分子化合物 葡萄糖、淀粉的检验 羊毛、合成纤维、棉的鉴别 能量转化与化学变化的关系 | 单选题 |
| 11 | 0.65 | 一氧化碳的还原性 酸的通性 几种常见碱的物理性质及用途 碳酸氢钠、碳酸钠、碳酸钙 | 单选题 |
| 12 | 0.94 | 化合反应 置换反应 | 单选题 |
| 13 | 0.65 | 制取二氧化碳的装置 二氧化碳物理性质及实验 气密性检测 固体药品的取用 | 单选题 |
| 14 | 0.65 | 氧气助燃性及实验 二氧化碳与水的反应及实验 浓硫酸的稀释 盐酸的物理性质 | 单选题 |
| 15 | 0.65 | 固体溶解度曲线的应用 溶解度的相关计算 溶质质量分数的涵义 | 单选题 |
| 16 | 0.65 | 氧气助燃性及实验 过氧化氢制取氧气实验 浓酸敞口放置的变化和现象 氯化钠 | 单选题 |
| 17 | 0.65 | 微粒的共性 微粒的观点解释现象 元素的概念 酸的通性的微观实质 | 单选题 |
| 18 | 0.85 | 金刚石的相关知识 碳的氧化物的全面比较 常见的酸碱指示剂及其变色情况 甲烷 | 单选题 |
| 19 | 0.65 | 有关质量守恒定律的计算 用质量守恒定律确定物质组成 化学式、分子式及涵义 根据化学式计算元素质量分数 | 单选题 |
| 20 | 0.65 | 金属与酸反应原理 探究铁生锈的条件 控制变量 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.65 | 资源综合利用和新能源开发的重要意义 蒸馏 | 填空题 |
| 23 | 0.65 | 化学方程式含义 二氧化碳与碱的反应及实验 生石灰的性质及用途 碳酸根离子的验证 | 填空题 |
| 24 | 0.65 | 化学方程式的书写 水的组成实验 电解水原理 | 科普阅读题 |
| 25 | 0.65 | 复分解反应的定义 金属与酸反应原理 常见的酸碱指示剂及其变色情况 盐类参与的反应 | 流程题 |
| 三、实验题 | |||
| 22 | 0.65 | 高锰酸钾制取氧气实验 氯酸钾制取氧气 氧气的制取中装置的选择 溶解度的相关计算 | |
| 四、科学探究题 | |||
| 26 | 0.4 | 不含杂质的化学方程式计算 木炭还原氧化铜的实验 控制变量 | |







