用如图装置进行实验。

(1)将试管中的稀硫酸倒入烧杯中。
①反应的化学方程式为______ 。
②电子天平示数减小,该变化______ (填“符合”或“不符合”)质量守恒定律。
(2)为验证反应前后质量守恒,可将稀硫酸替换为______(填序号)

(1)将试管中的稀硫酸倒入烧杯中。
①反应的化学方程式为
②电子天平示数减小,该变化
(2)为验证反应前后质量守恒,可将稀硫酸替换为______(填序号)
| A.稀盐酸 | B.硫酸铜溶液 | C.氯化镁溶液 | D.硝酸银溶液 |
更新时间:2023-05-18 21:14:20
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】中国古代典籍中记录了很多化学知识,展示了我国古代人民的智慧。《梦溪笔谈》中记载了用“苦泉水”制取铜的方法:“挹其水熬之,则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。主要流程如图所示:
(2)方案一:①在“烹”的过程中,胆矾(CuSO4·5H2O)首先转变成水和硫酸铜,继续加热到600℃,硫酸铜将会分解成氧气和两种氧化物,请写出该反应的化学方程式______ 。
②反应后的气体如果直接排放,会造成污染,该废气可用15%的氢氧化钠溶液吸收。现有30%的浓氢氧化钠溶液,想要得到15%的氢氧化钠溶液500g,需要加水的质量为______ 。
(3)方案二:写出“铁釜”中发生反应的化学方程式:______ 。
(4)铁釜外侧容易生锈,是因为铁与空气中的______ 发生反应。

| A.溶解 | B.过滤 | C.蒸发 |
②反应后的气体如果直接排放,会造成污染,该废气可用15%的氢氧化钠溶液吸收。现有30%的浓氢氧化钠溶液,想要得到15%的氢氧化钠溶液500g,需要加水的质量为
(3)方案二:写出“铁釜”中发生反应的化学方程式:
(4)铁釜外侧容易生锈,是因为铁与空气中的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】用如图实验研究质量守恒定律。称量总质量后,将注射器中热水推入瓶中,白磷燃烧,反应结束后,再次称量总质量。______ 。
(2)该实验验证了质量守恒定律,依据的是______ 。

(2)该实验验证了质量守恒定律,依据的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】杭州亚运会开幕式在世界上首次使用甲醇(CH3OH)作火炬燃料,实现了“零碳”排放。制备甲醇与甲醇燃烧的过程如图1所示:

(1)过程①利用太阳能发电进行电解水制氢气,反应的化学方程式为______ 。
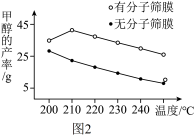
(2)写出过程②反应的化学方程式______ 。一定条件下,该反应在有、无分子筛膜时甲醇的产率随温度的变化如图2所示。由如图可知,为提高甲醇的产率,合成甲醇应选择的最佳条件为______ 。
(3)甲醇在常温下是一种无色液体,易溶于水,熔点-97.8℃,沸点64.7℃。过程③是利用水和甲醇的______ 不同将它们分离。
(4)从图示分析,若过程②和④中甲醇质量相等,则两过程中CO2质量相比较,前者与后者的关系是______(填字母)。


(1)过程①利用太阳能发电进行电解水制氢气,反应的化学方程式为
(2)写出过程②反应的化学方程式
(3)甲醇在常温下是一种无色液体,易溶于水,熔点-97.8℃,沸点64.7℃。过程③是利用水和甲醇的
(4)从图示分析,若过程②和④中甲醇质量相等,则两过程中CO2质量相比较,前者与后者的关系是______(填字母)。
| A.大于 | B.小于 | C.等于 | D.无法确定 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】我国研究人员研制出一种新型复合光催化剂,利用太阳光实现高效分解水,其主要过程如图所示。______ 。
(2)整个过程中数目保持不变的微粒是______ (填微粒符号)。
(3)写出整个过程的总反应化学方程式______ 。
(4)与电解水法相比,该方法最显著的优点是______ 。
(5)反应中的新型复合光催化剂经烘干后可以直接反复使用,其原因是______ 。

(2)整个过程中数目保持不变的微粒是
(3)写出整个过程的总反应化学方程式
(4)与电解水法相比,该方法最显著的优点是
(5)反应中的新型复合光催化剂经烘干后可以直接反复使用,其原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】通常,金属活动性越强,冶炼难度越大,人类使用该金属的时间越晚。
(1)如图为四种金属的最早冶炼历史年代。甲代表的金属是_____(填字母)。
(2)古代冶炼该金属的化学方程式是_____ 。
(3)将鱼用铝箔包好进行烤制,鱼很快被烤熟,在烤制过程中体现了铝箔具有良好的_____ 性;使用后的铝箔依然光亮如新,说明铝具有很好的抗腐蚀性,用化学方程式解释其原因_____ 。
(1)如图为四种金属的最早冶炼历史年代。甲代表的金属是_____(填字母)。

| A.铁 | B.铜 | C.钠 | D.锌 |
(2)古代冶炼该金属的化学方程式是
(3)将鱼用铝箔包好进行烤制,鱼很快被烤熟,在烤制过程中体现了铝箔具有良好的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】项目式学习小组的同学走进陕西省历史博物馆,探寻金属文化。
(1)认识金属文物。博物馆内的下列文物中,不是用金属材料制成的是________(填字母)。
(2)保护金属文物。某些贵重文物会保存在充满了某种保护气的密闭玻璃柜中。综合考虑成本、性质、安全性等因素,同学们推测该保护气是_______________ 。
(3)鉴别金属文物。一些仿制文物由黄铜(铜锌合金)制成,外观与黄金非常相似。为了鉴别成分,同学们分别取少量金属样品进行了下列实验。_______________ (填字母)。若该“文物”是由黄铜制成,则C试管中发生反应的化学方程式为_______________ (写一个)。
(1)认识金属文物。博物馆内的下列文物中,不是用金属材料制成的是________(填字母)。
| A.西周——青铜牛尊 | B.西汉——金怪兽 |
| C.东魏——鎏金佛菩萨三尊铜造像 | D.唐代——骑驼乐舞三彩陶俑 |
(2)保护金属文物。某些贵重文物会保存在充满了某种保护气的密闭玻璃柜中。综合考虑成本、性质、安全性等因素,同学们推测该保护气是
(3)鉴别金属文物。一些仿制文物由黄铜(铜锌合金)制成,外观与黄金非常相似。为了鉴别成分,同学们分别取少量金属样品进行了下列实验。
A. 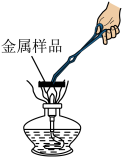 B.
B. 
C. 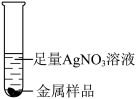 D.
D. 
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】人类社会发展离不开金属材料。如图是某硬铝的主要成分。

(1)将适量硬铝(已砂纸打磨处理)放入足量稀硫酸中,反应的化学方程式有_____ 。
(2)将足量硬铝粉末放入硝酸银溶液中,充分反应后,溶液出现蓝色,写出此时溶液中溶质成分并说明理由_____ 。

(1)将适量硬铝(已砂纸打磨处理)放入足量稀硫酸中,反应的化学方程式有
(2)将足量硬铝粉末放入硝酸银溶液中,充分反应后,溶液出现蓝色,写出此时溶液中溶质成分并说明理由
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】许多工厂未做处理直接将含铜废液、废渣等排放,既污染环境又浪费资源。一种从含铜废液[主要成分为CuCl2、FeCl2、CuSO4、Al2(SO4)3]中提取硫酸铜的工艺流程如图所示:

(1)反应器中充分反应后,排出的尾液的主要成分是_____ (写化学式)。
(2)净化器的主要目的是除去其中的杂质金属,加入的除杂试剂可能是_____ 。
(3)酸浸槽中发生反应的化学方程式为______ 。
(4)在结晶槽中冷却结晶得到硫酸铜,可知硫酸铜的溶解度随温度升高而_____ (填“增大”或“减小”)。
(5)酸浸槽中,不同浸出温度下铜的转化率变化如图所示,结合曲线分析在实际生产中如何设置反应条件,能使铜的转化率更高_____ 。


(1)反应器中充分反应后,排出的尾液的主要成分是
(2)净化器的主要目的是除去其中的杂质金属,加入的除杂试剂可能是
(3)酸浸槽中发生反应的化学方程式为
(4)在结晶槽中冷却结晶得到硫酸铜,可知硫酸铜的溶解度随温度升高而
(5)酸浸槽中,不同浸出温度下铜的转化率变化如图所示,结合曲线分析在实际生产中如何设置反应条件,能使铜的转化率更高

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】白铜是铜、镍(Ni)合金,某学习小组同学欲利用废弃的白铜回收铜、镍两种金属。
先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都有气泡产生,且锌粉与稀硫酸反应更剧烈,镍粉与稀硫酸反应后的溶液为绿色,说明锌、镍的金属活动性位于氢前。查阅资料可知,镍与稀硫酸反应的化学方程式为: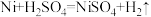 。
。
(1)接下来,同学们设计了如下实验流程回收铜和镍。________________ ,②中反应的化学方程式为________________ (写出一个)。
(2)要验证Ni、Zn、Cu的金属活动性顺序,用下列各组药品进行实验,能达到目的的是_______________(填字母)。
先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都有气泡产生,且锌粉与稀硫酸反应更剧烈,镍粉与稀硫酸反应后的溶液为绿色,说明锌、镍的金属活动性位于氢前。查阅资料可知,镍与稀硫酸反应的化学方程式为:
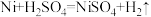 。
。(1)接下来,同学们设计了如下实验流程回收铜和镍。

(2)要验证Ni、Zn、Cu的金属活动性顺序,用下列各组药品进行实验,能达到目的的是_______________(填字母)。
| A.Ni、Cu、ZnSO4溶液 |
| B.Zn、Cu、NiSO4溶液 |
| C.Ni、ZnSO4溶液、CuSO4溶液 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】含有镁的合金广泛应用于航空航天领域,回答下列问题。
(1)取少量光亮的镁条于试管中,向其中加入稀盐酸,观察到___________ 的现象可推断二者发生了化学反应。
(2)若验证镁与稀盐酸反应后的溶液中有盐酸剩余,下列实验设计可行的是___________。
(3)向镁条中加入适量稀盐酸,完全反应后,再继续滴加过量氢氧化钠溶液,生成白色沉淀,写出加入氢氧化钠溶液时,生成白色沉淀的化学方程式___________ 。
(1)取少量光亮的镁条于试管中,向其中加入稀盐酸,观察到
(2)若验证镁与稀盐酸反应后的溶液中有盐酸剩余,下列实验设计可行的是___________。
| A.取生锈的铁钉于试管中,加入反应后的溶液 |
| B.取少量反应后的溶液于试管中,滴加AgNO3溶液 |
| C.取少量反应后的溶液于试管中,滴加稀氢氧化钠溶液 |
您最近一年使用:0次

 和
和 分别表示氯原子和氢原子。请回答:
分别表示氯原子和氢原子。请回答:


