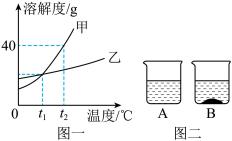
溶液与人们的生产、生活密切相关。请结合图一、图二所给信息,回答下列问题:_______ 乙(填“>”或“=”或“<”)。
(2)t2℃时,将等质量的甲、乙两物质分别放入两只烧杯中,各加入100g水,充分搅拌,溶解情况如图二所示,则B烧杯内的溶质是_______ 。(填“甲”或“乙”)
(3)下列有关甲、乙两物质的说法不正确的是_______。
(2)t2℃时,将等质量的甲、乙两物质分别放入两只烧杯中,各加入100g水,充分搅拌,溶解情况如图二所示,则B烧杯内的溶质是
(3)下列有关甲、乙两物质的说法不正确的是_______。
| A.甲、乙两物质相比,甲的溶解度受温度影响较大 |
| B.当甲中混有少量乙时,可采用降温结晶的方法提纯甲 |
| C.将t2℃时甲、乙两物质的饱和溶液降温至t1℃,析出晶体质量甲大于乙 |
| D.t2℃时,在50g水中加入30g甲物质充分溶解,得到70g甲溶液 |
2023·山东聊城·中考真题 查看更多[10]
2023年山东省聊城市中考化学真题(已下线)专题06 溶液-学易金卷:三年(2021-2023)中考化学真题分项汇编(全国通用)(已下线)专题12 溶液(第02期)-学易金卷:2023年中考化学真题分项汇编(全国通用)(已下线)专题07溶解度和溶质质量分数(考点)-广东备战2024年中考化学考点微专题山东省临沂市沂南县2023-2024年学年九年级上学期期末化学试题(已下线)2024年中考风向标-山东-溶解度曲线山东省烟台爱华双语学校2023-2024学年九年级(五四制)上学期期中质量检测化学试题(已下线)题型突破03 坐标曲线题-备战2024年中考化学复习题型突破学·练·考(全国通用)(已下线)专题03 坐标曲线题-2024年中考化学答题技巧与模板构建山东省聊城市东昌府区2023-2024学年九年级下学期期中模拟考试化学试题(一)
更新时间:2023-06-26 10:23:40
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】下面是某工厂苛化法生产烧碱的示意图。请回答下列问题:

(1)X的化学式________ 。
(2)反应池中,发生反应的化学方程式为:_______ 。
(3)操作②的名称是_________ ;结晶得到的固体烧碱中可能含有少量的__________ (写化学式);烧碱有强烈的腐蚀性,如果不慎将碱液沾到皮肤上,可先用较多的水冲洗,再涂上稀_________ 溶液。

(1)X的化学式
(2)反应池中,发生反应的化学方程式为:
(3)操作②的名称是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】有一种工业废水,其中含有大量的硫酸亚铁,少量硫酸铜以及污泥。某同学设计了一个既经济又合理的方法回收金属铜,并得到工业原料硫酸亚铁,其方案流程图如图所示(提示:硫酸亚铁的溶解度受温度变化影响不大):

回答下列问题:
(1)操作①的名称是______ 。
(2)加入过量的X是______ ,判断X过量的方法是______ 。
(3)步骤③过程中发生了置换反应,该反应的化学方程式是______ 。
(4)操作④采用的一种结晶方法是______ (填“降温结晶”或“蒸发结晶”)。

回答下列问题:
(1)操作①的名称是
(2)加入过量的X是
(3)步骤③过程中发生了置换反应,该反应的化学方程式是
(4)操作④采用的一种结晶方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】2020年,“中国水周”活动的主题为“坚持节水优先,建设幸福河湖”。
(1)生活中可用______ 的方法降低水的硬度;用洗涤剂洗餐具时,餐具上的油污以很小的液滴的形式分散到水中而洗去,该过程中发生了______ (填“溶解”、“乳化”或“反应”)。
(2)如图1是a、b、c三种物质的溶解度曲线,请回答。

①t2℃时,将30克a物质放入到50克水中,充分溶解后所得溶液中溶质与溶剂的质量比为______ 。
②a物质中混有少量b物质,若提纯a物质,可采取的结晶方法是______ 。
③t1℃时,取等质量的a、c饱和溶液分别置于甲、乙两支试管中,如图2所示。在大烧杯中加入一定质量的硝酸铵固体溶解后。
④a溶液的溶质质量分数______ (填“>”、“<”或“=”)c溶液的溶质质量分数。欲使图1中a物质溶解度曲线上的A点所示溶液变为B点所示溶液,可采取的措施是______ 。
(1)生活中可用
(2)如图1是a、b、c三种物质的溶解度曲线,请回答。

①t2℃时,将30克a物质放入到50克水中,充分溶解后所得溶液中溶质与溶剂的质量比为
②a物质中混有少量b物质,若提纯a物质,可采取的结晶方法是
③t1℃时,取等质量的a、c饱和溶液分别置于甲、乙两支试管中,如图2所示。在大烧杯中加入一定质量的硝酸铵固体溶解后。
④a溶液的溶质质量分数
您最近一年使用:0次
【推荐2】下列数据是硝酸钾固体在不同温度时的溶解度。
(1)硝酸钾固体的溶解度随温度的变化规律是___________ 。
(2)20℃时,在装有5gKNO3晶体的试管中,加入10g水并充分振荡,此时所得溶液为___________ (填“饱和”或“不饱和”)溶液。再将该试管放入盛有热水的烧杯中,使试管内溶液温度升至60℃(不考虑水分蒸发),则溶质与溶剂的质量比为__________ (填最简整数比)。
(3)如图所示,小烧杯中是底部有未溶解的硝酸钾溶液,若使其固体继硝酸钾续溶解,在大烧杯的水中可以加入的物质是 (填字母)。

温度/℃ | 0 | 20 | 40 | 60 | 80 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(1)硝酸钾固体的溶解度随温度的变化规律是
(2)20℃时,在装有5gKNO3晶体的试管中,加入10g水并充分振荡,此时所得溶液为
(3)如图所示,小烧杯中是底部有未溶解的硝酸钾溶液,若使其固体继硝酸钾续溶解,在大烧杯的水中可以加入的物质是 (填字母)。

| A.NH4NO3固体 | B.NaCl固体 | C.NaOH固体 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】甲、乙、丙三种物质的溶解度曲线如图所示,请回答。

(1)P点的含义是_______ 。
(2)气体的溶解度随温度变化的趋势与_______ (填“甲”、乙”或“丙”)相似。
(3)将质量分数20%的甲溶液40g,稀释为质量分数为10%的溶液,需要用到的仪器有烧杯、玻璃棒、 (填字母序号,下同)
(4)t3℃时,等质量的甲、乙、丙三种物质的饱和溶液分别降温至t1℃,对所得溶液分析正确的是 (填字母序号)。

(1)P点的含义是
(2)气体的溶解度随温度变化的趋势与
(3)将质量分数20%的甲溶液40g,稀释为质量分数为10%的溶液,需要用到的仪器有烧杯、玻璃棒、 (填字母序号,下同)
| A.50mL量筒 | B.托盘天平 | C.胶头滴管 | D.酒精灯 |
(4)t3℃时,等质量的甲、乙、丙三种物质的饱和溶液分别降温至t1℃,对所得溶液分析正确的是 (填字母序号)。
| A.溶解度:乙>甲=丙 | B.溶剂质量:丙>乙>甲 |
| C.溶液质量:乙>甲>丙 | D.溶质质量分数:乙>甲=丙 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】某化学小组的同学为研究物质的溶解现象进行了如下实验,请按题中要求回答问题:
(1)A、B中为饱和溶液的是______ (填序号)

(2)以下是氯化钠和高锰酸钾的溶解度表
①我们经常说“高锰酸钾易溶于水”,这句话是否正确?请说明理由______ 。
②将50℃的高锰酸钾饱和溶液和氯化钠的饱和溶液冷却到20℃时,氯化钠溶液的溶质质量分数______ (填“>”“<”或“=”)高锰酸钾溶液的溶质质量分数。
(3)如图是某气体在水中的溶解度曲线,根据图1所示可以得出影响气体溶解度的因素有______ ,若图中t2对应的温度为40℃,则t1对应的温度______ 40℃(填“>““<“或“=”)
(1)A、B中为饱和溶液的是

(2)以下是氯化钠和高锰酸钾的溶解度表
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解 度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| 高锰酸钾 | 2.8 | 4.3 | 6.4 | 9.0 | 12.6 | 18.0 | 22.1 | |
①我们经常说“高锰酸钾易溶于水”,这句话是否正确?请说明理由
②将50℃的高锰酸钾饱和溶液和氯化钠的饱和溶液冷却到20℃时,氯化钠溶液的溶质质量分数
(3)如图是某气体在水中的溶解度曲线,根据图1所示可以得出影响气体溶解度的因素有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】KNO3和KCl在不同温度时的溶解度如下表所示:
回答下列问题:
(1)30℃时,KC1的溶解度为_______ g。
(2)依据表中数据,绘制KNO3和KC1的溶解度曲线,如图中能表示KNO3溶解度曲线的是_______ (选填“a”或“b”)。

(3)40℃时,现有质量均为100g的硝酸钾和氯化钾两种饱和溶液,若将它们同时降温至10℃。下列说法不正确的是_______。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
(1)30℃时,KC1的溶解度为
(2)依据表中数据,绘制KNO3和KC1的溶解度曲线,如图中能表示KNO3溶解度曲线的是

(3)40℃时,现有质量均为100g的硝酸钾和氯化钾两种饱和溶液,若将它们同时降温至10℃。下列说法不正确的是_______。
| A.40℃时,硝酸钾饱和溶液水的质量大于氯化钾饱溶液中水的质量 |
| B.降温至10℃时,析出的KNO3晶体质量比析的KC1晶体质量大 |
| C.降温至10℃时,硝酸钾饱和溶液的质量分数大于氯化钾饱和溶液的质量分数 |
| D.当温度降至20℃和30℃之间的某一温度,两种溶液的质量分数可能相等 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:

(1)t2℃时,乙物质的溶解度是________ ;
(2)t3 ℃时,甲、乙、丙三种物质的溶解度大小关系是_________ ;
(3)t2 ℃时,乙物质的饱和溶液中溶质、溶剂的质量之比为______ (填最简整数比)。
(4)欲配制相同质量分数的乙,丙饱和溶液,应保持温度在___ ℃;
(5)欲将t3℃甲的不饱和溶液变成该温度下的饱和溶液,可采用的方法_____________ ;
(6)将t3 ℃时甲、乙、丙三种物质的饱和溶液各100 g,分别降温至t1 ℃,所得溶液质量的大小关系是____________ 。

(1)t2℃时,乙物质的溶解度是
(2)t3 ℃时,甲、乙、丙三种物质的溶解度大小关系是
(3)t2 ℃时,乙物质的饱和溶液中溶质、溶剂的质量之比为
(4)欲配制相同质量分数的乙,丙饱和溶液,应保持温度在
(5)欲将t3℃甲的不饱和溶液变成该温度下的饱和溶液,可采用的方法
(6)将t3 ℃时甲、乙、丙三种物质的饱和溶液各100 g,分别降温至t1 ℃,所得溶液质量的大小关系是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】水是一切生物生存所必需的,我们应该了解有关水的一些知识。
(1)节约用水、防止水污染应成为我们的自觉行为。下列说法中正确的是_____________ (填字母)。
A生活污水集中处理排放
B园林浇灌可采用喷灌、滴灌
C实验室废液未经处理直接排放
D提倡使用农家肥,禁止使用化肥和农药
(2)如图是水的电解实验:玻璃管b中收集的气体是____________ (填化学式),该反应的化学方程式为_____________ 。

(3)区分软水和硬水的物质是____________________ ,在生活中采用_______________ 的方法降低水的硬度。
(4)为预防新型冠状病毒,公共场所可用0.5%的过氧乙酸[化学式为C2H4O3]溶液来消毒,欲将50g 20%的过氧乙酸溶液,稀释为0.5%的过氧乙酸,需加入水的体积为___________ (水的密度为1.0g/mL)。
(1)节约用水、防止水污染应成为我们的自觉行为。下列说法中正确的是
A生活污水集中处理排放
B园林浇灌可采用喷灌、滴灌
C实验室废液未经处理直接排放
D提倡使用农家肥,禁止使用化肥和农药
(2)如图是水的电解实验:玻璃管b中收集的气体是

(3)区分软水和硬水的物质是
(4)为预防新型冠状病毒,公共场所可用0.5%的过氧乙酸[化学式为C2H4O3]溶液来消毒,欲将50g 20%的过氧乙酸溶液,稀释为0.5%的过氧乙酸,需加入水的体积为
您最近一年使用:0次
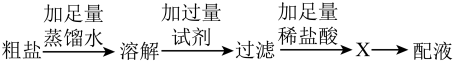
【推荐2】某同学利用含MgCl2、Na2SO4、CaCl2杂质的粗盐,配制一定溶质质量分数的氯化钠溶液,他设计了如下实验流程,请结合物质溶解性表,回答下列问题。
(1)步骤二中使用的三种试剂为:①Na2CO3溶液②BaCl2溶液③NaOH溶液,依次加入试剂的顺序为______ (填序号)。
(2)若经过滤,滤液仍浑浊的原因可能是______ (填序号)。
①滤纸破损 ②液面高于滤纸边缘 ③仪器不干净
(3)步骤三操作X的名称是______ 。用经X操作后得到的6g NaCl固体,配制溶质质量分数为6%的氯化钠溶液,所需水的质量为______ g。

(1)步骤二中使用的三种试剂为:①Na2CO3溶液②BaCl2溶液③NaOH溶液,依次加入试剂的顺序为
(2)若经过滤,滤液仍浑浊的原因可能是
①滤纸破损 ②液面高于滤纸边缘 ③仪器不干净
(3)步骤三操作X的名称是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】为了研究H2O2分解速率与二氧化锰的质量之间的关系。在60℃时,取溶质质量分数为3.4%的H2O2水溶液20mL(密度为1.01g·mL-1),分别加入不同质量的二氧化锰粉末,搅拌,实验测得H2O2浓度随时间的变化如图所示。

(1)写出上述反应的化学方程式为_________ ,在10min时,甲、乙、丙、丁四次实验中产生O2质量最多的是________ 实验(选填“甲”、“乙”、“丙”、丁”);
(2)通过上述对比实验,得到的结论是__________ ;
(3)20mL(密度为1.01g·mL-1)溶质质量分数为3.4%的H2O2的水溶液中所含溶质的质量为_______ g(小数点后面保留两位)。

(1)写出上述反应的化学方程式为
(2)通过上述对比实验,得到的结论是
(3)20mL(密度为1.01g·mL-1)溶质质量分数为3.4%的H2O2的水溶液中所含溶质的质量为
您最近一年使用:0次




