某“暖宝宝”取暖贴的透气无纺布袋内装有铁粉、活性炭、氯化钠、水等物质,兴趣小组同学对此展开探究。
【活动一】用铁钉探究铁的锈蚀
某同学用相同的铁钉探究铁生锈与哪些因素有关,设计了下图所示的实验。______ (填字母)
(2)该实验中将蒸馏水煮沸的目的是______ 。
(3)经过一周的观察,试管B和试管C中的铁钉无明显变化,试管A中的铁钉明显锈蚀,说明铁锈是铁与______ 发生化学反应生成的。
【活动二】用“暖宝宝”中的物质探究铁的锈蚀
用无纺布袋装入干燥的铁粉、活性炭和氯化钠,分别放在锥形瓶底部,进行下图所示的实验。______ ,打开无纺布袋,黑色粉末有部分变成______ 色,图2和图3所示实验均无明显现象。
(5)与【活动一】所示实验相比较,图1所示实验可在短时间内完成,除了铁粉的因素外,你对活性炭与氯化钠作用的合理猜测是______ (写出1点即可)。
【活动三】用“暖宝宝”测定空气里氧气的含量
(6)利用【活动二】中图1所示实验,测定空气里氧气的含量。
①实验时,需要获得的数据有锥形瓶内空气的体积、______ ;实验时需要注意的事项是______ (写出1点即可)。
②与用红磷测定空气里氧气的含量的实验相比,实验利用“暖宝宝”测定空气里氧气的含量的优点是______ (写出1条即可)。
【活动一】用铁钉探究铁的锈蚀
某同学用相同的铁钉探究铁生锈与哪些因素有关,设计了下图所示的实验。
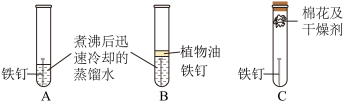
(2)该实验中将蒸馏水煮沸的目的是
(3)经过一周的观察,试管B和试管C中的铁钉无明显变化,试管A中的铁钉明显锈蚀,说明铁锈是铁与
【活动二】用“暖宝宝”中的物质探究铁的锈蚀
用无纺布袋装入干燥的铁粉、活性炭和氯化钠,分别放在锥形瓶底部,进行下图所示的实验。
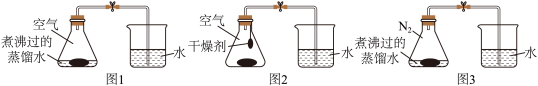
(5)与【活动一】所示实验相比较,图1所示实验可在短时间内完成,除了铁粉的因素外,你对活性炭与氯化钠作用的合理猜测是
【活动三】用“暖宝宝”测定空气里氧气的含量
(6)利用【活动二】中图1所示实验,测定空气里氧气的含量。
①实验时,需要获得的数据有锥形瓶内空气的体积、
②与用红磷测定空气里氧气的含量的实验相比,实验利用“暖宝宝”测定空气里氧气的含量的优点是
2023·安徽阜阳·二模 查看更多[5]
2023年安徽省阜阳市太和县中考二模化学试题内蒙古巴彦淖尔市杭锦后旗2023-2024学年九年级上学期期末化学试题安徽省淮北市五校联考2023-2024学年九年级上学期质量检测化学试题(已下线)黄金卷01(安徽专用)-【赢在中考·黄金8卷】备战2024年中考化学模拟卷(安徽专用)(已下线)专项11 科学探究题20题-2024年中考化学常考点必杀300题(全国通用)
更新时间:2023-07-15 21:53:41
|
相似题推荐
科学探究题
|
适中
(0.65)
名校
【推荐1】用来测定空气成分的方法很多,图1所示的是小明用红磷在空气中燃烧的测定方法。实验过程是:

第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。观察现象______ 。。
第三步:待红磷熄灭并冷却后,打开弹簧夹,观察现象___________ 。
请回答下列问题:
(1)填写第二步、第三步的观察现象;并写出该实验发生化学反应的表达式为____________________ 。
(2)上面的实验也证明了氮气有哪些性质?
①_____________________ ; ②_______________________ 。
(3)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能是(写一点即可)__________ 。
(4)某同学对实验进行反思后,提出了改进方法(如图2所示 ),你认为改进后的优点是:_________________ 。
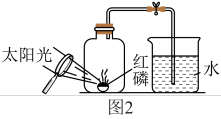

第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。观察现象
第三步:待红磷熄灭并冷却后,打开弹簧夹,观察现象
请回答下列问题:
(1)填写第二步、第三步的观察现象;并写出该实验发生化学反应的表达式为
(2)上面的实验也证明了氮气有哪些性质?
①
(3)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能是(写一点即可)
(4)某同学对实验进行反思后,提出了改进方法(如图2所示 ),你认为改进后的优点是:

您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
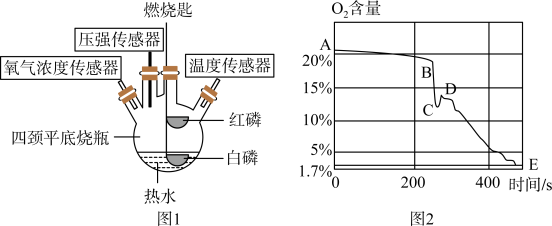
【推荐2】某化学兴趣小组对课本“测定空气中氧气含量”的实验完毕后,集气瓶中是否还含有氧气产生质疑,于是同学们设计了如图1装置来探究磷在空气中燃烧,氧气浓度的变化情况。
【提出问题】足量红磷在密闭的四颈平底瓶内燃烧,熄灭后容器中是否有氧气剩余?
【作出猜想】猜想①:有氧气剩余; 猜想②:无氧气剩余。
【实验验证】该小组同学按图1组装好实验装置,利用高能激光笔照射燃烧匙上的红磷,一段时间后红磷燃烧,待熄灭后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被很快点燃。
(1)激光笔的作用是________ 。
(2)红磷燃烧的符号表达式为_______ 。
【实验结论】
(3)根据上述实验现象,得出的结论是:猜想________ 正确。
(4)课本上用红磷燃烧的方法______ (填“能”或“不能”)精确地测定空气中氧气的含量,理由是________ 。
【拓展延伸】图2是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用传感器测量容器内氧气浓度变化的曲线图。
(5)图2中,在______ (填“A、B、C、D、E”)点时燃烧的红磷熄灭了,白磷开始燃烧至燃烧结束对应的曲线为______ 段(用图2中字母表示)。

【提出问题】足量红磷在密闭的四颈平底瓶内燃烧,熄灭后容器中是否有氧气剩余?
【作出猜想】猜想①:有氧气剩余; 猜想②:无氧气剩余。
【实验验证】该小组同学按图1组装好实验装置,利用高能激光笔照射燃烧匙上的红磷,一段时间后红磷燃烧,待熄灭后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被很快点燃。
(1)激光笔的作用是
(2)红磷燃烧的符号表达式为
【实验结论】
(3)根据上述实验现象,得出的结论是:猜想
(4)课本上用红磷燃烧的方法
【拓展延伸】图2是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用传感器测量容器内氧气浓度变化的曲线图。
(5)图2中,在
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】兴趣小组想深入探究人体呼出气体的成分,进行如下活动:
(1)(活动一)探究人体呼出气体中是否含有CO2
向装有呼出气体的集气瓶中滴加少量澄清石灰水,振荡后观察到_______ 。
(2)(活动二)探究人体呼出气体中CO2的体积分数(已知:CO2能与NaOH反应)
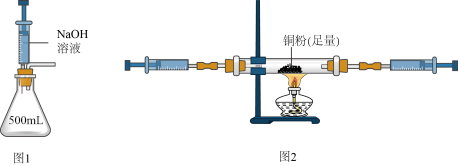
兴趣小组同学用图1所示装置进行实验。(锥形瓶内充满人体呼出的气体)实验前注射器内液体体积为50mL,向锥形瓶内注入少量液体后,注射器内的液体开始被自动吸入锥形瓶,完全反应后,注射器内NaOH溶液的体积为30mL。
结论:人体呼出气体中CO2的体积分数为_______ 。
(3)(活动三)探究人体呼出气体中O2的体积分数
兴趣小组同学用图2所示装置进行实验。(注射器及玻璃管内充满人体呼出的气体)
1实验中需反复推拉注射器的目的是_______ ;
2在操作中如何判断装置中的O2是否反应完?_______ 。
结论:人体呼出气体中O2的体积分数为16%。
(4)(实验反思)①活动三所用方法与教科书上“测定空气里O2的含量”的方法相比,优点是:_______ (答一点即可)。
②小组同学准确测量人体呼吸前后气体的体积分数如下表所示:
你认为呼吸过程中,氮气含量减少的原因是_______ 。

(1)(活动一)探究人体呼出气体中是否含有CO2
向装有呼出气体的集气瓶中滴加少量澄清石灰水,振荡后观察到
(2)(活动二)探究人体呼出气体中CO2的体积分数(已知:CO2能与NaOH反应)
兴趣小组同学用图1所示装置进行实验。(锥形瓶内充满人体呼出的气体)实验前注射器内液体体积为50mL,向锥形瓶内注入少量液体后,注射器内的液体开始被自动吸入锥形瓶,完全反应后,注射器内NaOH溶液的体积为30mL。
结论:人体呼出气体中CO2的体积分数为
(3)(活动三)探究人体呼出气体中O2的体积分数
兴趣小组同学用图2所示装置进行实验。(注射器及玻璃管内充满人体呼出的气体)
1实验中需反复推拉注射器的目的是
2在操作中如何判断装置中的O2是否反应完?
结论:人体呼出气体中O2的体积分数为16%。
(4)(实验反思)①活动三所用方法与教科书上“测定空气里O2的含量”的方法相比,优点是:
②小组同学准确测量人体呼吸前后气体的体积分数如下表所示:
| 氮气 | 氧气 | 二氧化碳 | 水 | 其他 | |
| 呼入气体 | 78% | 21% | 0.03% | 0.06% | 0.91% |
| 呼出气体 | 75% | 15% | 3.68% | 5.44% | 0.88% |
您最近一年使用:0次
【推荐1】暖贴发热是利用了铁粉生锈放出热量的原理,某小组同学设计并进行下列实验,探究铁生锈的条件及影响铁粉生锈速率的因素。
Ⅰ.探究铁生锈的条件
【设计实验】取3段光亮无锈的细铁丝,绕成螺旋状,进行如图所示的三个实验,实验要保证有足够长的时间来观察现象。
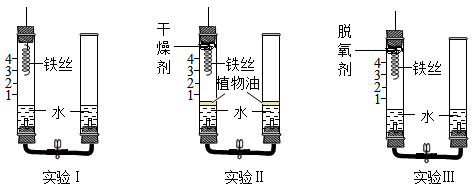
(1)对比实验______ (填序号),可以得出铁生锈需要水;得出“铁生锈需要与氧气接触”这一结论所依据的现象是________ 。
(2)实验Ⅰ中,当铁丝足量,时间足够长,打开止水夹后,还能观察到的现象是__________ 。
Ⅱ.探究影响铁粉生锈速率的因素
【查阅资料】暖贴的发热材料主要有铁粉、活性炭、食盐、水等物质。
【猜想假设】①活性炭能加快铁粉生锈的速率。
②食盐能加快铁粉生锈的速率。
【进行实验】下表是2g铁粉、5g水与不同量的活性炭、食盐均匀混合后,在10分钟内温度上升值的实验记录。
【解释与结论】
(3)上表中x的值为__________ 。
(4)对比实验1和3,得出的结论是_________ 。
(5)欲得出结论“活性炭与食盐同时存在会大幅度加快铁粉生锈速率”,需要对比________ (填实验编号)。
【反思与评价】
(6)下列说法或做法不正确的是_________ (填字母)。
A. 暖贴在使用前不需要密封保存
B. 活性炭粉在暖贴中可以起到分散铁粉,透气、防结块的作用
C. 利用铁生锈的原理,铁粉还可用于食品保鲜
D. 校内用钢架制作的自行车防雨棚应定期喷涂油漆防锈
Ⅰ.探究铁生锈的条件
【设计实验】取3段光亮无锈的细铁丝,绕成螺旋状,进行如图所示的三个实验,实验要保证有足够长的时间来观察现象。

(1)对比实验
(2)实验Ⅰ中,当铁丝足量,时间足够长,打开止水夹后,还能观察到的现象是
Ⅱ.探究影响铁粉生锈速率的因素
【查阅资料】暖贴的发热材料主要有铁粉、活性炭、食盐、水等物质。
【猜想假设】①活性炭能加快铁粉生锈的速率。
②食盐能加快铁粉生锈的速率。
【进行实验】下表是2g铁粉、5g水与不同量的活性炭、食盐均匀混合后,在10分钟内温度上升值的实验记录。
实验编号 | 活性炭/g | 食盐/g | 温度上升值/℃ |
1 | 0 | 0 | 0.1 |
2 | 0.2 | 0 | 22.0 |
3 | 0 | x | 3.1 |
4 | 0.2 | 0.1 | 56.3 |
【解释与结论】
(3)上表中x的值为
(4)对比实验1和3,得出的结论是
(5)欲得出结论“活性炭与食盐同时存在会大幅度加快铁粉生锈速率”,需要对比
【反思与评价】
(6)下列说法或做法不正确的是
A. 暖贴在使用前不需要密封保存
B. 活性炭粉在暖贴中可以起到分散铁粉,透气、防结块的作用
C. 利用铁生锈的原理,铁粉还可用于食品保鲜
D. 校内用钢架制作的自行车防雨棚应定期喷涂油漆防锈
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】兴趣小组的同学为了探究盐酸和硫酸铜溶液能否促进铁钉生锈,做了如图两个实验,一段时间后进行观察,请回答下列问题:

(1)铁钉生锈的条件是______ 。
(2)甲组实验中,b点和c点均比a点生锈多,可以得出的结论是______ 。c点和d点对比,可以看出c点比d点生锈多,是因为d点的铁钉______ 。
(3)乙组实验中,③中试管内液面比②中上升得更快,可能的原因是______ (用化学方程式表示)。
(4)乙组实验得出了硫酸铜溶液也能促进铁钉的生锈,他们观察到的实验现象是______ 。

(1)铁钉生锈的条件是
(2)甲组实验中,b点和c点均比a点生锈多,可以得出的结论是
(3)乙组实验中,③中试管内液面比②中上升得更快,可能的原因是
(4)乙组实验得出了硫酸铜溶液也能促进铁钉的生锈,他们观察到的实验现象是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某实践小组同学参加了“锈外慧中”的项目式学习。对铁的锈蚀与应用进行了进一步的探究。
任务一:探锈——铁锈蚀因素的探究
小雅同学用铁钉探究铁生锈与哪些因素有关,设计了如图所示的实验。

(1)经过一周的观察,试管B和试管C中的铁钉无明显变化,试管A中的铁钉明显锈蚀,说明铁锈是铁与_______ 发生化学反应生成的。
(2)该实验中将蒸馏水煮沸的目的是_______ 。
(3)结合实验结果和生活经验,写一条防止生活中铁制品生锈的方法:_______ 。
任务二:用锈——铁锈蚀原理的应用
小礼同学通过查阅资料了解到暖宝宝发热的原理是利用铁粉生锈放出热量。他购买了某品牌暖宝宝发现原料主要包括铁粉、活性炭、食盐等,针对该暖宝宝的原料进行如下探究活动:
活动一:验证暖宝宝原料中含有铁粉
(4)打开包装后观察到固体为黑色,判断原料含铁粉,但立即被其他同学否定,原因是_______ 。
(5)取少量原料固体于试管中,加入适量稀盐酸,观察到________ 现象。
分析得出结论:暖宝宝中的黑色物质含有铁粉。
活动二:暖宝宝的发热原理再利用
利用暖宝宝的发热原理,小礼设计如图实验装置来测定空气中氧气的含量。实验开始前,在容积为250mL的集气瓶中预装30mL水,量筒中水的读数为100mL。
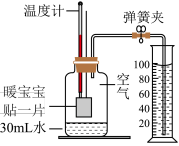
(6)实验开始一段时间后,待装置冷却至室温,打开弹簧夹,水从量筒中流入集气瓶,最后量筒内水为57mL(铁粉生锈消耗水的体积忽略不计),通过计算本实验数据测得空气中氧气的体积分数为_______ (结果精确到0.1%)。
任务一:探锈——铁锈蚀因素的探究
小雅同学用铁钉探究铁生锈与哪些因素有关,设计了如图所示的实验。

(1)经过一周的观察,试管B和试管C中的铁钉无明显变化,试管A中的铁钉明显锈蚀,说明铁锈是铁与
(2)该实验中将蒸馏水煮沸的目的是
(3)结合实验结果和生活经验,写一条防止生活中铁制品生锈的方法:
任务二:用锈——铁锈蚀原理的应用
小礼同学通过查阅资料了解到暖宝宝发热的原理是利用铁粉生锈放出热量。他购买了某品牌暖宝宝发现原料主要包括铁粉、活性炭、食盐等,针对该暖宝宝的原料进行如下探究活动:
活动一:验证暖宝宝原料中含有铁粉
(4)打开包装后观察到固体为黑色,判断原料含铁粉,但立即被其他同学否定,原因是
(5)取少量原料固体于试管中,加入适量稀盐酸,观察到
分析得出结论:暖宝宝中的黑色物质含有铁粉。
活动二:暖宝宝的发热原理再利用
利用暖宝宝的发热原理,小礼设计如图实验装置来测定空气中氧气的含量。实验开始前,在容积为250mL的集气瓶中预装30mL水,量筒中水的读数为100mL。

(6)实验开始一段时间后,待装置冷却至室温,打开弹簧夹,水从量筒中流入集气瓶,最后量筒内水为57mL(铁粉生锈消耗水的体积忽略不计),通过计算本实验数据测得空气中氧气的体积分数为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】某同学设计了如图所示的实验装置探究“分子的性质”,请回答下列问题:
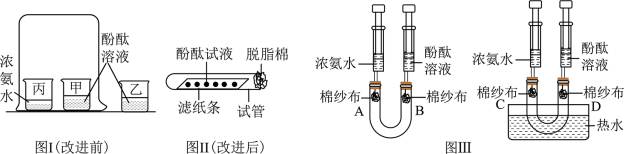
【查阅资料】氨水易分解产生有刺激性气味的氨气。
【进行实验】图Ⅰ是课本中某个探究实验,几分钟后该实验中可以看到的现象是甲烧杯_____ ;其中烧杯乙的作用是_______ ;通过该实验可以得出或推导出一些结论:_______ (答一条即可)。
【实验改进】老师对图Ⅰ所示的装置进行了改进(如图Ⅱ所示),并进行了以下操作:
①取一长条形滤纸,等距离滴加无色酚酞试液;
②将滴加了无色酚酞试液的长条形滤纸放入一洁净的试管中,并在试管口塞一团棉花;
③向脱脂棉上滴加几滴浓氨水。
【分析讨论】实验过程中若发现滤纸条没有变红而棉花变红,其可能原因是_______ 。
【拓展延伸】同学们经过讨论后认为,图Ⅰ、图Ⅱ所示装置虽能证明分子的性质,但不能证明影响分子性质的因素,于是又设计了如图Ⅲ所示的装置。在U型管的两个管口分别放入卷成筒状的棉纱布,并用橡皮塞塞紧。用注射器吸取2mL的酚酞溶液从橡皮塞慢慢注入棉纱布上,使其润湿,从另一管口插入吸取了2mL浓氨水的注射器。按此方法再组装好另一套装置,将其中一套装置的下端放入热水中,并同时向两支U型管中注入浓氨水。
(1)按照图Ⅲ所示的装置进行操作,几分钟后看到的现象是:B、D中棉纱布均变红,且B中棉纱布的变红速率比D要_______ (填“快”或“慢”)。通过该实验现象说明了_______ 。
(2)图Ⅲ所示的实验方法相对于图Ⅱ所示的实验方法,有何优点:_______ 。

【查阅资料】氨水易分解产生有刺激性气味的氨气。
【进行实验】图Ⅰ是课本中某个探究实验,几分钟后该实验中可以看到的现象是甲烧杯
【实验改进】老师对图Ⅰ所示的装置进行了改进(如图Ⅱ所示),并进行了以下操作:
①取一长条形滤纸,等距离滴加无色酚酞试液;
②将滴加了无色酚酞试液的长条形滤纸放入一洁净的试管中,并在试管口塞一团棉花;
③向脱脂棉上滴加几滴浓氨水。
【分析讨论】实验过程中若发现滤纸条没有变红而棉花变红,其可能原因是
【拓展延伸】同学们经过讨论后认为,图Ⅰ、图Ⅱ所示装置虽能证明分子的性质,但不能证明影响分子性质的因素,于是又设计了如图Ⅲ所示的装置。在U型管的两个管口分别放入卷成筒状的棉纱布,并用橡皮塞塞紧。用注射器吸取2mL的酚酞溶液从橡皮塞慢慢注入棉纱布上,使其润湿,从另一管口插入吸取了2mL浓氨水的注射器。按此方法再组装好另一套装置,将其中一套装置的下端放入热水中,并同时向两支U型管中注入浓氨水。
(1)按照图Ⅲ所示的装置进行操作,几分钟后看到的现象是:B、D中棉纱布均变红,且B中棉纱布的变红速率比D要
(2)图Ⅲ所示的实验方法相对于图Ⅱ所示的实验方法,有何优点:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组的同学设计了以下实验,探究教材实验6-2中“碳还原氧化铜”的最佳实验方法。
【实验原理】
(1)写出教材实验6-2中碳和氧化铜反应的化学方程式______ 。
【实验探究】实验Ⅰ:取质量比为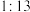 的木炭粉和氧化铜混合物进行实验,根据实验现象对实验效果进行评分(评分越高,效果越好)。
的木炭粉和氧化铜混合物进行实验,根据实验现象对实验效果进行评分(评分越高,效果越好)。
(2)通过实验Ⅰ可得出的结论是装置______ (填“A”或“B”)实验效果较好。
实验Ⅱ:化学兴趣小组的同学在查阅资料后提出了猜想:木炭粉和氧化铜的质量比、木炭的颗粒大小会影响实验效果。于是用实验Ⅰ中效果较好的装置再次进行了实验,根据实验现象对实验效果进行评分。
(3)实验③中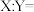
______ 。
【实验结论】
(4)通过实验组合______(填标号)可得到结论:木炭粉和氧化铜质量比为 时效果最好。
时效果最好。
【拓展延伸】
(5)碳还原氧化铜得到的铜中可能含有氧化亚铜,氧化亚铜为红色固体,能与稀硫酸反应: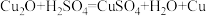 。化学兴趣小组的同学们为验证反应所得红色固体中是否含有氧化亚铜,取一定量红色固体样品,加入足量的稀硫酸,观察到
。化学兴趣小组的同学们为验证反应所得红色固体中是否含有氧化亚铜,取一定量红色固体样品,加入足量的稀硫酸,观察到______ (填写实验现象),说明所得红色固体中含有氧化亚铜。
【实验原理】
(1)写出教材实验6-2中碳和氧化铜反应的化学方程式
【实验探究】实验Ⅰ:取质量比为
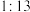 的木炭粉和氧化铜混合物进行实验,根据实验现象对实验效果进行评分(评分越高,效果越好)。
的木炭粉和氧化铜混合物进行实验,根据实验现象对实验效果进行评分(评分越高,效果越好)。| 装置序号 | A | B |
| 装置 | 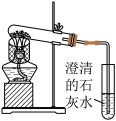 | 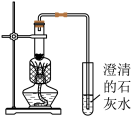 |
| 实验现象 | 黑色固体中有极少量 红色固体 | 出现红热现象,黑色固体 中有少量红色固体 |
| 实验效果评分 | 3.5 | 4.1 |
实验Ⅱ:化学兴趣小组的同学在查阅资料后提出了猜想:木炭粉和氧化铜的质量比、木炭的颗粒大小会影响实验效果。于是用实验Ⅰ中效果较好的装置再次进行了实验,根据实验现象对实验效果进行评分。
| 实验组 | 第一组 | 第二组 | ||||||
| 实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 木炭粉和氧化铜的质量比 | 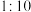 |  |  | 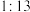 | 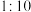 |  | 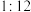 | 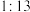 |
| 木炭颗粒 | 细 | 细 | 细 | 细 | 极细 | 极细 | 极细 | 极细 |
| 实验效果评分 | 6.3 | 6.9 | 5.1 | 3.8 | 7.8 | 9.2 | 6.8 | 4.0 |
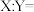
【实验结论】
(4)通过实验组合______(填标号)可得到结论:木炭粉和氧化铜质量比为
 时效果最好。
时效果最好。| A.①②③④ | B.①②⑦⑧ | C.⑤⑥⑦⑧ | D.③④⑤⑥ |
【拓展延伸】
(5)碳还原氧化铜得到的铜中可能含有氧化亚铜,氧化亚铜为红色固体,能与稀硫酸反应:
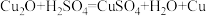 。化学兴趣小组的同学们为验证反应所得红色固体中是否含有氧化亚铜,取一定量红色固体样品,加入足量的稀硫酸,观察到
。化学兴趣小组的同学们为验证反应所得红色固体中是否含有氧化亚铜,取一定量红色固体样品,加入足量的稀硫酸,观察到
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】探究影响锌与稀硫酸反应快慢的因素。可选用的实验仪器与装置如图:

实验过程中,控制其他条件均相同,进行4组实验,获得数据如下表。
(1)设计能控制H2制备、测量H2体积的装置,应选的仪器为_____ (填编号)。
(2)比较实验b和实验c,可以得到的结论是_____ 。
(3)为了研究硫酸浓度对反应快慢的影响,需比较实验是_____ (填编号)。
(4)a和c比较,比较影响锌与硫酸反应的快慢各因素的间大小关系_____ 。

实验过程中,控制其他条件均相同,进行4组实验,获得数据如下表。
| 实验编号 | 不同纯度的锌 | 试剂/相同体积和不同浓度的稀硫酸 | 收集前10min内产生的氢气体积(mL) |
| a | 纯锌 | 30mL35% | 626.5 |
| b | 纯锌 | 30mL30% | 564.3 |
| c | 含杂质的锌 | 30mL30% | 634.7 |
| d | 纯锌 | 30mL20% | 449.3 |
(1)设计能控制H2制备、测量H2体积的装置,应选的仪器为
(2)比较实验b和实验c,可以得到的结论是
(3)为了研究硫酸浓度对反应快慢的影响,需比较实验是
(4)a和c比较,比较影响锌与硫酸反应的快慢各因素的间大小关系
您最近一年使用:0次



