如图1所示是两种固体A、B的溶解度曲线。
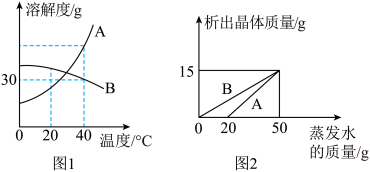
(1)在20℃时,将固体A、B各30g分别加入100g水中,充分溶解后,所得溶液的质量较大的是_____ (填“A”或“B”)溶液。
(2)若A中混有少量B,提纯A的方法是_____ (填“升温结晶”或“降温结晶”)。
(3)在40℃时,将一定质量的A、B溶液分别进行恒温蒸发,析出晶体的质量与蒸发水的质量关系如图2所示,则40℃时A的溶解度为_____ 。蒸发过程中,溶质质量分数始终保持不变的是 ____ 溶液(填“A”或“B”)。

(1)在20℃时,将固体A、B各30g分别加入100g水中,充分溶解后,所得溶液的质量较大的是
(2)若A中混有少量B,提纯A的方法是
(3)在40℃时,将一定质量的A、B溶液分别进行恒温蒸发,析出晶体的质量与蒸发水的质量关系如图2所示,则40℃时A的溶解度为
更新时间:2023-08-20 09:19:08
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
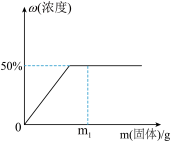
【推荐1】在室温下,向50g的水中加入某固体物质,所得溶液的质量分数(ω)与加入该物质的质量(m)的对应关系,如图所示。______ 。
(2)根据图,该固态物质在室温下的溶解度为______ g。
(3)若加入的固体物质质量为m1时,将混合体系的温度降低,所得溶液的浓度小于50%,则该物质的溶解度随温度升高而______ (填“增大”、“减小”或“不变”)。在室温下,加入的固体物质质量为m1时,若再加入30g水,固体恰好完全溶解,则m1=______ 。
(2)根据图,该固态物质在室温下的溶解度为
(3)若加入的固体物质质量为m1时,将混合体系的温度降低,所得溶液的浓度小于50%,则该物质的溶解度随温度升高而
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】NaCl、KNO3的部分溶解度数据见下表。
(1)20°C时KNO3的溶解度是________ 。
(2)在____ 温度范围内,NaCl和KNO3饱和溶液溶质质量分数可能相等;
(3)从含有84.5g KNO3和9gNaCl的混合物中提纯KNO3,不考虑实验过程中的提耗,进行如下实验:

①最终得到KNO3固体的质量为______ ; KNO3固体②对整个实验过程分析正确的是______ 。
A.若溶液1直接降温至20°C,析出KNO3的质量变少
B.溶液2为KNO3的饱和溶液
C.为得到更多纯净的KNO3固体,溶液3最多还可以恒温蒸发25g水
D.上述方法能将NaCl和KNO3完全分离
| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 20.9 | 31.6 | 45.8 | 64 | 110 | 169 | 246 |
| NaCl | 35.8 | 36 | 36.3 | 37 | 37 | 38.4 | 39.8 | |
(2)在
(3)从含有84.5g KNO3和9gNaCl的混合物中提纯KNO3,不考虑实验过程中的提耗,进行如下实验:

①最终得到KNO3固体的质量为
A.若溶液1直接降温至20°C,析出KNO3的质量变少
B.溶液2为KNO3的饱和溶液
C.为得到更多纯净的KNO3固体,溶液3最多还可以恒温蒸发25g水
D.上述方法能将NaCl和KNO3完全分离
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】硫酸亚铁铵晶体俗称摩尔盐,化学式为FeSO4·(NH4)2SO4·6H2O,在制药、电镀方面有广泛的应用。某化学兴趣小组的学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如下:

资料:①硫酸亚铁铵晶体易溶于水,不溶于酒精;硫酸亚铁铵晶体在100℃~110℃时分解。
②相关物质的溶解度(单位:g)如下表:
请回答下列问题:
(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍。碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH_______ 7(选填“>”、“<”或“=”)。
(2)①中发生反应的化学方程式为_____________________________ 。
(3)操作①中过滤时,要趁热进行的原因是____________ ,过滤后得到的固体中一定含有的物质是 ________ 。
(4)操作③中使用无水酒精洗涤,可快速晾干。这样做的优点是________ (填字母)。
A 避免用水洗涤所造成的晶体损耗
B 酒精易挥发,可低温晾干晶体

资料:①硫酸亚铁铵晶体易溶于水,不溶于酒精;硫酸亚铁铵晶体在100℃~110℃时分解。
②相关物质的溶解度(单位:g)如下表:
| 温度/℃ | FeSO4 | (NH4) 2SO4 | FeSO4·(NH4)2SO4·6H2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21. 6 |
| 30 | 32.9 | 78 | 28.1 |
(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍。碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH
(2)①中发生反应的化学方程式为
(3)操作①中过滤时,要趁热进行的原因是
(4)操作③中使用无水酒精洗涤,可快速晾干。这样做的优点是
A 避免用水洗涤所造成的晶体损耗
B 酒精易挥发,可低温晾干晶体
您最近一年使用:0次
【推荐2】 和KCl两种固体的溶解度曲线如图所示。
和KCl两种固体的溶解度曲线如图所示。
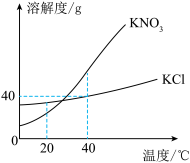
(1)20℃时, 的溶解度
的溶解度________ (填“大于”“等于”或“小于”)KCl。
(2)40℃时,将70gKCl的饱和溶液稀释成质量分数为20%的溶液,需加水________ mL(水的密度看作1g/mL);若在量取水的体积时,仰视读数(其他操作无误),最终所得溶液的质量分数________ (填“大于”或“小于”)20%。
 和KCl两种固体的溶解度曲线如图所示。
和KCl两种固体的溶解度曲线如图所示。
(1)20℃时,
 的溶解度
的溶解度(2)40℃时,将70gKCl的饱和溶液稀释成质量分数为20%的溶液,需加水
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】如图是a、b、c三种物质的溶解度曲线。请根据图中信息回答下列问题:

(1)P点的含义是______ ;
(2)t3℃时,把30克a充分溶解在50克水中,所得溶液溶质质量分数是______ ;(保留两位小数)
(3)t3℃时,a、b、c三种物质的等质量饱和溶液中,所含溶剂质量由大到小的顺序是______ ;
(4)将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为______ ;
(5)若a中混有少量b,要得到纯净的a,常用的提纯方法是______ 。

(1)P点的含义是
(2)t3℃时,把30克a充分溶解在50克水中,所得溶液溶质质量分数是
(3)t3℃时,a、b、c三种物质的等质量饱和溶液中,所含溶剂质量由大到小的顺序是
(4)将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为
(5)若a中混有少量b,要得到纯净的a,常用的提纯方法是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】研究物质的溶解对于生产、生活有着重要意义。下表是碳酸钠的部分溶解度数据。
(1)由表中数据可知,碳酸钠属于________ 物质(填“易溶”“可溶”“微溶”或“难溶”)。
(2)由表中数据可知,碳酸钠的溶解度随温度升高________ 。
(3)小东同学进行了如下图所示的实验,请比较②③④中溶质质量分数的大小____ ,若使烧杯③中的溶液达到饱和,至少需再加入___ g碳酸钠;升温至60℃时,烧杯④中会出现的现象是___ 。

(4)40℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中。向烧杯中加入适量某物质后,试管底部的粉末增加,则加入的物质可能是 (填字母序号)。
(5)t℃时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量关系绘制成如图所示斜线。下列说法错误的是 (填字母序号)。

| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| 溶解度/g | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 | 45.1 | 44.7 |
(1)由表中数据可知,碳酸钠属于
(2)由表中数据可知,碳酸钠的溶解度随温度升高
(3)小东同学进行了如下图所示的实验,请比较②③④中溶质质量分数的大小

(4)40℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中。向烧杯中加入适量某物质后,试管底部的粉末增加,则加入的物质可能是 (填字母序号)。
| A.氢氧化钠 | B.生石灰 | C.硝酸铵 | D.氯化钠 |
(5)t℃时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量关系绘制成如图所示斜线。下列说法错误的是 (填字母序号)。

| A.t℃时该物质的溶解度是20g |
| B.该物质的溶解度随温度的升高而增大 |
| C.N点所示的溶液中溶质质量分数是10% |
| D.图中4个点所示的溶液中溶质质量分数大小关系是N<M<G=Q |
您最近一年使用:0次
【推荐2】生活、生产、环保等都离不开化学。我们学习了化学知识后,观察物质世界就要从化学视角看。
(1)节假日,某班同学去郊外进行野炊活动。请回答下列问题。
①他们所带的下列物品中,主要材料属于合成高分子材料的是___________ 。(填序号)
a.纯净水 b.塑料凳子 c.铁锅 d.棉布围裙 e.自行车轮胎
②有些同学所骑自行车的链条生锈了,请你帮助分析:链条生锈的原因是链条与空气中的__________ 发生了化学反应。
③洗涤剂可用来洗碗,是因为它对油污具有__________ 功能。
(2)水是生命之源,也是人类最宝贵的资源。水是最重要的溶剂,可以配制不同的溶液。
①20℃时,NaCl的溶解度是36g。该温度下,饱和食盐水中溶质与溶液的质量比为__________ 。
②某酒精溶液中,酒精分子与水分子中含有的氢原子个数比是1:1。则酒精溶液中溶质的质量分数为__________ 。
(1)节假日,某班同学去郊外进行野炊活动。请回答下列问题。
①他们所带的下列物品中,主要材料属于合成高分子材料的是
a.纯净水 b.塑料凳子 c.铁锅 d.棉布围裙 e.自行车轮胎
②有些同学所骑自行车的链条生锈了,请你帮助分析:链条生锈的原因是链条与空气中的
③洗涤剂可用来洗碗,是因为它对油污具有
(2)水是生命之源,也是人类最宝贵的资源。水是最重要的溶剂,可以配制不同的溶液。
①20℃时,NaCl的溶解度是36g。该温度下,饱和食盐水中溶质与溶液的质量比为
②某酒精溶液中,酒精分子与水分子中含有的氢原子个数比是1:1。则酒精溶液中溶质的质量分数为
您最近一年使用:0次

 时,若
时,若 ,则该溶液属于
,则该溶液属于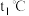 时,将NaCl、
时,将NaCl、



