质量守恒定律的发现对化学的发展做出了重要贡献。
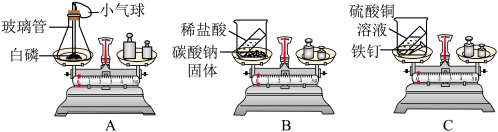
(1)用如图所示的3个实验验证质量守恒定律,其中实验前后天平不能保持平衡的是_______ (填字母),理由是_______ 。
(2)A实验中气球的作用是:_______ 。
(3)从微观角度分析,化学反应中质量守恒的原因_______ 。

(1)用如图所示的3个实验验证质量守恒定律,其中实验前后天平不能保持平衡的是
(2)A实验中气球的作用是:
(3)从微观角度分析,化学反应中质量守恒的原因
更新时间:2023-11-21 11:21:31
|
相似题推荐
实验题
|
适中
(0.65)
【推荐1】下列实验均用到红磷或白磷,请分析并回答相关问题。
(1)实验1中红磷要过量的目的是___________ 。
(2)实验2中红磷___________ (填“需要”或“不需要”)过量。
(3)实验1中,为达到实验目的,红磷___________ (填“能”或“不能”)用铁丝替代。
(4)实验3铜片上的红磷未燃烧的原因是___________ ,烧杯中热水的作用___________ (填一条即可)。
| ||
| 实验1测定空气里氧气的含量 | 实验2红磷燃烧前后质量的测定 | 实验3燃烧条件的实验 |
(1)实验1中红磷要过量的目的是
(2)实验2中红磷
(3)实验1中,为达到实验目的,红磷
(4)实验3铜片上的红磷未燃烧的原因是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如图)。观察到镁条在空气中剧烈燃烧,发出耀眼的白光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。

(1)实验前,用砂纸打磨镁条的目的是______ ,写出镁条燃烧的化学方程式_____ 。
(2)通过称量发现:在石棉网上收集到的产物的质量小于镁条的质量。你认为出现这一实验结果的原因可能是______ 。
(3)小红按如图所示的改进装置验证质量守恒定律,发现白色固体中含有少量黄色固体。
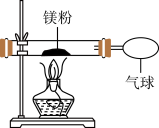
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色固体氮化镁(Mg3N2)
③氮化镁可与水剧烈反应白色固体【Mg(OH)2】和氨气(NH3),氨气能使湿润的红色石蕊试纸变蓝。
【作出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想。
【反思与交流】①空气中氮气(N2)和氧气(O2)的体积比约为______ ,可是镁条在空气中的燃烧产物MgO却远多于Mg3N2,合理的解释是_______ 。
②氮化镁与水反应的化学方程式______ 。

(1)实验前,用砂纸打磨镁条的目的是
(2)通过称量发现:在石棉网上收集到的产物的质量小于镁条的质量。你认为出现这一实验结果的原因可能是
(3)小红按如图所示的改进装置验证质量守恒定律,发现白色固体中含有少量黄色固体。

【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色固体氮化镁(Mg3N2)
③氮化镁可与水剧烈反应白色固体【Mg(OH)2】和氨气(NH3),氨气能使湿润的红色石蕊试纸变蓝。
【作出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想。
| 实验操作 | 实验现象 | 结论 |
| a.取少量产物中的黄色固体于试管中,并往其中加入适量的 b.在试管口放置一片湿润的红色石蕊试纸 | 生成有刺激性气味的气体,试纸由红色变成 | 猜想正确 |
②氮化镁与水反应的化学方程式
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】某化学小组同学,用如图所示实验探究质量守恒定律。

(1)充分反应冷却后,天平仍然平衡的是________ (填字母序号),其反应的化学方程式为________ ;另一个不平衡的原因是___________ 。
(2)由上述实验可知,在化学反应前后,一定不变的是______ (填序号)。
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类

(1)充分反应冷却后,天平仍然平衡的是
(2)由上述实验可知,在化学反应前后,一定不变的是
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组开启寻镁之旅。
(一)探究金属Mg。镁是一种______ 色的固体,质软,有导电性;将镁条放入食醋中,观察到固体消失,产生大量______ ,放热。
(二)制备金属Mg。工业上用电解氯化镁的方法生产镁,其原理:MgCl2 Mg+Cl2。该反应属于
Mg+Cl2。该反应属于______ 反应。(填反应基本类型)
(三)再探金属镁。兴趣小组用下图装置进行镁条在空气中燃烧的实验。

【资料】Ⅰ、镁+氮气 氮化镁,氮化镁是一种黄绿色固体。
氮化镁,氮化镁是一种黄绿色固体。
Ⅱ、镁在二氧化碳中燃烧,生成炭黑和一种白色固体。
(1)写出Ⅱ中反应的表达式______ 。
(2)实验后,进入集气瓶中水的体积约占容积的70%。经分析,镁燃烧时一定还消耗了氮气。理由是______ 。
(3)银白色的镁条表面常有一层灰黑色的“外衣“,
Ⅰ、甲同学认为该外衣是MgO,遭到否定,否定的理由是______ 。
Ⅱ、查阅资料:镁条变黑是因为生成了碱式碳酸镁[Mg2 (OH)2CO3],其性质与铜绿相似,写出碱式碳酸镁受热分解的表达式______ 。
(一)探究金属Mg。镁是一种
(二)制备金属Mg。工业上用电解氯化镁的方法生产镁,其原理:MgCl2
 Mg+Cl2。该反应属于
Mg+Cl2。该反应属于(三)再探金属镁。兴趣小组用下图装置进行镁条在空气中燃烧的实验。

【资料】Ⅰ、镁+氮气
 氮化镁,氮化镁是一种黄绿色固体。
氮化镁,氮化镁是一种黄绿色固体。Ⅱ、镁在二氧化碳中燃烧,生成炭黑和一种白色固体。
(1)写出Ⅱ中反应的表达式
(2)实验后,进入集气瓶中水的体积约占容积的70%。经分析,镁燃烧时一定还消耗了氮气。理由是
(3)银白色的镁条表面常有一层灰黑色的“外衣“,
Ⅰ、甲同学认为该外衣是MgO,遭到否定,否定的理由是
Ⅱ、查阅资料:镁条变黑是因为生成了碱式碳酸镁[Mg2 (OH)2CO3],其性质与铜绿相似,写出碱式碳酸镁受热分解的表达式
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组利用镁条验证质量守恒定律。
(1)小组成员小明取一根用砂纸打磨干净的长镁带和一个石棉网,将它们一起放在托盘天平上,称量好质量。取下石棉网,在石棉网上方点燃镁带,燃烧结束后将所得的物质与石棉网一起再放回托盘天平上称量,小明发现质量减轻了,如图所示。请回答以下问题。

①请写出镁条与氧气反应的化学方程式____ 。并请你分析产生“质量减轻”这一现象的原因可能是____ 。
②小明认为这个反应不遵循质量守恒定律。你_______ (“同意”或“不同意”)小明的观点,请从微观角度说明你的理由:_______ 。
(2)小组成员小红按下图装置改进实验验证了质量守恒定律,却发现产物白色固体中还有少量黄色固体。查阅资料得知:镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体。请写出镁和氮气反应的化学方程式:_______ 。

①空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释_______ 。
②实验中气球的作用除了使装置密闭之外,还可以防止_______ ;实验时若取用镁的量不足,对实验的结果_______ (选填“有”或“没有”)影响。
(3)小组成员小丽将镁条放入Na2CO3溶液(Na2CO3溶于水得到的混合物)中,意外发现快速产生了较多气泡,有白色沉淀生成。并利用如图装置称量反应前后的质量,发现药混合前、后质量关系为:m前>m后。

①请你解释质量减轻的原因_______ 。
②小组同学对反应产生的气体作出如下猜想:可能是氢气;可能是二氧化碳;也可能是氢气和二氧化碳。请你说明做出以上三种猜想的依据是_______ 。
(1)小组成员小明取一根用砂纸打磨干净的长镁带和一个石棉网,将它们一起放在托盘天平上,称量好质量。取下石棉网,在石棉网上方点燃镁带,燃烧结束后将所得的物质与石棉网一起再放回托盘天平上称量,小明发现质量减轻了,如图所示。请回答以下问题。

①请写出镁条与氧气反应的化学方程式
②小明认为这个反应不遵循质量守恒定律。你
(2)小组成员小红按下图装置改进实验验证了质量守恒定律,却发现产物白色固体中还有少量黄色固体。查阅资料得知:镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体。请写出镁和氮气反应的化学方程式:

①空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释
②实验中气球的作用除了使装置密闭之外,还可以防止
(3)小组成员小丽将镁条放入Na2CO3溶液(Na2CO3溶于水得到的混合物)中,意外发现快速产生了较多气泡,有白色沉淀生成。并利用如图装置称量反应前后的质量,发现药混合前、后质量关系为:m前>m后。

①请你解释质量减轻的原因
②小组同学对反应产生的气体作出如下猜想:可能是氢气;可能是二氧化碳;也可能是氢气和二氧化碳。请你说明做出以上三种猜想的依据是
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐1】学习了碳酸钠(Na2CO3)的性质后,课题小组运用课堂学习的方法,合作探究家庭蒸馒头用到的小苏打(NaHCO3)的性质,请回答下列问题。
【基础实验记录与分析】
(1)填写下表。
【拓展实验记录与分析】
(2)同学们通过查阅资料,在老师的指导下采用下图所示装置对小苏打和碳酸钠做了对比实验。实验中小试管内沾有白色固体无水硫酸铜粉末的棉花球变蓝色,a烧杯中石灰水无明显现象,b烧杯中石灰水出现白色浑浊,通过该实验得出的结论是:碳酸氢钠受热________ ,生成物中有水和二氧化碳气体。碳酸钠受热________ 。

【反思与拓展】
(3)①甲同学分析实验一得出:盐溶液________ (选填“一定”或“不一定”)显中性。
②乙同学用稀硫酸代替实验二中的稀盐酸进行探究,发现实验现象相同。从微观角度分析,这是因为稀盐酸和稀硫酸中都含有________ 。
③医疗上,小苏打( NaHCO3)可以治疗胃酸(主要成分是盐酸)过多;依据的原理是是实验二得出的结论该反应的化学方程式_______ 。
【基础实验记录与分析】
(1)填写下表。
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
实验现象 | 溶液由无色变为红色 | 固体溶解,生成无色气泡 | 生成白色沉淀 |
实验结论 | 碳酸氢钠溶液显 |
【拓展实验记录与分析】
(2)同学们通过查阅资料,在老师的指导下采用下图所示装置对小苏打和碳酸钠做了对比实验。实验中小试管内沾有白色固体无水硫酸铜粉末的棉花球变蓝色,a烧杯中石灰水无明显现象,b烧杯中石灰水出现白色浑浊,通过该实验得出的结论是:碳酸氢钠受热

【反思与拓展】
(3)①甲同学分析实验一得出:盐溶液
②乙同学用稀硫酸代替实验二中的稀盐酸进行探究,发现实验现象相同。从微观角度分析,这是因为稀盐酸和稀硫酸中都含有
③医疗上,小苏打( NaHCO3)可以治疗胃酸(主要成分是盐酸)过多;依据的原理是是实验二得出的结论该反应的化学方程式
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为“去除粗盐中难溶性杂质并计算产率”的实验操作示意图。
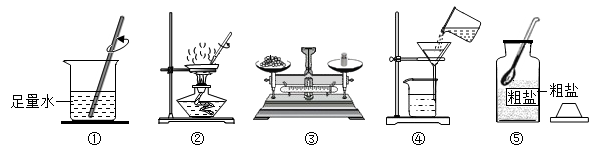
(1)上述操作的合理排序为______ (填序号)、计算产率;
(2)操作②中,用玻璃棒的作用是______ ;
(3)通过以上操作只能除去粗盐中难溶性杂质,欲除去可溶性杂质如MgCl2、CaCl2还需依次用到NaOH溶液、Na2CO3溶液和稀盐酸(三种药品均过量)
①加入NaOH溶液发生的化学反应方程式为______ ;
②稀盐酸的作用是_____ ;
③除去可溶性杂质后计算出NaCl的产率γ,γ______ (填“可能”或“不可能”)大于100%。

(1)上述操作的合理排序为
(2)操作②中,用玻璃棒的作用是
(3)通过以上操作只能除去粗盐中难溶性杂质,欲除去可溶性杂质如MgCl2、CaCl2还需依次用到NaOH溶液、Na2CO3溶液和稀盐酸(三种药品均过量)
①加入NaOH溶液发生的化学反应方程式为
②稀盐酸的作用是
③除去可溶性杂质后计算出NaCl的产率γ,γ
您最近一年使用:0次









