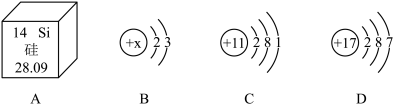
如图中A是锡元素在元素周期表中的信息,B、C分别为两种粒子的结构示意图,D为元素周期表中的部分信息,请根据图中信息回答下列问题:

(1)锡元素的相对原子质量是_______ 。
(2)B表示的原子,其核外电子数是_______ ,若C表示氯离子,则x=_______ 。
(3)元素在元素周期表中的分布是有规律的,D中甲的原子序数_______ (填“大于”或“小于”)乙的原子序数。乙所代表的元素,属于_______ (填“金属”“非金属”或“稀有气体”)元素。
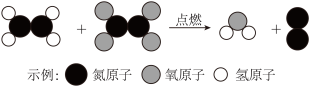
(4)很久之前运载火箭使用联氨(N2H4)和四氧化二氮气体作为火箭动力,如上图是联氨和四氧化二氮反应的微观示意图,请写出其化学反应方程式_______ ,从上图微观示意图中,可得出的结论是_______ (任写一个即可)。

(1)锡元素的相对原子质量是
(2)B表示的原子,其核外电子数是
(3)元素在元素周期表中的分布是有规律的,D中甲的原子序数

(4)很久之前运载火箭使用联氨(N2H4)和四氧化二氮气体作为火箭动力,如上图是联氨和四氧化二氮反应的微观示意图,请写出其化学反应方程式
更新时间:2024-01-16 18:55:25
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】请沿用科学家认识事物的方式认识“空气”。
(1)从分类角度:空气属于_______ (填“混合物”或“纯净物”)。
(2)从微观角度:用“ ”表示氮原子,“
”表示氮原子,“ ”表示氧原子。
”表示氧原子。
①用“ ”可表示的微粒是
”可表示的微粒是_______ (填名称)。
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,下图可表示空气微观模型的是_______ (填标号)。
A. B.
B.  C.
C. 
(3)从变化角度:已知:常压下,氮气沸点-196℃,氧气沸点-183℃。将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是_______ 。
(1)从分类角度:空气属于
(2)从微观角度:用“
 ”表示氮原子,“
”表示氮原子,“ ”表示氧原子。
”表示氧原子。①用“
 ”可表示的微粒是
”可表示的微粒是②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,下图可表示空气微观模型的是
A.
 B.
B.  C.
C. 
(3)从变化角度:已知:常压下,氮气沸点-196℃,氧气沸点-183℃。将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】某物质在点燃的条件下发生反应,生成物和反应物共四种,它们的微观示意图和反应前后的质量如表所示。
(1)由 构成的物质中
构成的物质中 所代表的元素的化合价为
所代表的元素的化合价为_____ ;
(2)表中的四种物质中,属于氧化物的是_____ (填化学式);
(3)上述反应的化学方程式为_______________________ 。
| 物质序号 | 甲 | 乙 | 丙 | 丁 |  |
| 微观示意图 |  | 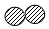 | 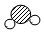 |  | |
| 反应前质量/g | 68 | 100 | 1 | 0 | |
| 反应后质量/g | 0 | x | y | z |
(1)由
 构成的物质中
构成的物质中 所代表的元素的化合价为
所代表的元素的化合价为(2)表中的四种物质中,属于氧化物的是
(3)上述反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】水是生命之源,人类的日常生活与工农业生产都离不开水。

(1)图1为电解水的实验装置图,接通电源观察两电极都有气泡产生,发生反应的化学方程式为____________________ ,通电一段时间后,玻璃管a收集到的气体是_____ ,可用_____ 检验玻璃管b中气体。
(2)已知同温同压下,气体的体积比决定于气体的分子数之比。该实验中能说明水的化学式为“H2O”的实验现象是____________________ 。
(3)水电解的过程可用下列图示表示。该反应发生时,微粒运动变化的先后顺序是___ 。


(4)下列是几种常见的净水方法:①过滤 ②活性炭吸附 ③用漂白粉消毒
④静置沉降 ⑤加明矾沉降 ⑥蒸馏
请从物质变化的角度,选择一种分类标准对以上6个过程进行分类:分类标准________ ,包括事例________ (填序号)。
(5)图2是探究燃烧条件的实验,烧杯中热水的作用一是提供热量,二是______________ 。
(6)小海用图3装置验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸
而不是水或二氧化碳,应该采取的实验操作顺序是___ (填序号)。

①从b端通氮气
②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳
④从分液漏斗中滴加适量水

(1)图1为电解水的实验装置图,接通电源观察两电极都有气泡产生,发生反应的化学方程式为
(2)已知同温同压下,气体的体积比决定于气体的分子数之比。该实验中能说明水的化学式为“H2O”的实验现象是
(3)水电解的过程可用下列图示表示。该反应发生时,微粒运动变化的先后顺序是

| A.①②③④ | B.④①③② | C.①②④⑨ | D.①④③② |

(4)下列是几种常见的净水方法:①过滤 ②活性炭吸附 ③用漂白粉消毒
④静置沉降 ⑤加明矾沉降 ⑥蒸馏
请从物质变化的角度,选择一种分类标准对以上6个过程进行分类:分类标准
(5)图2是探究燃烧条件的实验,烧杯中热水的作用一是提供热量,二是
(6)小海用图3装置验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸
而不是水或二氧化碳,应该采取的实验操作顺序是

①从b端通氮气
②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳
④从分液漏斗中滴加适量水
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)根据下列粒子的结构示意图,回答问题。

①图中粒子共表示_____ 种元素(填数字)。
②与A原子的化学性质最相似的是_____ (填序号)。
③ 写出B与C形成的化合物的化学式:_____ 。
(2)下图为某化学反应的微观示意图。

根据图示写出反应的符号表达式或化学方程式_____ 。
(1)根据下列粒子的结构示意图,回答问题。

①图中粒子共表示
②与A原子的化学性质最相似的是
③ 写出B与C形成的化合物的化学式:
(2)下图为某化学反应的微观示意图。

根据图示写出反应的符号表达式或化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】1.原子序数11—17元素的符号和原子结构示意图如下,请结合下图回答:

(1)原子序数为15的元素名称为_______ 原子的最外层有______ 电子;
(2)结合上图用符号表示下列内容:
①原子序数为13的原子形成的离子符号____________ ,
②原子序数为12、17的元素组成化合物的化学式_______________ 。
(3)从Na-Cl,随着原子序数的增加,其原子结构(或元素的性质)呈现出的变化规律是:_________________________ 。(任写一条)

(1)原子序数为15的元素名称为
(2)结合上图用符号表示下列内容:
①原子序数为13的原子形成的离子符号
②原子序数为12、17的元素组成化合物的化学式
(3)从Na-Cl,随着原子序数的增加,其原子结构(或元素的性质)呈现出的变化规律是:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】2017年4月我国的研究人员已研发出锂-氮充电电池(Li-N2),结构如下图。该电池由锂箔作阳极,碳布作阴极,玻璃纤维作隔板。Li-N2电池可在环境温度条件下,在大气氮中运行,该电池反应方程式:6Li+N2=2Li3N。请回答:


(1)空气中氮气的体积分数约为_________ 。
(2)Li3N中氮元素的化合价为__________ 。
(3)锂原子的原子核内质子数为______ ,它在化学反应中易______ (填“得到”或“失去”)电子。
(4)玻璃纤维是玻璃熔融状态下抽成丝制得,它属于 (填序号)。
(5)碳布可作为锂-氮电池的电极,是利用了碳单质的________________ (填一种物理性质即可)。


(1)空气中氮气的体积分数约为
(2)Li3N中氮元素的化合价为
(3)锂原子的原子核内质子数为
(4)玻璃纤维是玻璃熔融状态下抽成丝制得,它属于 (填序号)。
| A.无机非金属材料 | B.金属材料 | C.有机高分子材料 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】宏观和微观相结合是认识物质结构与性质的重要方法。
(1)氧原子的结构示意图为 ,硫原子的结构示意图为
,硫原子的结构示意图为 。
。
①一个硫原子得到二个电子形成一种新粒子,该粒子的符号为__________ 。
②氧气和硫单质分别与氢气反应生成H2O和H2S。H2O、H2S中氧与硫元素的化合价均为-2价,从原子结构上分析它们化合价相同的原因是__________ 。
(2)硫及其化合物的“化合价一物质类别”关系图如图所示。物质X的化学式为________ 。

(3)过氧乙酸溶液是常用的消毒液。过氧乙酸(C2H4O2)无色且有辛辣味;具有强氧化性,温度稍高即分解放出氧气并生成醋酸(C2H4O3)。其分解的化学方程式为___________ 。
(1)氧原子的结构示意图为
 ,硫原子的结构示意图为
,硫原子的结构示意图为 。
。①一个硫原子得到二个电子形成一种新粒子,该粒子的符号为
②氧气和硫单质分别与氢气反应生成H2O和H2S。H2O、H2S中氧与硫元素的化合价均为-2价,从原子结构上分析它们化合价相同的原因是
(2)硫及其化合物的“化合价一物质类别”关系图如图所示。物质X的化学式为

(3)过氧乙酸溶液是常用的消毒液。过氧乙酸(C2H4O2)无色且有辛辣味;具有强氧化性,温度稍高即分解放出氧气并生成醋酸(C2H4O3)。其分解的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】核电荷数为1~18的元素原子结构示意图等信息如图,回答下列问题:

(1)氧元素与硫元素化学性质相似,主要是因为___________ 。
(2)由11号元素和17号元素组成的化合物的化学式为___________ 。
(3)在第三周期中,各原子结构的共同之处是___________ ;该周期中,各原子核外电子排布的变化规律是___________ 。
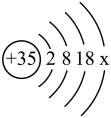
(4)第35号元素是溴元素,其原子结构示意图如图,在元素周期表中溴元素应该排在___________ 元素(填元素符号)的下方。

(1)氧元素与硫元素化学性质相似,主要是因为
(2)由11号元素和17号元素组成的化合物的化学式为
(3)在第三周期中,各原子结构的共同之处是
(4)第35号元素是溴元素,其原子结构示意图如图,在元素周期表中溴元素应该排在

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】铝是地壳中含量最高的金属,作为材料新秀,薄如蝉認的铝箔应用广泛。
(1)铝材能加工成薄如蝉翼的铝箔,是因为铝具有很好的____ 性,铝箔用作空调热交换器翅片是利用了铝的____ 性。
(2)铝具有很好的抗腐蚀性能,是因为铝在空气中发生反应生成的保护膜阻止其进一步被氧化,保护膜的成分是____ 。
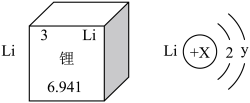
(3)在新能源汽车的动力锂电池中,铝管作正极集流体,承载电极活性物质LiFePO4。元素周期表中,Li的相关信息如图所示,则x、y的值分别为___ 。__ 。
(4)铝、钛等金属与稀土形成的特种合金常用于航空、航天领域。关于稀土资源,下列说法正确的是____(填字母)。
(1)铝材能加工成薄如蝉翼的铝箔,是因为铝具有很好的
(2)铝具有很好的抗腐蚀性能,是因为铝在空气中发生反应生成的保护膜阻止其进一步被氧化,保护膜的成分是
(3)在新能源汽车的动力锂电池中,铝管作正极集流体,承载电极活性物质LiFePO4。元素周期表中,Li的相关信息如图所示,则x、y的值分别为
(4)铝、钛等金属与稀土形成的特种合金常用于航空、航天领域。关于稀土资源,下列说法正确的是____(填字母)。
| A.稀土的开采与环境、生态问题无关 |
| B.稀土广泛应用于新材料领域 |
| C.我国的稀土储量目前居世界第一位 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是元素周期表的部分内容,请认真分析并回答后面的问题:
(1)请从上表中查出地壳中含量最多的非金属元素的相对原子质量为___________ 。
(2)表中不同种元素最本质的区别是___________(填序号):
(3)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:___________(填字母序号)
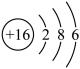
(4)元素周期表中,原子序数为16的硫元素的原子结构示意图如图,该原子在化学反应中易____ (填“得到”或“失去”)电子。说明元素的化学性质与原子的______ 关系密切。
| IA | 0 | |||||||
| 1 | 1 H 氢 1.008 | 2 He 氦 4.003 | ||||||
| IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)表中不同种元素最本质的区别是___________(填序号):
| A.相对原子质量不同 | B.中子数不同 | C.质子数不同 | D.电子数不同 |
| A.从左到右,各元素原子的电子层数相同 |
| B.从左到右,各元素原子的原子序数依次增加 |
| C.从左到右,各元素原子的最外层电子数相同 |

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】航天器应用的新型镁锂合金材料是由西安四方超轻材料有限公司自主研发。
(1)镁锂合金硬度比其纯金属的硬度__________ 。(填“大”或“小”)

(2)图1为镁在元素周期表中的部分信息,则镁的相对原子质量为__________ 。
(3)图2为几种粒子的结构示意图,其中属于同种元素的是___________ (填序号),与镁元素化学性质相似的是__________ (填序号)。镁元素与E元素形成化合物的化学式为__________ 。
(4)锂原子(Li)在反应中易失去1个电子形成锂离子,写出锂离子的符号:__________ 。
(1)镁锂合金硬度比其纯金属的硬度

(2)图1为镁在元素周期表中的部分信息,则镁的相对原子质量为
(3)图2为几种粒子的结构示意图,其中属于同种元素的是
(4)锂原子(Li)在反应中易失去1个电子形成锂离子,写出锂离子的符号:
您最近一年使用:0次