实验室欲将100g质量分数为10%的氯化钠溶液:
(1)完成该实验,下图中有一种仪器不必用到,请写出该仪器的名称___________ ;
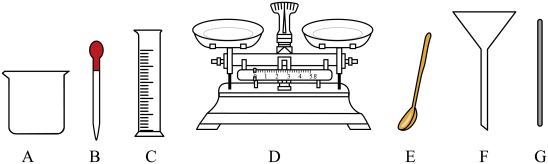
(2)计算:需要称氯化钠___________ g,量取水的体积__________ (水的密度1g/mL);
(3)称量:在称量时,发现托盘天平的指针向左偏转,此时应该______________ ;
(4)量取:量取蒸馏水时选择量筒规格:___________ (填“20mL”或“50mL”或“100mL”);
(5)溶解装瓶贴标签后检测发现,所配溶液溶质的质量分数偏小的是___________ 。
(1)完成该实验,下图中有一种仪器不必用到,请写出该仪器的名称

(2)计算:需要称氯化钠
(3)称量:在称量时,发现托盘天平的指针向左偏转,此时应该
| A.增加适量氯化钠 | B.减少适量氯化钠 |
| C.增加砝码 | D.调节天平平衡螺母 |
(4)量取:量取蒸馏水时选择量筒规格:
(5)溶解装瓶贴标签后检测发现,所配溶液溶质的质量分数偏小的是
| A.量取蒸馏水仰视读数 |
| B.量取蒸馏水时俯视读数 |
| C.配好的溶液转移过程中洒落 |
| D.称好的氯化钠转移至烧杯时,氯化钠固体洒落 |
更新时间:2024-02-05 13:33:06
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将30g固体物质x(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得0℃、t1℃、t2℃、t3℃、t4℃时烧杯中溶液的质量分别如图中A、B、C、D、E点所示,回答下列问题:

(1)A、B、C、D四点对应的溶液中可能属于饱和溶液的是_________ (填序号);
(2)t2℃时,物质x的溶解度是_________ ;
(3)E点对应的溶液的溶质质量分数是_________ ;
(4)B点对应溶液恒温蒸发2g水析出x的质量_________ (填“>”、“<”或“=”)C点对应溶液恒温蒸发2g水析出x的质量。

(1)A、B、C、D四点对应的溶液中可能属于饱和溶液的是
(2)t2℃时,物质x的溶解度是
(3)E点对应的溶液的溶质质量分数是
(4)B点对应溶液恒温蒸发2g水析出x的质量
您最近一年使用:0次
【推荐2】下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | |
(1)下图中,甲可表示
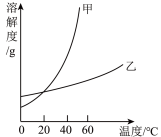
(2)40℃时,两种物质的饱和溶液中,溶质质量分数较小的物质是
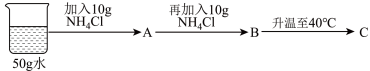
(3)20℃时,按图示操作:B中的溶液是
您最近一年使用:0次
【推荐1】化学实验室常需配制一定溶质质量分数的溶液。
(1)实验室配制溶液有如下步骤:(已知20℃时氯化钾的溶解度是34g)
①计算:20℃时,将67g的氯化钾饱和溶液稀释为20%,需加水_______ mL。
②量取:用量筒量取水倒入烧杯中,提供的量筒规格有10mL、20mL、50mL,应该选择____ mL的量筒。
③混匀:用搅拌,使溶液混合均匀。
(2)根据如图溶解度曲线及所学知识,判断下列说法正确的是_______ 。

A .已知40℃时,硝酸钾的溶解度是64g,表示100g硝酸钾饱和溶液中含64g硝酸钾
B. 温度越高,配制成的氢氧化钙饱和溶液浓度越大
C. 硝酸钾中混有少量氯化钾,可用冷却热饱和溶液的方法提纯
D .60℃时,将等质量的硝酸钾、氯化钾两种物质分别配制成饱和溶液,硝酸钾需要水的质量大于氯化钾
(1)实验室配制溶液有如下步骤:(已知20℃时氯化钾的溶解度是34g)
①计算:20℃时,将67g的氯化钾饱和溶液稀释为20%,需加水
②量取:用量筒量取水倒入烧杯中,提供的量筒规格有10mL、20mL、50mL,应该选择
③混匀:用搅拌,使溶液混合均匀。
(2)根据如图溶解度曲线及所学知识,判断下列说法正确的是

A .已知40℃时,硝酸钾的溶解度是64g,表示100g硝酸钾饱和溶液中含64g硝酸钾
B. 温度越高,配制成的氢氧化钙饱和溶液浓度越大
C. 硝酸钾中混有少量氯化钾,可用冷却热饱和溶液的方法提纯
D .60℃时,将等质量的硝酸钾、氯化钾两种物质分别配制成饱和溶液,硝酸钾需要水的质量大于氯化钾
您最近一年使用:0次
【推荐2】酸、碱、盐在生产生活中具有广泛的用途。
(l)用氢氧化钠固体配制10%的氢氧化钠溶液:
①过程中需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要________ 。
②下列操作正确的是_______ (填字母)。
A称量氢氧化钠固体时,在托盘天平的左右托盘上垫上相同大小的纸
B将准确称量的氢氧化钠固体放入装有水的烧杯中溶解
C用玻璃棒搅拌,加快氢氧化钠溶解速率
D将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如图实验,请回答下列问题:

① 反应I 的化学方程式为_______ 。
② 白色沉淀C是_______ (填化学式)。
③ 原固体粉末中一定不含_______ (填化学式)。
(l)用氢氧化钠固体配制10%的氢氧化钠溶液:
①过程中需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要
②下列操作正确的是
A称量氢氧化钠固体时,在托盘天平的左右托盘上垫上相同大小的纸
B将准确称量的氢氧化钠固体放入装有水的烧杯中溶解
C用玻璃棒搅拌,加快氢氧化钠溶解速率
D将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如图实验,请回答下列问题:

① 反应I 的化学方程式为
② 白色沉淀C是
③ 原固体粉末中一定不含
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】很多同学都喜欢既别致又实用的叶脉书签,其制作方法如下:首先选取大小适当、稍老一些的树叶(如桂树叶)放在烧杯中,加入100g溶质质量分数为12%的氢氧化钠溶液,加热煮沸10—15分钟(不搅拌),取出,冲洗,将叶片压平,最后系上各色丝带,漂亮的叶脉书签便做好了。
(1)在制作过程中,需称取12g氢氧化钠固体。由于氢氧化钠易潮解,称取时,要将其放在_____ 中,称量时若发现天平指针向左偏转,则应 _____ (填序号);
A 增加砝码 B 移动游码 C 取出一些氢氧化钠固体 D 再加一些氢氧化钠固体
(2)量取88ml的蒸馏水,量取时最好选用_____ (填“10mL”“100mL”或“500nL”)量筒,读数时视线应 _____ ;
(3)小明将称好的氢氧化钠固体放入盛有88mL水的量筒中,边加边用玻璃棒搅拌,完全溶解后得到了100g12%的氢氧化钠溶液。小明的操作是否正确?_____ 为什么? _____ ;
(4)小芳用如图所示的装置制作叶脉书签,请指出图中两处错误:

①_____ ;
②_____ 。
(1)在制作过程中,需称取12g氢氧化钠固体。由于氢氧化钠易潮解,称取时,要将其放在
A 增加砝码 B 移动游码 C 取出一些氢氧化钠固体 D 再加一些氢氧化钠固体
(2)量取88ml的蒸馏水,量取时最好选用
(3)小明将称好的氢氧化钠固体放入盛有88mL水的量筒中,边加边用玻璃棒搅拌,完全溶解后得到了100g12%的氢氧化钠溶液。小明的操作是否正确?
(4)小芳用如图所示的装置制作叶脉书签,请指出图中两处错误:

①
②
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】为抗击新冠肺炎疫情,过氧乙酸(CH3COOOH)消 毒剂被广泛使用。请回答下列问题:
(1)一个过氧乙酸分子中含有______ 个原子。
(2)过氧乙酸中碳、氢、氧三种元素的质量比为______ (填最简整数比)。
(3)过氧乙酸用于消毒时,要将原液稀释至 0.2%-0.5%之间。某同学欲用溶质质量分数为 15%的过氧乙酸溶液配制 1000g溶质质量分数为 0.3%的 过氧乙酸溶液,回答下列问题:
①需要溶质质量分数为 15%的 过氧乙酸溶液的质量为______ g。
②若用量筒量取水时仰视读数,而其它操作均正确,则所配制的过氧乙酸溶液溶质的质量分数______ (选填“大于”“小于”或“等于”)0.3%。
(1)一个过氧乙酸分子中含有
(2)过氧乙酸中碳、氢、氧三种元素的质量比为
(3)过氧乙酸用于消毒时,要将原液稀释至 0.2%-0.5%之间。某同学欲用溶质质量分数为 15%的过氧乙酸溶液配制 1000g溶质质量分数为 0.3%的 过氧乙酸溶液,回答下列问题:
①需要溶质质量分数为 15%的 过氧乙酸溶液的质量为
②若用量筒量取水时仰视读数,而其它操作均正确,则所配制的过氧乙酸溶液溶质的质量分数
您最近一年使用:0次
【推荐2】如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:

(1)A、B两种物质在______ ℃时溶解度相同。
(2)t2℃时,将30gB物质加入到50g水中,充分溶解,所得溶液的质量为______ g。
(3)将t2℃时三种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数由大到小的顺序为______ (填字母)。
(4)已知t1℃时,A物质的溶解度为35g。现有A、B的固体混合物80g,为了得到其中的A,设计如图实验:

原混合物中A的质量分数为______ 。
(5)某同学配制50g溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为______ g。
②配制过程有以下步骤:a.称量及量取b.计算c.溶解d.装瓶贴标签,正确顺序是______ (填序号)。

(1)A、B两种物质在
(2)t2℃时,将30gB物质加入到50g水中,充分溶解,所得溶液的质量为
(3)将t2℃时三种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数由大到小的顺序为
(4)已知t1℃时,A物质的溶解度为35g。现有A、B的固体混合物80g,为了得到其中的A,设计如图实验:

原混合物中A的质量分数为
(5)某同学配制50g溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为
②配制过程有以下步骤:a.称量及量取b.计算c.溶解d.装瓶贴标签,正确顺序是
您最近一年使用:0次
【推荐3】(1)水是生命之源,爱护水资源是每个公民应尽的责任。
①天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化。其中单一操作相对净化程度较高的是_________ ;
②测得某地河水pH为7.4,可知该河水水样呈_____ 性;为了除去河水中的臭味和颜色,可以加入________ 进行吸附;
③硬水给生活和生产带来很多不利的影响,生活中可用______ 来区分硬水和软水;
④生活中通过_________ 的方法可以降低水的硬度。
(2)溶液在日常生活、农业和科学研究中具有广泛的用途。下图是某同学配制50g6%氯化钠溶液的实验操作示意图。

①该实验正确的操作顺序是______ (填字母);
②实验过程中,玻璃棒的作用是____________ ;
③该同学在用量筒量取水时仰视读数,这样会使所配制的溶液中溶质质量分数________ (填“>”、“<”或“=”)6%。
①天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化。其中单一操作相对净化程度较高的是
②测得某地河水pH为7.4,可知该河水水样呈
③硬水给生活和生产带来很多不利的影响,生活中可用
④生活中通过
(2)溶液在日常生活、农业和科学研究中具有广泛的用途。下图是某同学配制50g6%氯化钠溶液的实验操作示意图。

①该实验正确的操作顺序是
②实验过程中,玻璃棒的作用是
③该同学在用量筒量取水时仰视读数,这样会使所配制的溶液中溶质质量分数
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答溶液的相关问题。
【研究一】:小刚做静脉点滴时发现,医用葡萄糖溶液的溶质质量分数为5%,他应用化学课学到的知识,配置了一份200g溶质质量分数为5%的葡萄糖溶液,步骤如下:
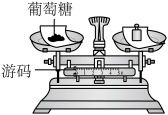
(1)计算:实验中需要称量葡萄糖的质量为___________ g。
(2)称量:实验中选用与需要称量葡萄糖质量相等的砝码,游码未归零,位置如图所示。若其他操作正确,则配置溶液中葡萄糖的质量分数___________ 5%(选填“>”“=”或“<”)。
(3)量取:量取所需体积的水,应选择___________ mL(选填“100”“250”或“500”)量筒。
(4)溶解:需要用到玻璃棒和烧杯,玻璃棒的作用是___________ 。
(5)装瓶:把配好的溶液倒入细口瓶中,贴上标签。
【研究二】:小刚从家中冰箱中取出一杯含有葡萄糖晶体的溶液,常温放置一段时间,现象如图11所示(假设水不蒸发)。
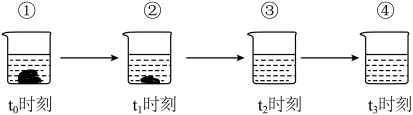
(1)由如图的现象,推测葡萄糖的溶解度受温度影响的变化规律___________ 。
(2)上述四个烧杯,一定为饱和溶液的是___________ (选填“①”、“②”,“③”或“④”,下同)。溶液质量最小的是___________ 。
【研究一】:小刚做静脉点滴时发现,医用葡萄糖溶液的溶质质量分数为5%,他应用化学课学到的知识,配置了一份200g溶质质量分数为5%的葡萄糖溶液,步骤如下:

(1)计算:实验中需要称量葡萄糖的质量为
(2)称量:实验中选用与需要称量葡萄糖质量相等的砝码,游码未归零,位置如图所示。若其他操作正确,则配置溶液中葡萄糖的质量分数
(3)量取:量取所需体积的水,应选择
(4)溶解:需要用到玻璃棒和烧杯,玻璃棒的作用是
(5)装瓶:把配好的溶液倒入细口瓶中,贴上标签。
【研究二】:小刚从家中冰箱中取出一杯含有葡萄糖晶体的溶液,常温放置一段时间,现象如图11所示(假设水不蒸发)。

(1)由如图的现象,推测葡萄糖的溶解度受温度影响的变化规律
(2)上述四个烧杯,一定为饱和溶液的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】溶液对动植物的生理活动和人类的生产具有重要意义、室温下,某实验小组欲配制50g溶质质量分数为10%的碳酸钠溶液,按如下图所示步骤操作。

请回答以下问题:
(1)计算:需 粉末
粉末______ g,水______ mL(室温时,水的密度约为 ),量取水时应选用量筒规格为
),量取水时应选用量筒规格为______ mL。
(2)称量:调节天平平衡后称量所需的碳酸钠粉末时,发现托盘天平的指针偏左,此时应______(填序号)。
(3)配制溶液:用量筒量取所需的水,倒入盛有 的烧杯中,用
的烧杯中,用______ 搅拌,其目的是______ ,这样得到的溶液即是50g溶质质量分数为10%的 溶液。
溶液。
(4)若用量筒量取水时仰视读数,其他操作均正确,则所配碳酸钠溶液的溶质质量分数______ (填“偏大”“偏小”或“无影响”下同),称量时若发现砝码生锈,则所配溶液的溶质质量分数______ 。

请回答以下问题:
(1)计算:需
 粉末
粉末 ),量取水时应选用量筒规格为
),量取水时应选用量筒规格为(2)称量:调节天平平衡后称量所需的碳酸钠粉末时,发现托盘天平的指针偏左,此时应______(填序号)。
| A.调节天平平衡螺母 | B.增加适量 | C.减少适量 |
(3)配制溶液:用量筒量取所需的水,倒入盛有
 的烧杯中,用
的烧杯中,用 溶液。
溶液。(4)若用量筒量取水时仰视读数,其他操作均正确,则所配碳酸钠溶液的溶质质量分数
您最近一年使用:0次
【推荐3】水是人类生产、生活中不可缺少的重要物质,更是人类文明延续和发展的重要物质保障条件。
(1)在自来水厂中常常使用活性炭等净化水,其利用了活性炭的___________ 性。
(2)化学实验室中经常用到水,如溶液的配制。配制100g溶质质量分数为3%的氯化钠溶液,需要氯化钠质量为3g,需要水的质量为___________ g。
(3)水常用作物质溶解的溶剂。著名化学家侯德榜先生创立了联合制碱法,打破了外国势力对制碱技术的垄断。Na2CO3和NaCl是制碱法的主要原料,两种物质的溶解度曲线如图所示,试回答下列问题:

①t1℃时,Na2CO3的溶解度为___________ g。
②t1℃时,向25g水中加入6gNa2CO3固体,经搅拌充分溶解,所得溶液的质量是___________ g。
③将t2℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液均降温至t1℃,此时所得两溶液的溶质质量分数大小关系是___________ ,析出晶体质量更多的是___________ 。
(1)在自来水厂中常常使用活性炭等净化水,其利用了活性炭的
(2)化学实验室中经常用到水,如溶液的配制。配制100g溶质质量分数为3%的氯化钠溶液,需要氯化钠质量为3g,需要水的质量为
(3)水常用作物质溶解的溶剂。著名化学家侯德榜先生创立了联合制碱法,打破了外国势力对制碱技术的垄断。Na2CO3和NaCl是制碱法的主要原料,两种物质的溶解度曲线如图所示,试回答下列问题:

①t1℃时,Na2CO3的溶解度为
②t1℃时,向25g水中加入6gNa2CO3固体,经搅拌充分溶解,所得溶液的质量是
③将t2℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液均降温至t1℃,此时所得两溶液的溶质质量分数大小关系是
您最近一年使用:0次



