将20g表面生锈的铁钉(假设不含其它杂质)浸泡在100g溶质质量分数为7.3%的稀盐酸中充分反应,观察到铁锈已完全消失,但未见气泡产生。假设溶液中只发生了如下反应: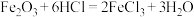
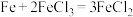 ,反应停止后,取出光亮的铁钉洗涤、干燥、称量,质量为12.8g。计算:
,反应停止后,取出光亮的铁钉洗涤、干燥、称量,质量为12.8g。计算:
(1)氧化铁中铁元素与氧元素的质量比。
(2)所得溶液中溶质的质量分数。
(3)运用元素守恒的方法计算原锈铁钉中铁元素的质量分数
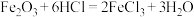
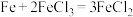 ,反应停止后,取出光亮的铁钉洗涤、干燥、称量,质量为12.8g。计算:
,反应停止后,取出光亮的铁钉洗涤、干燥、称量,质量为12.8g。计算:(1)氧化铁中铁元素与氧元素的质量比。
(2)所得溶液中溶质的质量分数。
(3)运用元素守恒的方法计算原锈铁钉中铁元素的质量分数
更新时间:2024-04-04 05:45:06
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某石灰石样品(主要成分是碳酸钙)18.0g,将其充分煅烧后剩余固体质量为11.4g,请回答下列问题:(已知:碳酸钙高温分解生成氧化钙固体和二氧化碳。)
(1)CaCO3中钙元素质量分数_______ 。
(2)列式计算生成氧化钙的质量。
(1)CaCO3中钙元素质量分数
(2)列式计算生成氧化钙的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】工业上高温煅烧石灰石(主要成分CaCO3)可制得生石灰(CaO)和二氧化碳。某兴趣小组为测定石灰石样品中的碳酸钙的质量分数,进行实验(杂质不参加反应),测得相关数据如图所示:

(1)反应生成的二氧化碳的质量为_______ 。
(2)计算该样品中碳酸钙的质量分数(写出计算过程)。

(1)反应生成的二氧化碳的质量为
(2)计算该样品中碳酸钙的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某兴趣实验小组在实验室发现盛有固体氢氧化钠的试剂瓶破裂,而瓶盖处有“白色”状固体物质存在。
(1)根据所学知识推断,该“白色”状物质中含有碳酸钠,依据是___________ (用文字表达)。
(2)为了测定白色固体中氢氧化钠的含量,兴趣小组分别取四份不同质量的盐酸,分别加入到四个盛有14.6 g白色固体的烧杯中进行实验,所得数据如下表:
试计算该固体样品中氢氧化钠的质量分数(写出计算过程,结果精确到0.1%)。
(1)根据所学知识推断,该“白色”状物质中含有碳酸钠,依据是
(2)为了测定白色固体中氢氧化钠的含量,兴趣小组分别取四份不同质量的盐酸,分别加入到四个盛有14.6 g白色固体的烧杯中进行实验,所得数据如下表:
实验组 | 第1组 | 第2组 | 第3组 | 第4组 |
加入盐酸的质量/g | 14.6 | 29.2 | 43.8 | 50.8 |
生成气体的质量/g | 0 | 2.2 | 4.4 | 4.4 |
试计算该固体样品中氢氧化钠的质量分数(写出计算过程,结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】金属材料包括纯金属和合金,回答下列金属和合金的问题。
(1)生铁和钢都是铁合金,它们中含碳量较少的是_____________;
(2)铁生锈是铁与空气中的____________共同发生的复杂的化学反应;
(3)高温下,用一氧化碳和赤铁矿(主要成分是Fe2O3)反应来冶炼生铁,化学方程式为___________;
(4)工业上用含Fe2O380%的赤铁矿石100t,理论上最多得到纯铁的质量是_____________ t。
(1)生铁和钢都是铁合金,它们中含碳量较少的是_____________;
(2)铁生锈是铁与空气中的____________共同发生的复杂的化学反应;
(3)高温下,用一氧化碳和赤铁矿(主要成分是Fe2O3)反应来冶炼生铁,化学方程式为___________;
(4)工业上用含Fe2O380%的赤铁矿石100t,理论上最多得到纯铁的质量是_____________ t。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】小甲和小乙去巴蜀后山玩耍,发现了大理石样品。(其中杂质既不溶于水也不与盐酸反应,他们想测定该样品中碳酸钙的质量分数,选取了一块大理石样品,将其敲打粉碎后,称出6g放入烧杯内(烧杯质量为20g)。然后加入逐滴加入一定质量分数的稀盐酸至不再产生气泡为止,此时加入稀盐酸质量为50g,反应所需时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示请完成下列问题:

(1)实验结束时,理论上共放出二氧化碳的质量为____________ g。
(2)计算该石灰石样品中碳酸钙的质量分数及所加盐酸的质量分数。(保留到0.1%)。

(1)实验结束时,理论上共放出二氧化碳的质量为
(2)计算该石灰石样品中碳酸钙的质量分数及所加盐酸的质量分数。(保留到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】豆浆营养丰富被称为“植物奶”,其中含有的异黄酮(C15H10O2)具有防癌功能。
(1)异黄酮中氢、氧两种元素的质量比为______ (填最简比);
(2)11.1g异黄酮中碳元素的质量为______ g。
(1)异黄酮中氢、氧两种元素的质量比为
(2)11.1g异黄酮中碳元素的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某100gNaOH样品(该样品中含有杂质)中钠元素的质量分数为46%。
(1)NaOH中Na、O、H三种元素的质量比___________ 。
(2)NaOH中Na元素的质量分数___________ 。
(3)求该样品中NaOH的质量分数(杂质不含钠元素)。
(1)NaOH中Na、O、H三种元素的质量比
(2)NaOH中Na元素的质量分数
(3)求该样品中NaOH的质量分数(杂质不含钠元素)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】现有80g质量分数为10%的硝酸钠溶液,请列式计算:
(1)若向上述溶液中加入20g硝酸钠,全部溶解后,则所得溶液中溶质的质量分数为多少?
(2)若向上述溶液中加入20g水,则所得溶液中溶质的质量分数为多少?
(3)若将上述溶液蒸发掉20g水,无晶体析出,则所得溶液中溶质的质量分数多少?
(4)若使上述溶液中溶质的质量分数变为20%,则应再加入硝酸钠的质量为多少?
(1)若向上述溶液中加入20g硝酸钠,全部溶解后,则所得溶液中溶质的质量分数为多少?
(2)若向上述溶液中加入20g水,则所得溶液中溶质的质量分数为多少?
(3)若将上述溶液蒸发掉20g水,无晶体析出,则所得溶液中溶质的质量分数多少?
(4)若使上述溶液中溶质的质量分数变为20%,则应再加入硝酸钠的质量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】溶液在农业生产中有重要作用。董允坝已建成国家现代农业示范园区,已知某农户在种植有机蔬菜时常用溶质质量分数为10%~20%的氯化钠溶液来选种。该农户在温室中(20℃)配制出了饱和的的氯化钠溶液500克。
(1)若从溶液中取出50克,蒸干水分,得到了13.2克氯化钠固体。那么温室中这500g饱和的氯化钠溶液溶质质量分数为_________ 。
(2)如果要使剩下的饱和氯化钠溶液成为符合选种标准的溶液,该农户至少需要在饱和的氯化钠溶液中加入多少克水?(写出计算过程,结果精确到小数点后一位)
(1)若从溶液中取出50克,蒸干水分,得到了13.2克氯化钠固体。那么温室中这500g饱和的氯化钠溶液溶质质量分数为
(2)如果要使剩下的饱和氯化钠溶液成为符合选种标准的溶液,该农户至少需要在饱和的氯化钠溶液中加入多少克水?(写出计算过程,结果精确到小数点后一位)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】为测定某种贝壳中碳酸钙的含量,取12.5g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示。(已知杂质不参与反应也不溶于水)。

请计算:
(1)这种贝壳中碳酸钙的质量分数_______________ 。
(2)12.5g贝壳与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数_____ (写出计算过程)。

请计算:
(1)这种贝壳中碳酸钙的质量分数
(2)12.5g贝壳与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数
您最近一年使用:0次




